-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

摩熵咨询医药行业观察周报(2025.03.24-2025.03.30)
1.1总体概况
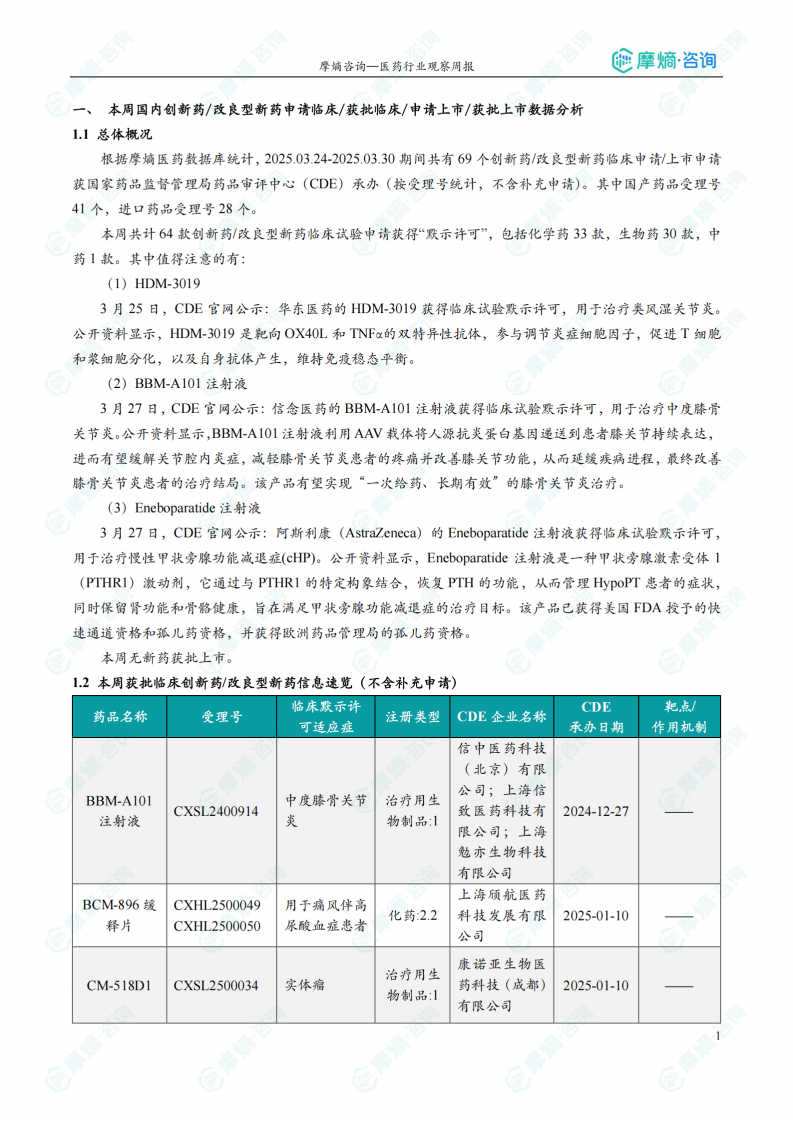
根据摩熵医药数据库统计,2025.03.24-2025.03.30期间共有69个创新药/改良型新药临床申请/上市申请获国家药品监督管理局药品审评中心(CDE)承办(按受理号统计,不含补充申请)。其中国产药品受理号41个,进口药品受理号28个。
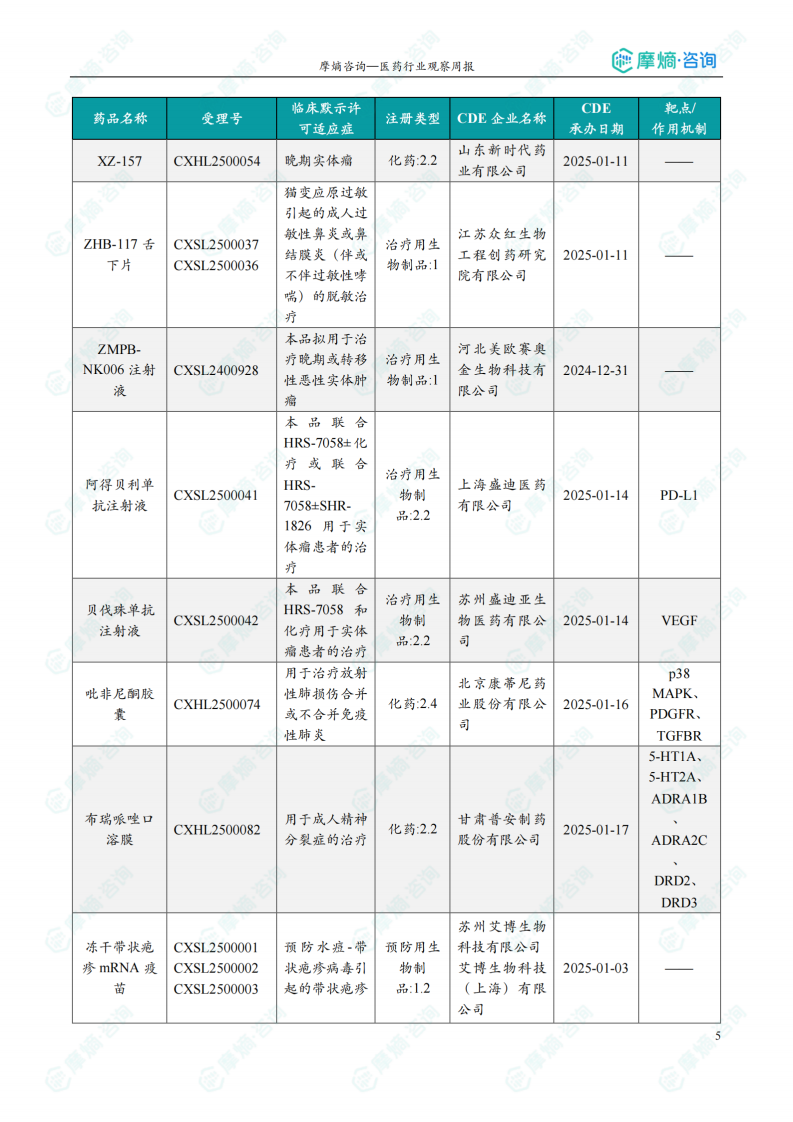
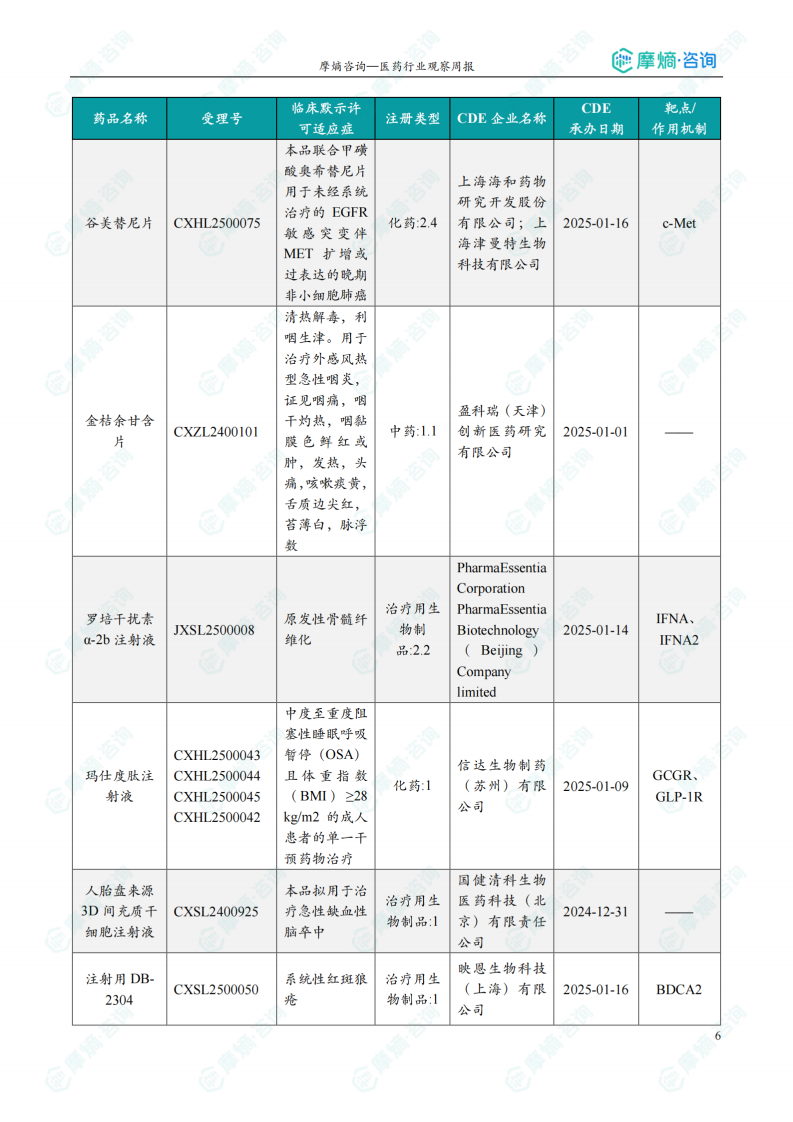
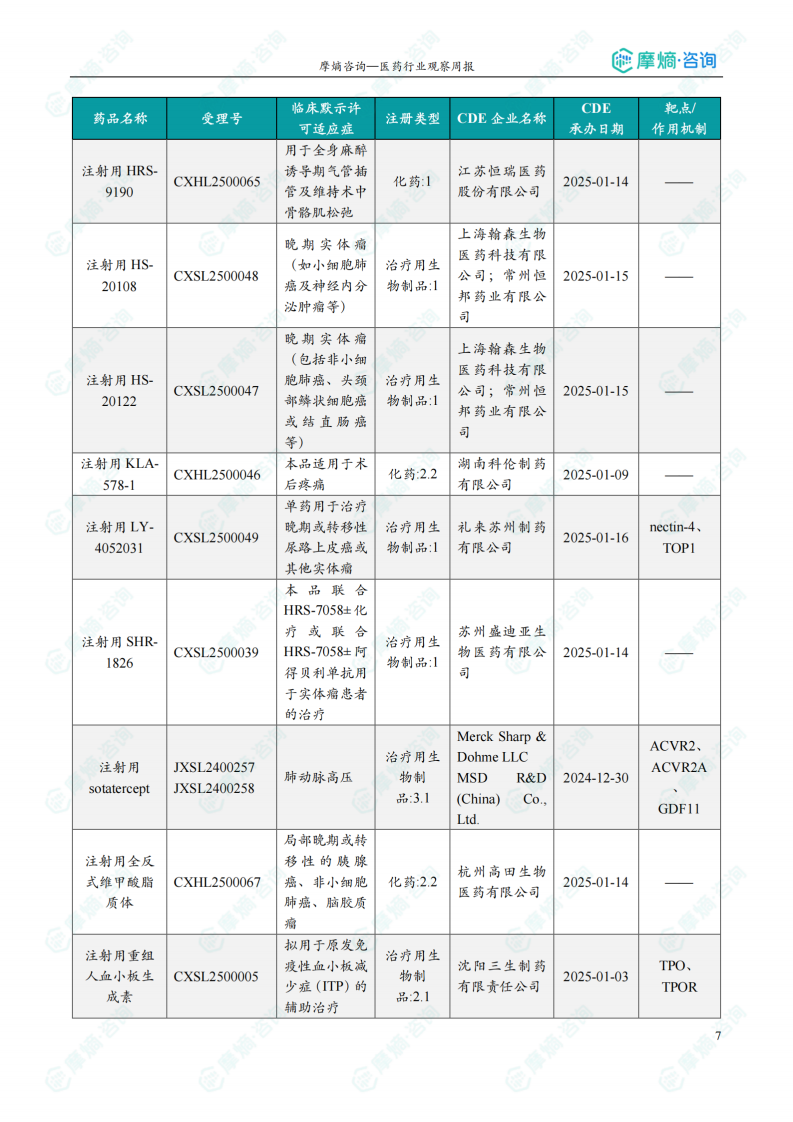
本周共计64款创新药/改良型新药临床试验申请获得“默示许可”,包括化学药33款,生物药30款,中药1款。其中值得注意的有:
(1)HDM-3019
3月25日,CDE官网公示:华东医药的HDM-3019获得临床试验默示许可,用于治疗类风湿关节炎。公开资料显示,HDM-3019是靶向OX40L和TNFα的双特异性抗体,参与调节炎症细胞因子,促进T细胞和浆细胞分化,以及自身抗体产生,维持免疫稳态平衡。
(2)BBM-A101注射液
3月27日,CDE官网公示:信念医药的BBM-A101注射液获得临床试验默示许可,用于治疗中度膝骨关节炎。公开资料显示,BBM-A101注射液利用AAV载体将人源抗炎蛋白基因递送到患者膝关节持续表达,进而有望缓解关节腔内炎症,减轻膝骨关节炎患者的疼痛并改善膝关节功能,从而延缓疾病进程,最终改善膝骨关节炎患者的治疗结局。该产品有望实现“一次给药、长期有效”的膝骨关节炎治疗。
(3)Eneboparatide注射液
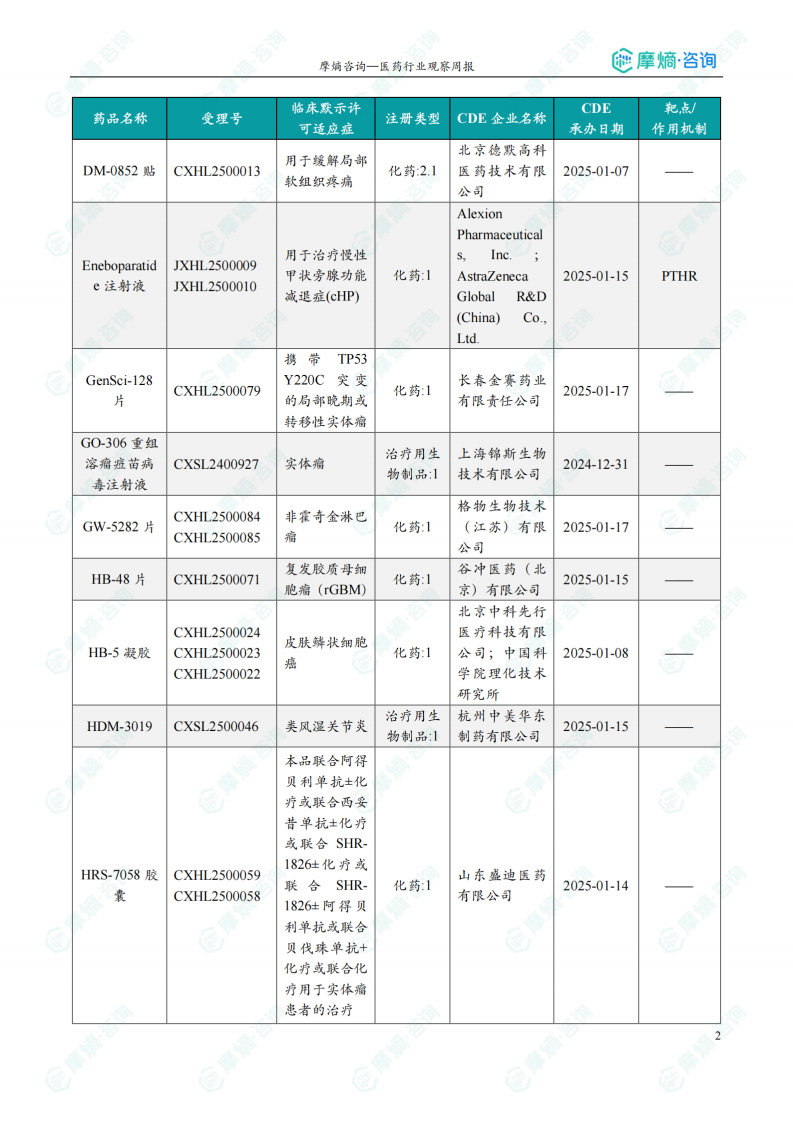
3月27日,CDE官网公示:阿斯利康(AstraZeneca)的Eneboparatide注射液获得临床试验默示许可,用于治疗慢性甲状旁腺功能减退症(cHP)。公开资料显示,Eneboparatide注射液是一种甲状旁腺激素受体1(PTHR1)激动剂,它通过与PTHR1的特定构象结合,恢复PTH的功能,从而管理HypoPT患者的症状,同时保留肾功能和骨骼健康,旨在满足甲状旁腺功能减退症的治疗目标。该产品已获得美国FDA授予的快速通道资格和孤儿药资格,并获得欧洲药品管理局的孤儿药资格。
本报告涉及: 相关药物:Eneboparatide注射液, 相关靶点:PTHR, 相关适应症:慢性甲状旁腺功能减退症 。
中心思想
本报告基于摩熵咨询医药行业观察周报(2025.03.24-2025.03.30)的数据,对国内外医药市场创新药、仿制药及相关政策法规进行了统计分析。核心观点如下:
- 创新药研发活跃: 国内外创新药研发持续推进,多个靶点药物获批临床或上市,展现出医药行业技术创新的蓬勃态势,尤其在肿瘤、神经系统疾病和罕见病领域。
- 仿制药市场竞争激烈: 国内仿制药市场竞争加剧,多个品种通过一致性评价,但市场集中度仍有待提高。
- 政策法规持续完善: 国家持续出台相关政策法规,规范医药行业发展,保障药品质量安全和患者权益。
主要内容
国内创新药/改良型新药研发进展
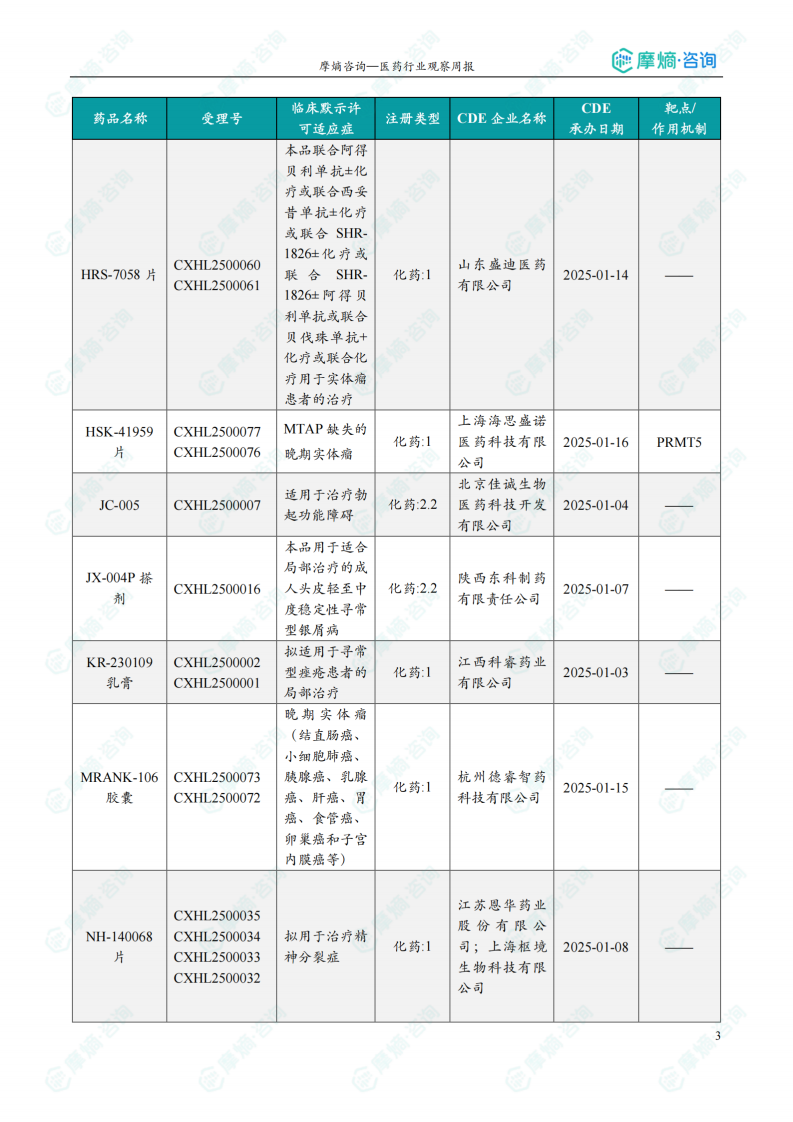
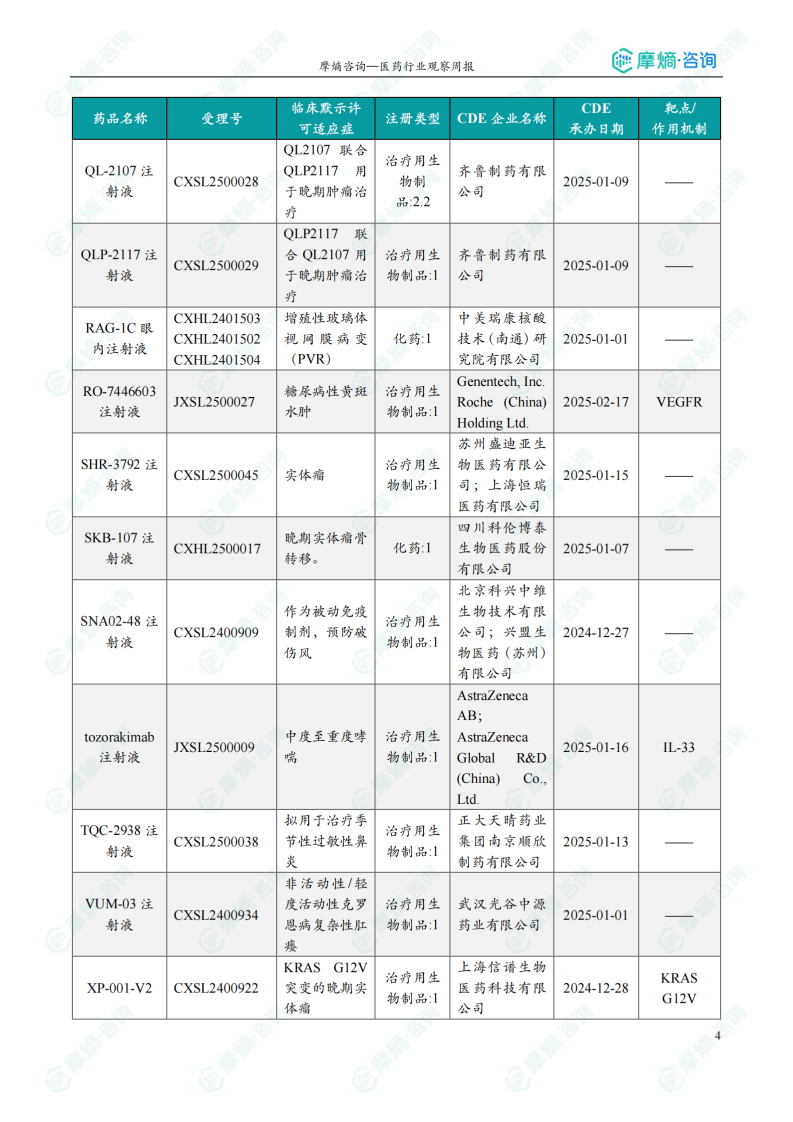
本周(2025.03.24-2025.03.30)共有69个创新药/改良型新药临床申请/上市申请获CDE承办,其中国产41个,进口28个。64款创新药/改良型新药临床试验申请获得“默示许可”,包括化学药33款,生物药30款,中药1款。值得关注的品种包括:华东医药的HDM-3019(靶向OX40L和TNFα的双特异性抗体,用于治疗类风湿关节炎)、信念医药的BBM-A101注射液(AAV载体递送人源抗炎蛋白基因,用于治疗中度膝骨关节炎)、阿斯利康的Eneboparatide注射液(甲状旁腺激素受体1激动剂,用于治疗慢性甲状旁腺功能减退症)。本周无新药获批上市。 数据显示,创新药研发在多个领域取得进展,但仍需关注临床试验结果及后续上市情况。
国内仿制药/生物类似物市场分析
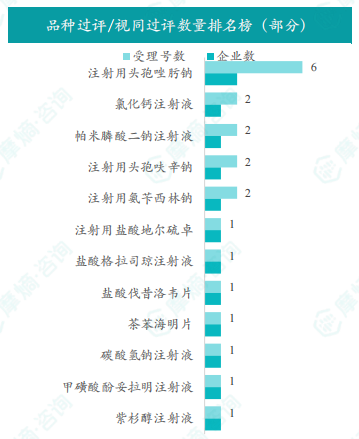
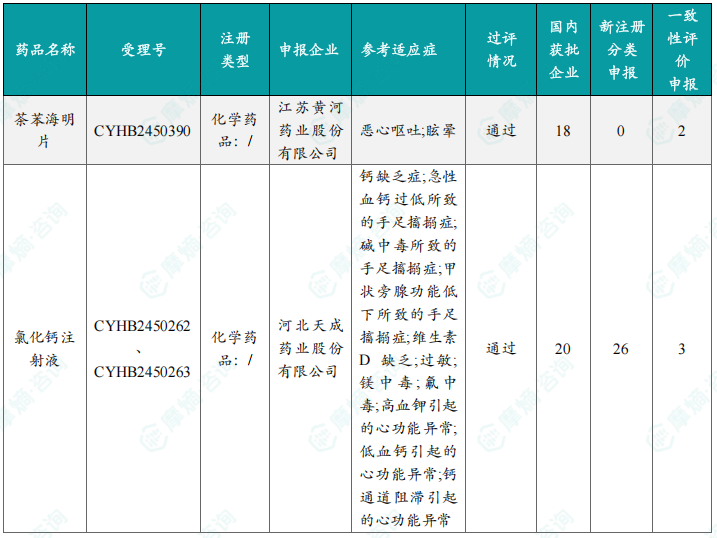
本周共有95项仿制药申报上市/申报临床获CDE承办,其中新注册分类上市申请受理号79项,新注册分类临床申请受理号9项,一致性评价申请7项。12个品种通过一致性评价(按受理号计21项),本周无视同通过一致性评价品种及生物类似物注册申报动态。通过一致性评价的品种主要为系统用抗感染药物,剂型主要为注射剂。注射用头孢唑肟钠过评受理号数量最多,达6个。河北天成药业股份有限公司过评品种数最多,达2种。数据表明,国内仿制药市场竞争激烈,一致性评价工作持续推进,但市场集中度仍需进一步提升。
国内医药大健康行业政策法规解读
本周发布的重点政策包括:国家药监局关于实施2025年版《中华人民共和国药典》的公告、关于发布推荐性卫生行业标准《X射线计算机体层成像儿童诊断参考水平标准》的通告、关于规范公立医疗机构预交金管理工作的通知。这些政策旨在规范药品生产、流通和使用,保障药品质量安全,降低儿童CT检查辐射风险,规范公立医院预交金管理,维护患者权益。这些政策的出台,体现了国家对医药行业监管力度的加强,以及对患者权益的重视。
全球创新药研发动态
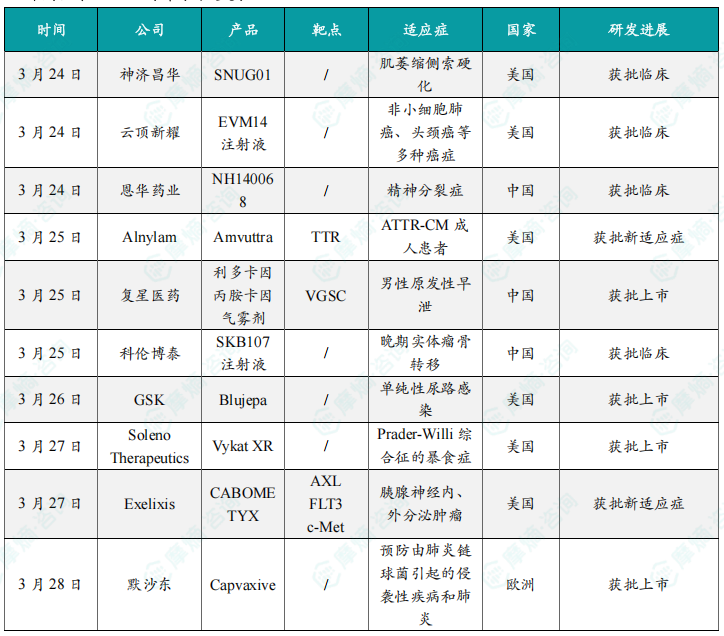
本周全球TOP10创新药研发进展涵盖多个领域,包括肿瘤、神经系统疾病、罕见病等。多个创新药物获批临床或上市,例如神济昌华的SNUG01(基因疗法,用于治疗肌萎缩侧索硬化)、云顶新耀的EVM14注射液(抗体偶联药物,用于治疗多种癌症)、Alnylam的Amvuttra(RNAi疗法,用于治疗ATTR-CM)、复星医药的利多卡因丙胺卡因气雾剂(用于治疗男性原发性早泄)等。此外,多个临床试验取得积极结果,例如Beam Therapeutics的碱基编辑疗法BEA M-101在镰状细胞病治疗中展现潜力,强生Rybrevant/Lazcluze组合在EGFR突变肺癌治疗中降低死亡风险,BioNTech双抗BNT327联合化疗在小细胞肺癌治疗中展现高疾病控制率等。这些进展表明全球创新药研发持续活跃,新疗法不断涌现,为患者带来新的治疗希望。
总结
本报告对2025年3月24日至30日一周内国内外医药市场进行了数据分析,涵盖创新药、仿制药研发进展以及相关政策法规。数据显示,国内外创新药研发持续活跃,多个新药获批临床或上市,展现出医药行业技术创新的蓬勃态势。国内仿制药市场竞争加剧,一致性评价工作持续推进。国家持续出台相关政策法规,规范医药行业发展,保障药品质量安全和患者权益。 未来,医药行业需持续关注创新药研发进展、仿制药市场竞争以及政策法规变化,以推动行业健康可持续发展。 本报告数据来源于摩熵咨询医药数据库,更详细的数据及分析可通过摩熵医药数据库或联系摩熵医药客服获取。
-

摩熵咨询医药行业观察周报(2026.04.27-2026.05.03)
-

2026年4月仿制药月报
-

2026年4月全球在研新药月报
-

2026年4月摩熵医药健康投融资&交易月报
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送