-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

摩熵咨询医药行业观察周报(2025.02.17-2025.02.23)
1.1总体概况
根据摩熵数据统计,2025.02.17-2025.02.23期间共有57个创新药/改良型新药临床申请/上市申请获国家药品监督管理局药品审评中心(CDE)承办(按受理号统计,不含补充申请)。其中国产药品受理号46个,进口药品受理号11个。
本周共计51款创新药/改良型新药临床试验申请获得“默示许可”,包括化学药21款,生物药30款,无中药。其中值得注意的有:
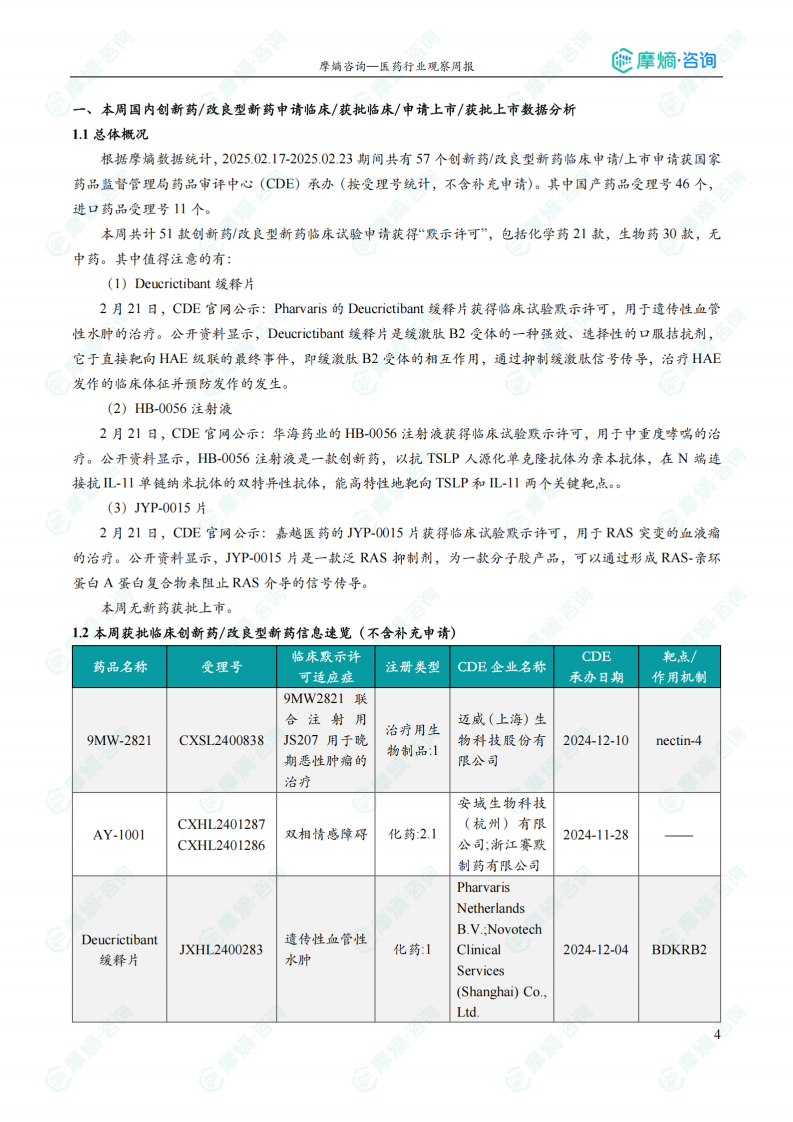
(1)Deucrictibant缓释片
2月21日,CDE官网公示:Pharvaris的Deucrictibant缓释片获得临床试验默示许可,用于遗传性血管性水肿的治疗。公开资料显示,Deucrictibant缓释片是缓激肽B2受体的一种强效、选择性的口服拮抗剂,它于直接靶向HAE级联的最终事件,即缓激肽B2受体的相互作用,通过抑制缓激肽信号传导,治疗HAE发作的临床体征并预防发作的发生。
(2)HB-0056注射液
2月21日,CDE官网公示:华海药业的HB-0056注射液获得临床试验默示许可,用于中重度哮喘的治疗。公开资料显示,HB-0056注射液是一款创新药,以抗TSLP人源化单克隆抗体为亲本抗体,在N端连接抗IL-11单链纳米抗体的双特异性抗体,能高特性地靶向TSLP和IL-11两个关键靶点。
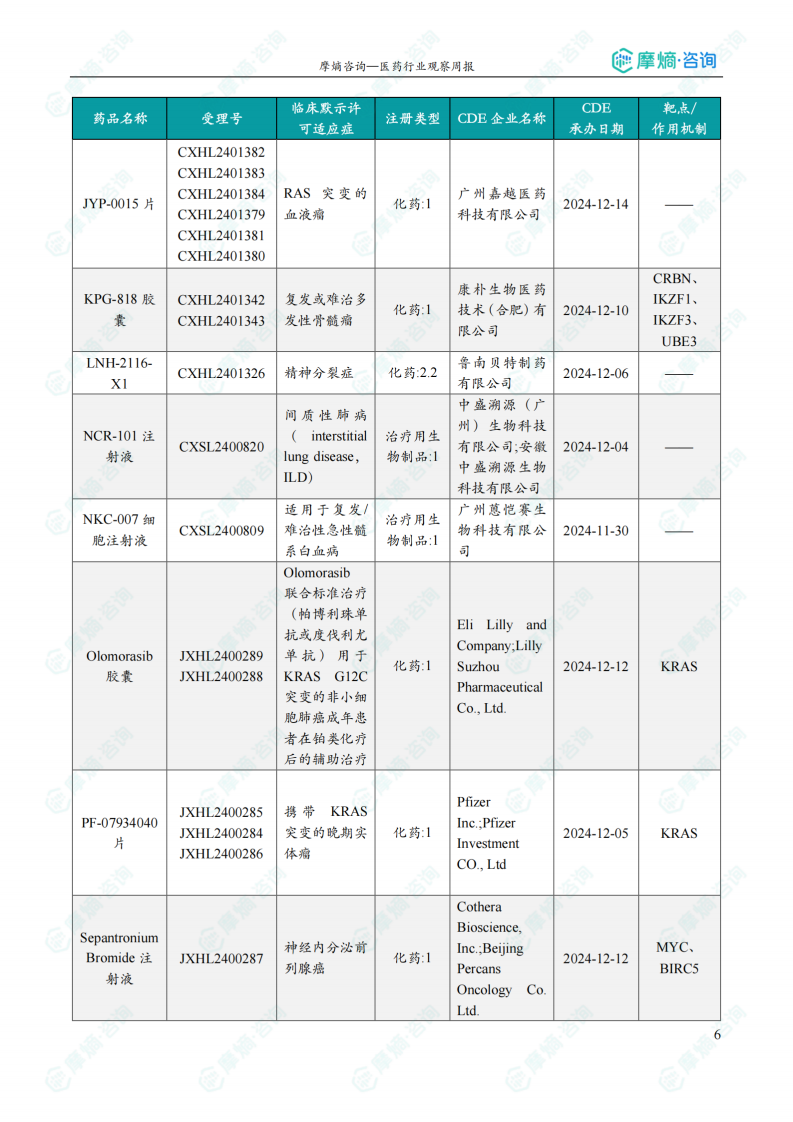
(3)JYP-0015片
2月21日,CDE官网公示:嘉越医药的JYP-0015片获得临床试验默示许可,用于RAS突变的血液瘤的治疗。公开资料显示,JYP-0015片是一款泛RAS抑制剂,为一款分子胶产品,可以通过形成RAS-亲环蛋白A蛋白复合物来阻止RAS介导的信号传导。
本报告涉及: 相关药物:9MW-2821, 相关靶点:nectin-4, 相关适应症:晚期恶性肿瘤 。
中心思想
本报告基于摩熵咨询2025年2月17日至2月23日医药行业观察周报数据,对国内外创新药、改良型新药及仿制药的研发、审批和上市情况进行统计分析,并对同期医药大健康行业政策法规进行总结。报告核心观点如下:
国内创新药研发审批加速,全球研发竞争激烈
国内创新药/改良型新药研发审批呈现加速态势,本周共有57个创新药/改良型新药临床申请/上市申请获受理,其中默示许可达51个,涵盖化学药和生物药。然而,本周无新药获批上市,显示出新药上市仍面临挑战。全球创新药研发竞争激烈,多家药企在研产品取得积极进展,例如Galderma的白介素-31受体靶向单抗获批上市,吉利德的Lenacapavir获批用于治疗多重耐药HIV-1感染等。同时,部分临床试验也公布了积极或失败的结果,反映出研发过程中的风险与机遇并存。
国内仿制药一致性评价稳步推进,政策法规持续完善
国内仿制药一致性评价稳步推进,本周共有96项仿制药申报上市/申报临床获受理,1个品种通过一致性评价。医药大健康行业政策法规持续完善,本周发布了多个重要政策文件,涉及医疗器械注册证书注销、非处方药转换以及中药材标准等方面,旨在规范市场秩序,保障药品安全有效。
主要内容
国内创新药/改良型新药研发及审批情况分析
国内创新药研发审批概况
本周(2025.02.17-2025.02.23)CDE共受理57个创新药/改良型新药临床申请/上市申请(不含补充申请),其中国产药品46个,进口药品11个。51款创新药/改良型新药临床试验申请获得“默示许可”,包括化学药21款,生物药30款。值得关注的是Pharvaris的Deucrictibant缓释片、华海药业的HB-0056注射液和嘉越医药的JYP-0015片均获得临床试验默示许可,分别用于治疗遗传性血管性水肿、中重度哮喘和RAS突变的血液瘤。本周无新药获批上市。
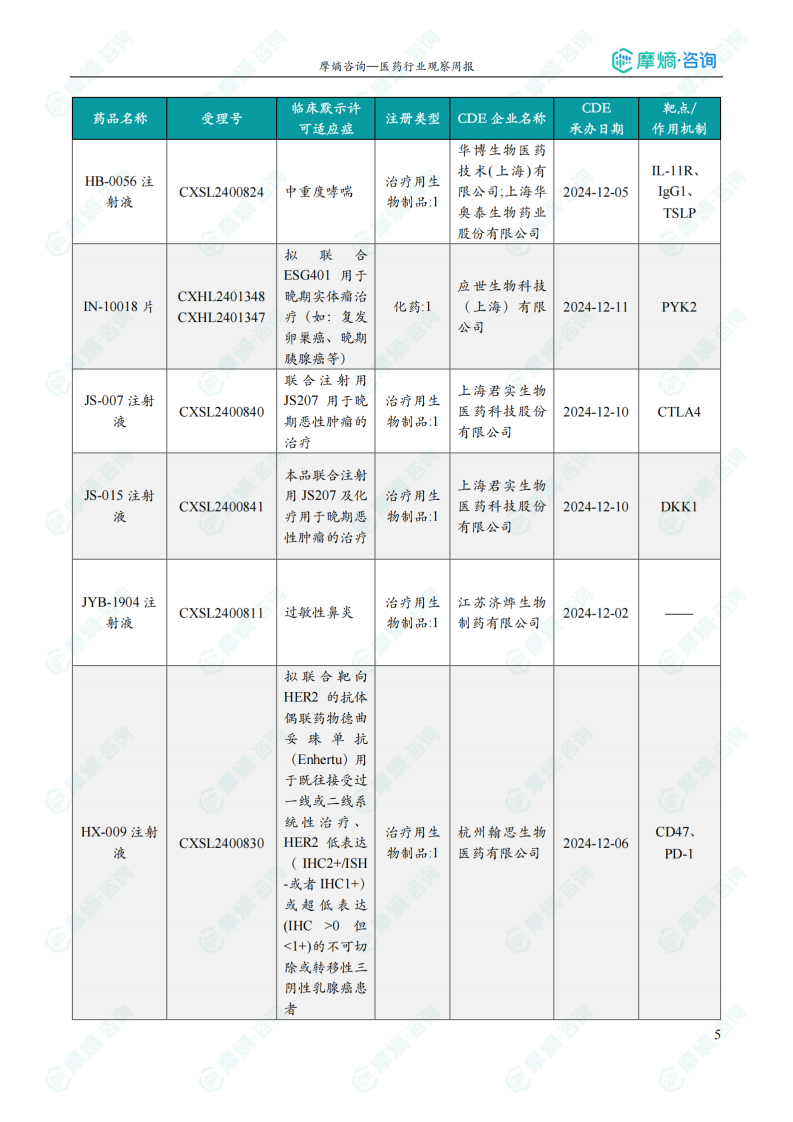
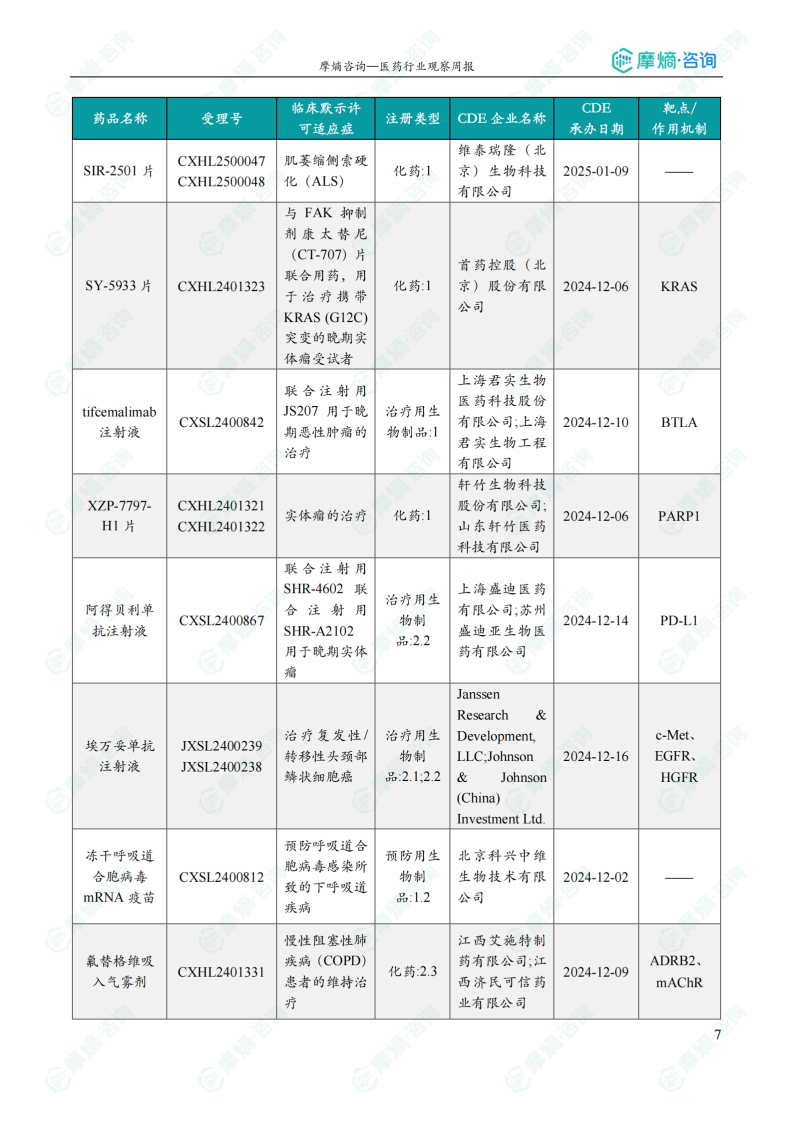
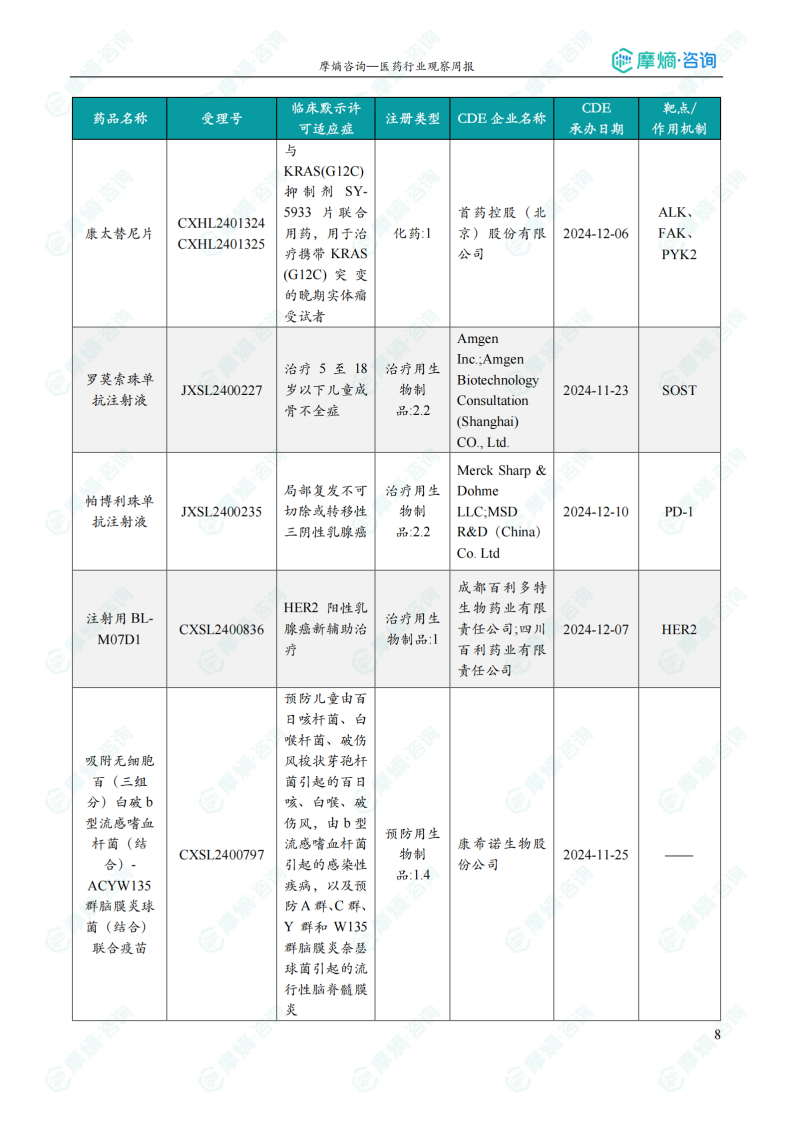
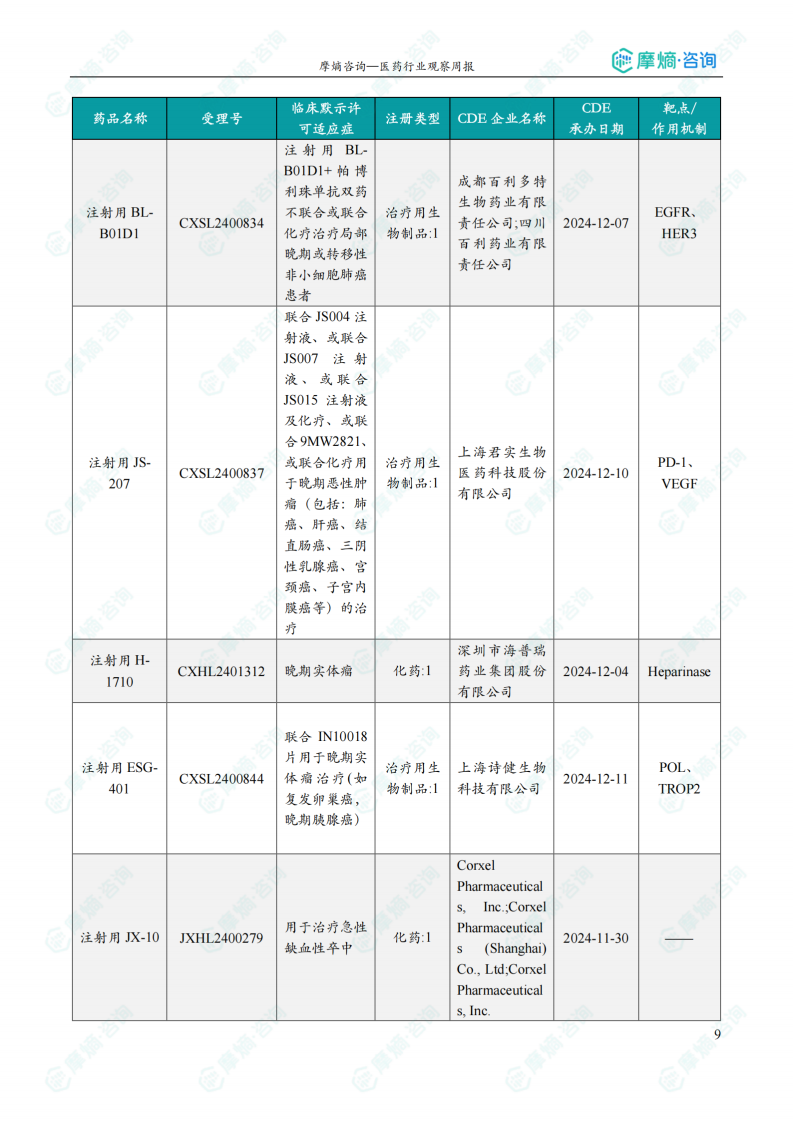
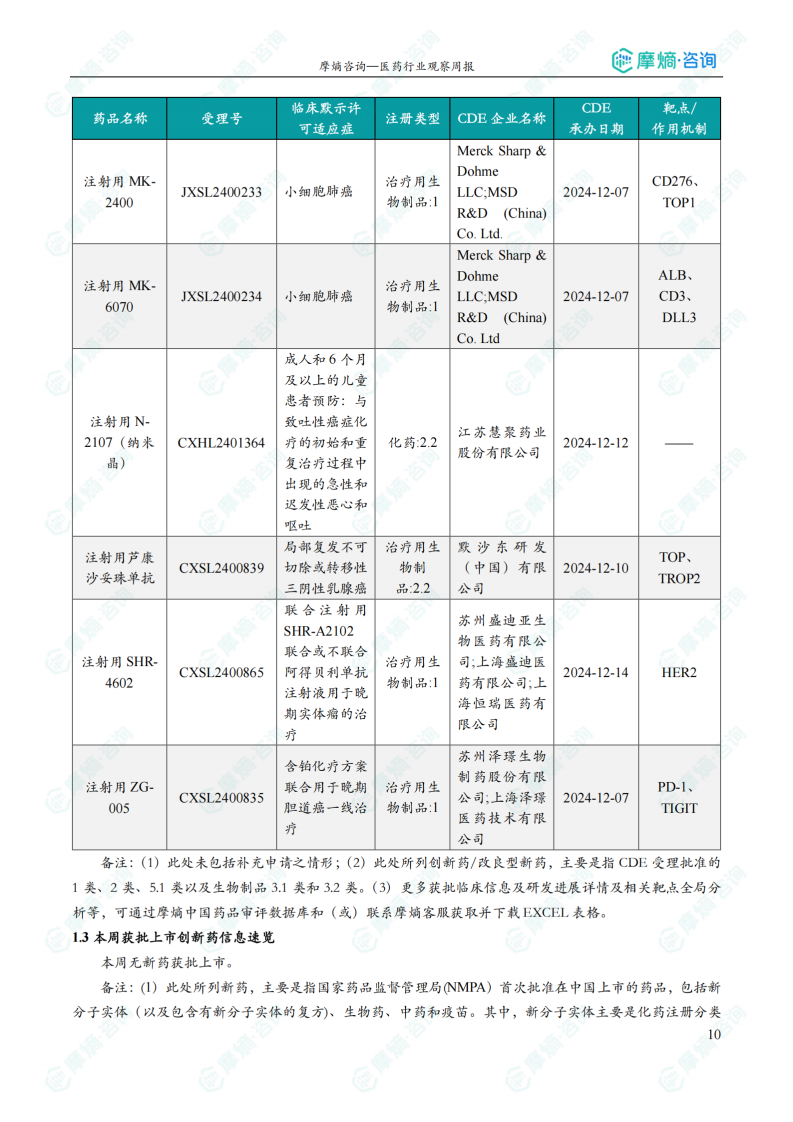
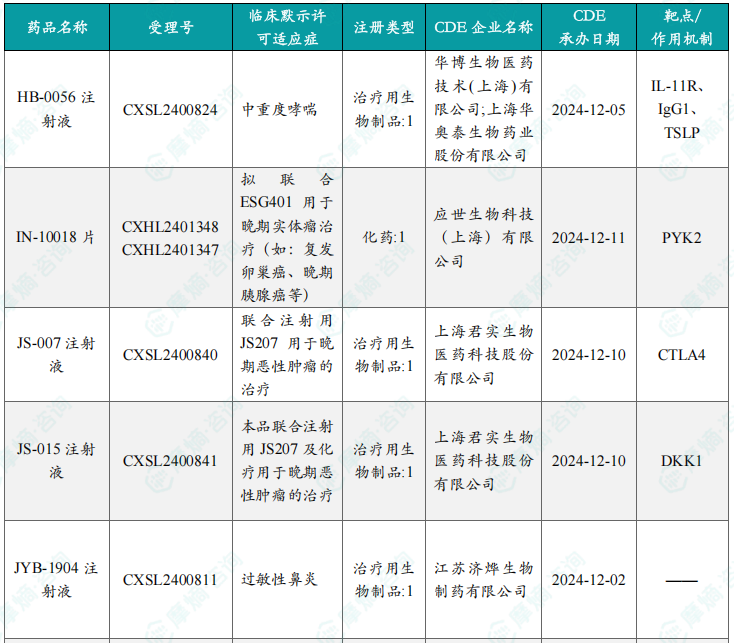
国内获批临床创新药/改良型新药信息速览
报告详细列出了本周获批临床的创新药/改良型新药信息,包括药品名称、受理号、注册类型、CDE企业名称、可适应症、承办日期、靶点和作用机制等。数据显示,获批临床的药品涵盖多个治疗领域,靶点也较为多样化,体现了国内创新药研发的多元化发展趋势。
国内获批上市创新药信息速览
本周无新药获批上市。
国内仿制药/生物类似物申报/审批情况分析
国内仿制药申报审批概况
本周CDE共承办96项仿制药申报上市/申报临床,其中新注册分类上市申请受理号78项,新注册分类临床申请受理号9项,一致性评价申请9项。本周1个品种通过一致性评价,无视同通过一致性评价品种。杭州中美华东制药有限公司的德谷胰岛素注射液有注册申报动态。
国内一致性评价分析
本周过评/视同过评品种主要为血液和造血系统药物,剂型主要为注射剂。甘露醇注射液过评/视同过评受理号数量最多,山东齐都药业有限公司过评/视同过评品种数最多。本周无首次过评/视同过评品种和过评/视同过评达7家企业品种。
国内医药大健康行业政策法规汇总
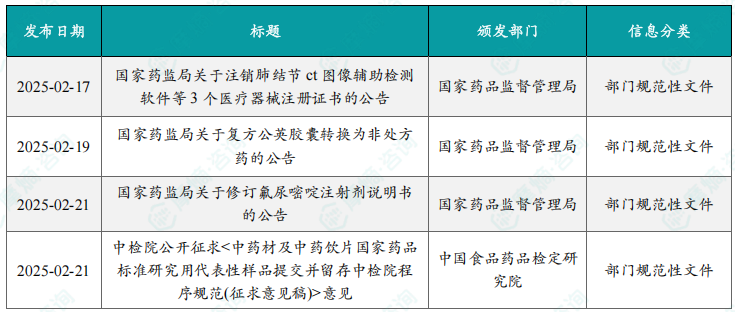
本周国内医药大健康行业政策法规速览
报告列出了本周发布的四个重要政策文件,包括注销部分医疗器械注册证书的公告、复方公英胶囊转换为非处方药的公告、氟尿嘧啶注射剂说明书修订公告以及中检院公开征求中药材及中药饮片国家药品标准研究用代表性样品提交并留存中检院程序规范意见稿。
本周重点行业政策详细说明
报告对上述四个政策文件进行了详细解读,分析了其对医药大健康行业的影响,并指出这些政策的发布有利于规范市场秩序,保障药品安全有效,推动行业健康发展。
全球创新药研发概览
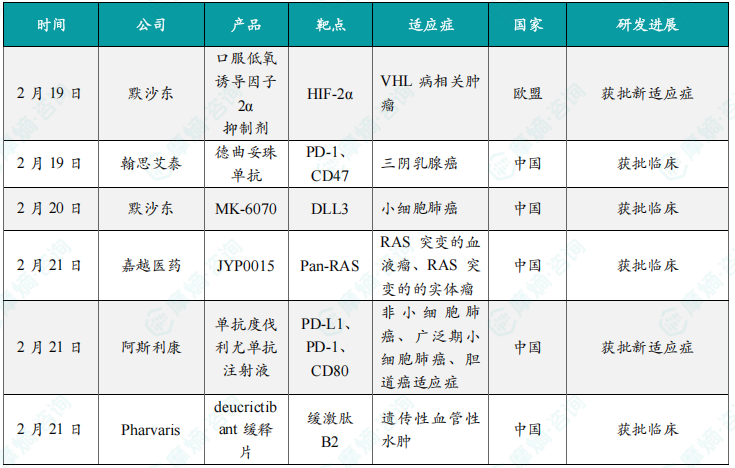
本周全球TOP10创新药研发进展
报告总结了本周全球TOP10创新药研发进展,包括研发企业、产品名称、靶点、适应症、国家和研发进展等信息。这些进展涵盖了多个治疗领域,例如肿瘤、感染性疾病和罕见病等,体现了全球创新药研发的蓬勃发展态势。
本周全球TOP10积极/失败临床结果
报告总结了本周全球TOP10创新药临床试验结果,包括研发企业、产品名称、靶点、适应症和临床数据(有效性)等信息。部分临床试验结果积极,显示出良好的疗效和安全性;部分临床试验结果未达到预期,反映出研发过程中的风险与挑战。
总结
本报告基于摩熵咨询医药行业观察周报数据,对2025年2月17日至2月23日期间国内外医药行业动态进行了全面分析。报告显示,国内创新药研发审批加速,但新药上市仍面临挑战;国内仿制药一致性评价稳步推进;医药大健康行业政策法规持续完善,旨在规范市场秩序,保障药品安全有效;全球创新药研发竞争激烈,多家药企在研产品取得积极进展,但临床试验结果也反映出研发过程中的风险与机遇并存。 这些信息为医药行业从业者提供了重要的市场参考和决策依据。 未来,持续关注创新药研发进展、政策法规变化以及市场竞争态势,将对医药行业发展具有重要意义。
-

摩熵咨询医药行业观察周报(2026.04.27-2026.05.03)
-

2026年4月仿制药月报
-

2026年4月全球在研新药月报
-

2026年4月摩熵医药健康投融资&交易月报
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送