-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

摩熵咨询医药行业观察周报(2025.07.07-2025.07.13)
摩熵咨询医药行业观察周报(2025.07.07-2025.07.13)
-
下载次数:
809 次
-
发布机构:
摩熵咨询了解机构实力
-
发布日期:
2025-07-13
-
页数:
25页
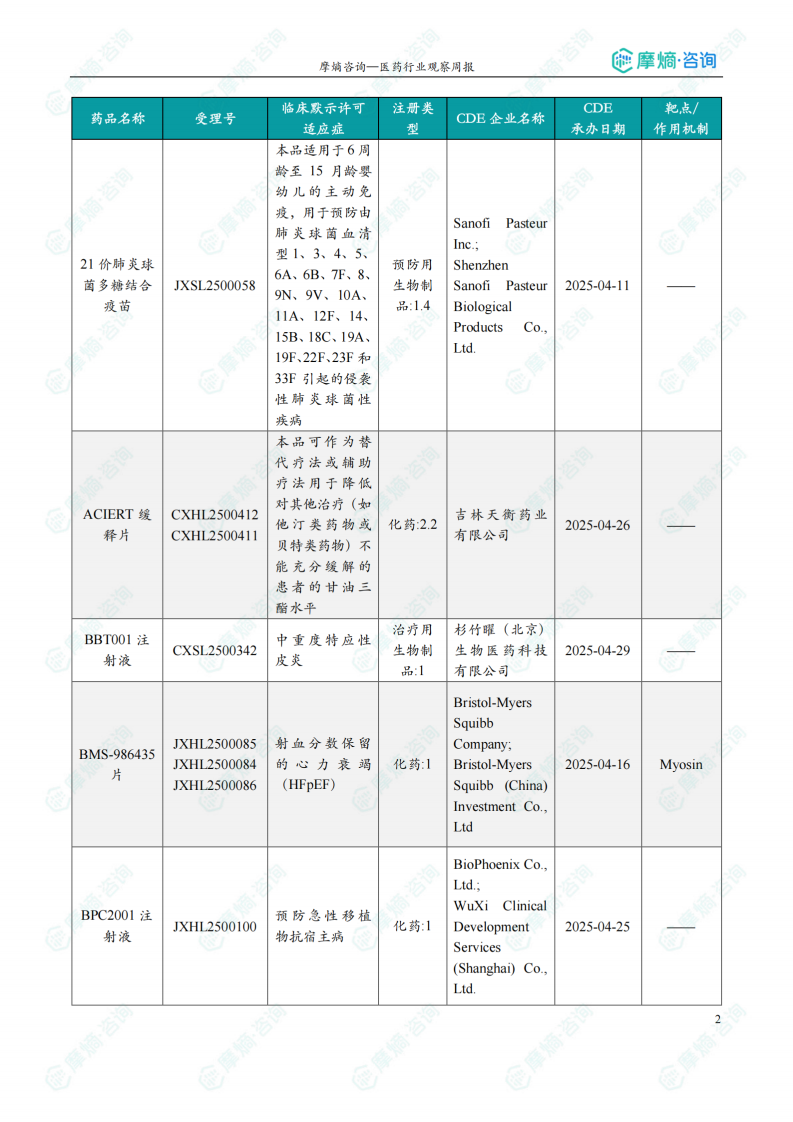
根据摩熵医药数据库统计,2025.07.07-2025.07.13期间共有122个创新药/改良型新药临床申请/上市申请获国家药品监督管理局药品审评中心(CDE)承办(按受理号统计,不含补充申请)。其中国产药品受理号95个,进口药品受理号27个。
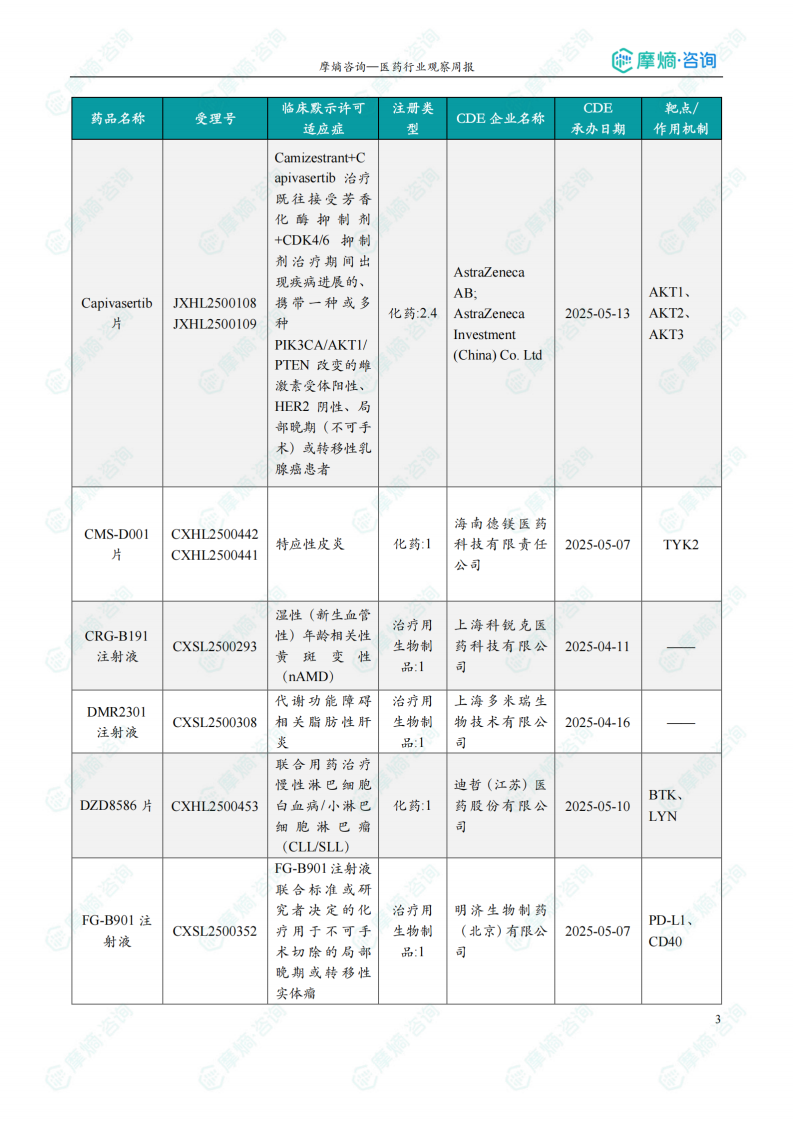
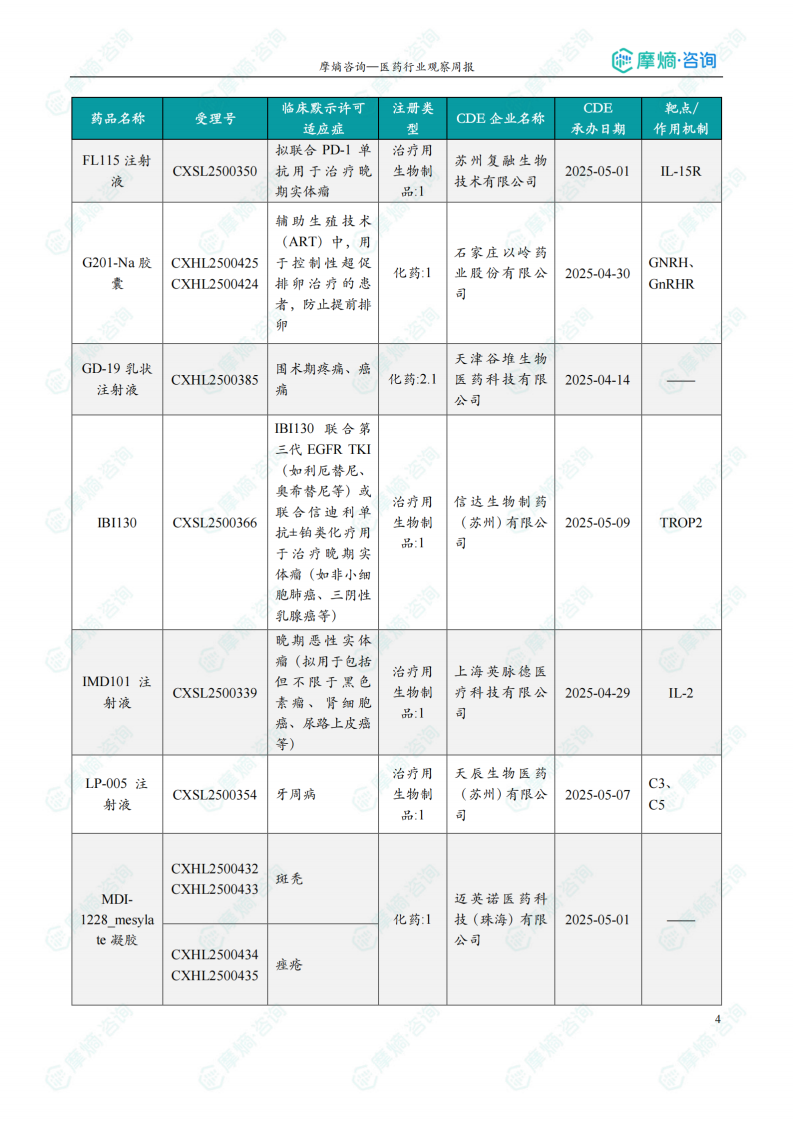
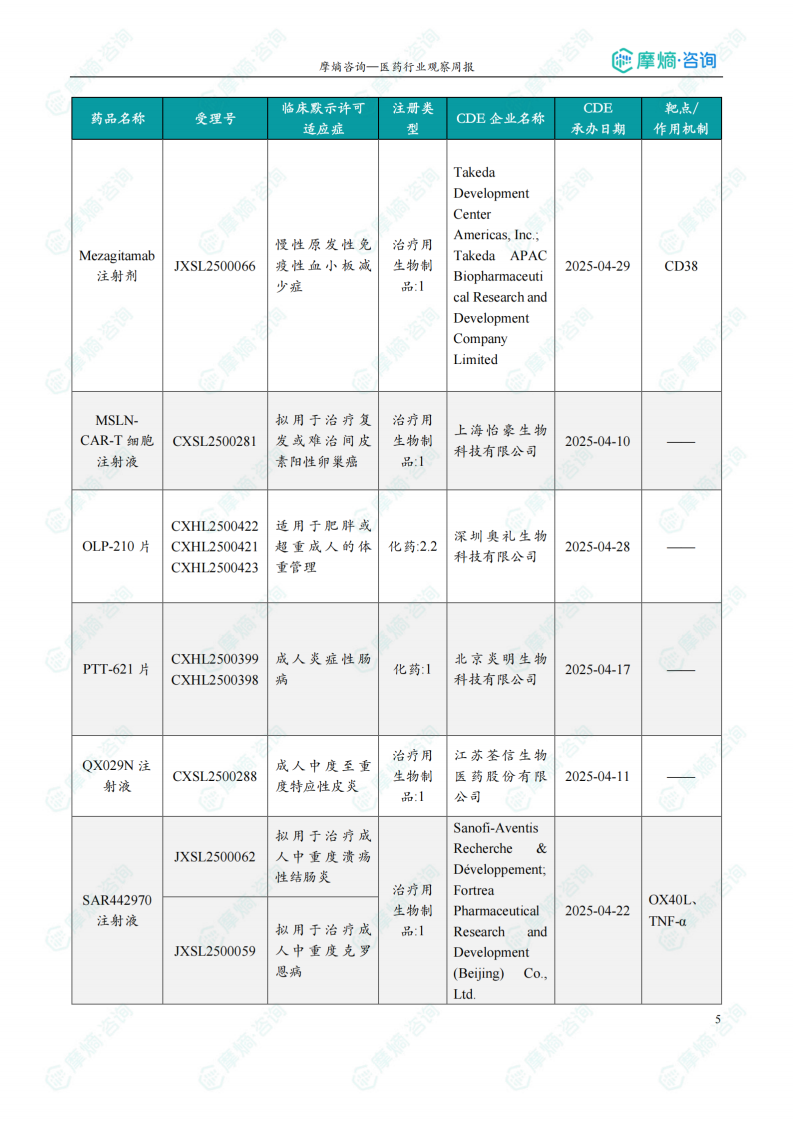
本周共计51款创新药/改良型新药临床试验申请获得“默示许可”,包括化学药20款,生物药29款,中药2款。其中值得注意的有:
(1)BBT001注射液
7月11日,CDE官网公示:杉竹曜生物的BBT001注射液获得临床试验默示许可,用于治疗中重度特应性皮炎。公开资料显示,BBT001注射液是一款靶向IL4Ra和IL31的四价双特异性抗体。
(2)CRG-B191注射液
7月7日,CDE官网公示:科锐克医药的CRG-B191注射液获得临床试验默示许可,用于治疗湿性(新生血管性)年龄相关性黄斑变性(nAMD)。公开资料显示,CRG-B191注射液是采用“新一代共价封闭端DNA基因组构型”的AAV(cceAAV)基因治疗药物,经视网膜下注射后,可在视网膜细胞中稳定、持续、高效表达经氨基酸序列优化的抗VEGF蛋白,有望实现一次注射长期有效,解决传统治疗中反复眼内注射带来的风险及患者依从性差等问题。
(3)注射用YL242
7月8日,CDE官网公示:宜联生物的注射用YL242获得临床试验默示许可,用于治疗晚期实体瘤,包括但不限于结肠直肠癌、胃腺癌或胃食管结合部腺癌、非小细胞肺癌、肝细胞癌等。公开资料显示,注射用YL242是一款靶向可溶性VEGF的非内化型ADC,旨在结合靶向VEGF的抗血管生成作用和肿瘤微环境释放的细胞毒载荷来发挥抗肿瘤活性。
本报告涉及: 相关药物:利沙托克拉片, 相关靶点:BCL2, 相关适应症:慢性淋巴细胞白血病、小淋巴细胞淋巴瘤 。
中心思想
本报告基于摩熵咨询医药行业观察周报(2025.07.07-2025.07.13)的数据,对国内外医药市场创新药、仿制药及相关政策法规进行了统计分析。核心观点如下:
- 创新药研发活跃: 国内外创新药研发持续推进,多个创新药获批临床或上市,涵盖多个治疗领域,展现出强大的研发实力。值得关注的是靶向IL4Ra和IL31的双特异性抗体BBT001注射液、靶向可溶性VEGF的ADC药物注射用YL242以及新型口服药物Ekterly等。
- 仿制药市场竞争激烈: 国内仿制药市场竞争激烈,多个品种通过或视同通过一致性评价,其中心血管系统药物占比最高。
- 政策法规持续完善: 国内医药大健康行业政策法规持续完善,发布多项政策文件,规范行业发展,例如关于《职业病分类和目录》实施的通知。
主要内容
国内创新药/改良型新药研发进展分析
本周共有122个创新药/改良型新药临床申请/上市申请获CDE承办,其中国产药品95个,进口药品27个。51款创新药/改良型新药临床试验申请获得“默示许可”,包括化学药20款,生物药29款,中药2款。3款新药获批上市,分别是力胜克拉片(治疗CLL/SLL)、斯美瑞非片(治疗勃起功能障碍)和褪黑素颗粒(改善儿童入睡困难)。
值得关注的获批临床创新药包括:
- BBT001注射液: 靶向IL4Ra和IL31的四价双特异性抗体,用于治疗中重度特应性皮炎。
- CRG-B191注射液: 采用“新一代共价封闭端DNA基因组构型”的AAV基因治疗药物,用于治疗湿性年龄相关性黄斑变性(nAMD)。
- 注射用YL242: 靶向可溶性VEGF的非内化型ADC,用于治疗晚期实体瘤。
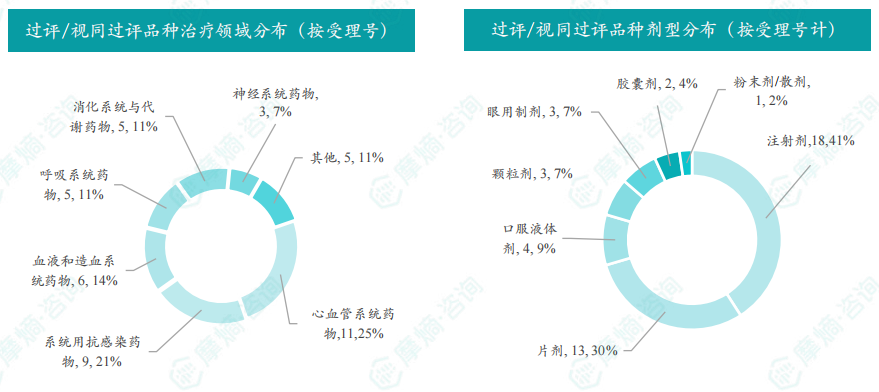
国内仿制药/生物类似物审批情况分析
本周共有138项仿制药申报上市/申报临床获CDE承办,其中包括125项上市申请和4项临床申请,以及9项一致性评价申请。4个品种通过一致性评价,35个品种视同通过一致性评价。本周心血管系统药物过评/视同过评数量最多,注射剂剂型占比最高。盐酸尼卡地平注射液过评/视同过评受理号数量最多,共有9家企业参与。浙江易泽达医药科技有限公司、浙江华海药业股份有限公司和天津力生制药股份有限公司过评/视同过评品种数最多。
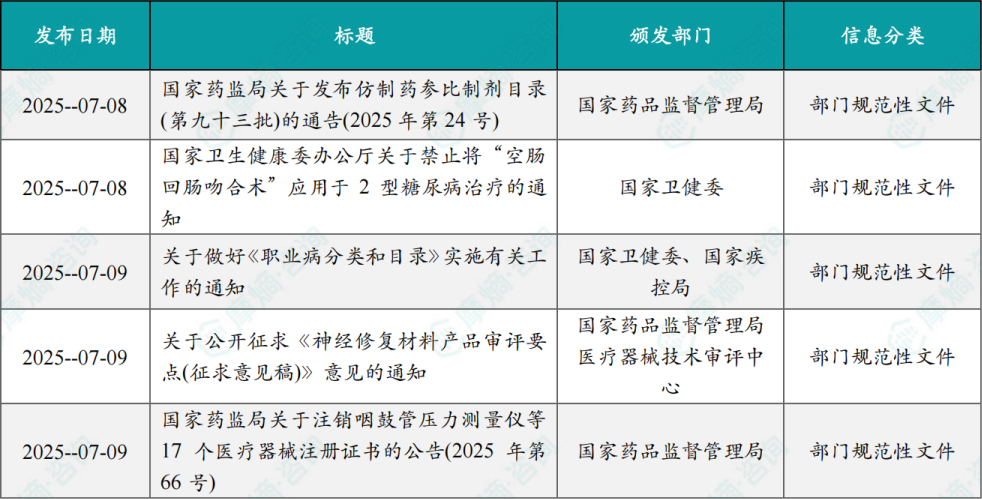
国内医药大健康行业政策法规解读
本周发布多项政策文件,涵盖仿制药参比制剂目录、禁止“空肠回肠吻合术”用于2型糖尿病治疗、做好《职业病分类和目录》实施工作等方面,体现了国家对医药行业监管的力度不断加强。其中,《职业病分类和目录》实施有关工作的通知,要求各地加强职业卫生监管人员培训,完善职业病诊断与鉴定专家库,确保职业病诊断、鉴定结论的公正、科学、准确。
全球创新药研发动态
本周全球TOP10创新药研发进展涵盖获批临床、获批上市、申报上市及纳入优先审评等多个阶段,涉及慢性乙肝、滤泡性淋巴瘤、遗传性血管性水肿、细菌性肺炎、小细胞肺癌、乳腺癌等多个治疗领域。其中,星汉德生物的SCG101V、徐诺药业的艾贝司他、KalVista Pharmaceuticals的Ekterly等药物进展值得关注。此外,本周还公布了多个创新药的积极临床试验结果,例如天境生物的givastomig、Celcuity的gedatolisib、Aurinia Pharmaceuticals的aritinercept等,也有一些药物的临床试验未能达到预期目标,例如大鹏药品的TAS-205。
总结
本周医药行业观察周报显示,国内外创新药研发持续活跃,多个创新药取得重要进展;国内仿制药市场竞争激烈,一致性评价工作稳步推进;国家持续完善医药大健康行业政策法规,规范行业发展。 未来,创新药研发仍将是行业发展的重要驱动力,而仿制药市场将面临更激烈的竞争。 持续关注政策法规变化,将有助于企业更好地把握市场机遇,促进医药行业健康发展。 本报告仅基于周报数据进行分析,更详细的数据和分析可通过摩熵医药数据库获取。

-

摩熵咨询医药行业观察周报(2026.04.27-2026.05.03)
-

2026年4月仿制药月报
-

2026年4月全球在研新药月报
-

2026年4月摩熵医药健康投融资&交易月报
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送