-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

摩熵咨询医药行业观察周报(2025.04.07-2025.04.13)
1.总体概况
根据摩熵医药数据库统计,2025.04.07-2025.04.13期间共有83个创新药/改良型新药临床申请/上市申请获国家药品监督管理局药品审评中心(CDE)承办(按受理号统计,不含补充申请)。其中国产药品受理号62个,进口药品受理号21个。
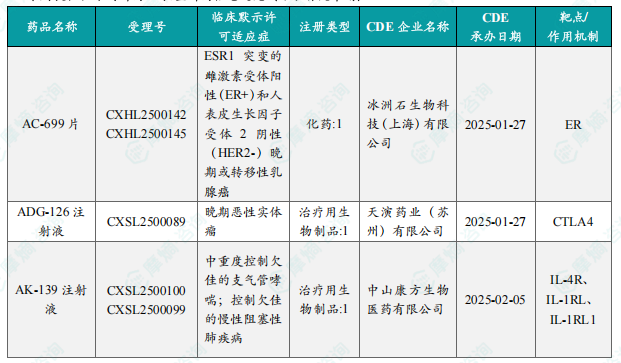
本周共计43款创新药/改良型新药临床试验申请获得“默示许可”,包括化学药19款,生物药24款,无中药。其中值得注意的有:
(1)AK-139注射液
4月10日,CDE官网公示:康方生物的AK-139注射液获得临床试验默示许可,用于治疗中重度控制欠佳的支气管哮喘和控制欠佳的慢性阻塞性肺疾病。公开资料显示,AK-139注射液是自主研发的全球首个靶向IL-4Rα/ST2双特异性抗体,可同时阻断IL-4、IL13(通过结合IL-4和IL-13受体复合物共享的IL-4Rα亚单位)和IL-33/ST2介导的炎症通路。
(2)DNV-001注射液
4月10日,CDE官网公示:鼎乐新为的DNV-001注射液获得临床试验默示许可,用于血脂异常的治疗,包括以低密度脂蛋白胆固醇(LDL-C)升高为特征的成人原发性高胆固醇血症(杂合子型家族性和非家族性)或混合型血脂异常患者的治疗。公开资料显示,DNV-001注射液是一种GalNAc-siRNA,通过敲降肝脏细胞中PCSK9 mRNA,从源头上阻断PCSK9的表达。
本周共1款新药获批上市,即枸橼酸艾瑞芬净片。
本报告涉及: 相关药物:AC-699片, 相关靶点:ER, 相关适应症:乳腺癌 。
中心思想
本报告基于摩熵咨询医药数据库,对2025年4月7日至13日期间中国及全球医药行业创新药、仿制药及相关政策法规进行了数据分析,总结如下:
国内创新药研发进展迅速
国内创新药研发持续活跃,本周共有83个创新药/改良型新药临床申请/上市申请获受理,其中国产药品62个,进口药品21个。43款创新药/改良型新药临床试验申请获得“默示许可”,1款新药获批上市。值得关注的是康方生物的AK-139注射液(靶向IL-4Rα/ST2双特异性抗体)和鼎乐新为的DNV-001注射液(GalNAc-siRNA)。
全球创新药研发动态
全球创新药研发方面,多个重要进展值得关注,包括CERo公司、Radiance公司和Epicrispr公司在研创新疗法获批临床,诺华、礼来等公司产品在中国申报上市,以及多个药物的临床试验结果公布,涵盖肿瘤、心血管疾病、过敏性疾病、肥胖症等多个领域。
主要内容
国内创新药/改良型新药申请临床/获批临床/申请上市/获批上市数据分析
国内创新药研发总体概况
2025年4月7日至13日期间,共有83个创新药/改良型新药临床申请/上市申请获CDE承办(按受理号统计,不含补充申请),其中国产药品62个,进口药品21个。本周共计43款创新药/改良型新药临床试验申请获得“默示许可”,包括化学药19款,生物药24款。本周仅1款新药获批上市,即江苏豪森的枸橼酸艾瑞芬净片,用于治疗外阴阴道念珠菌病。
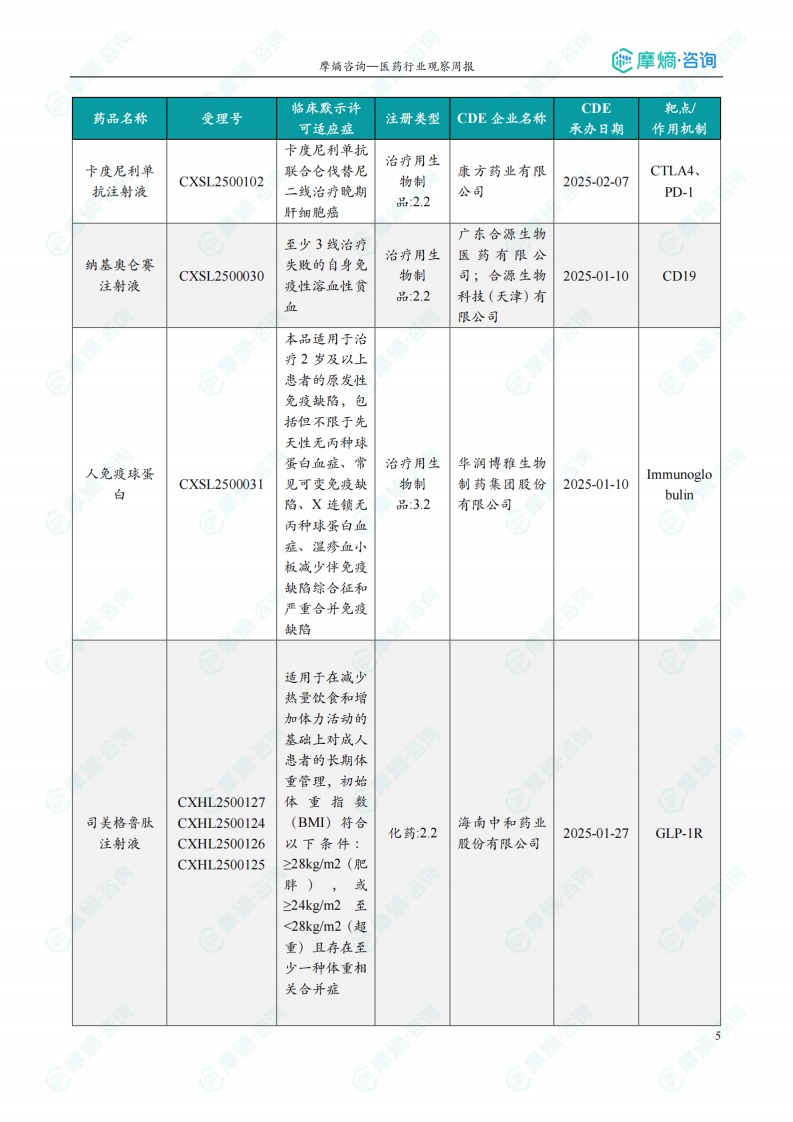
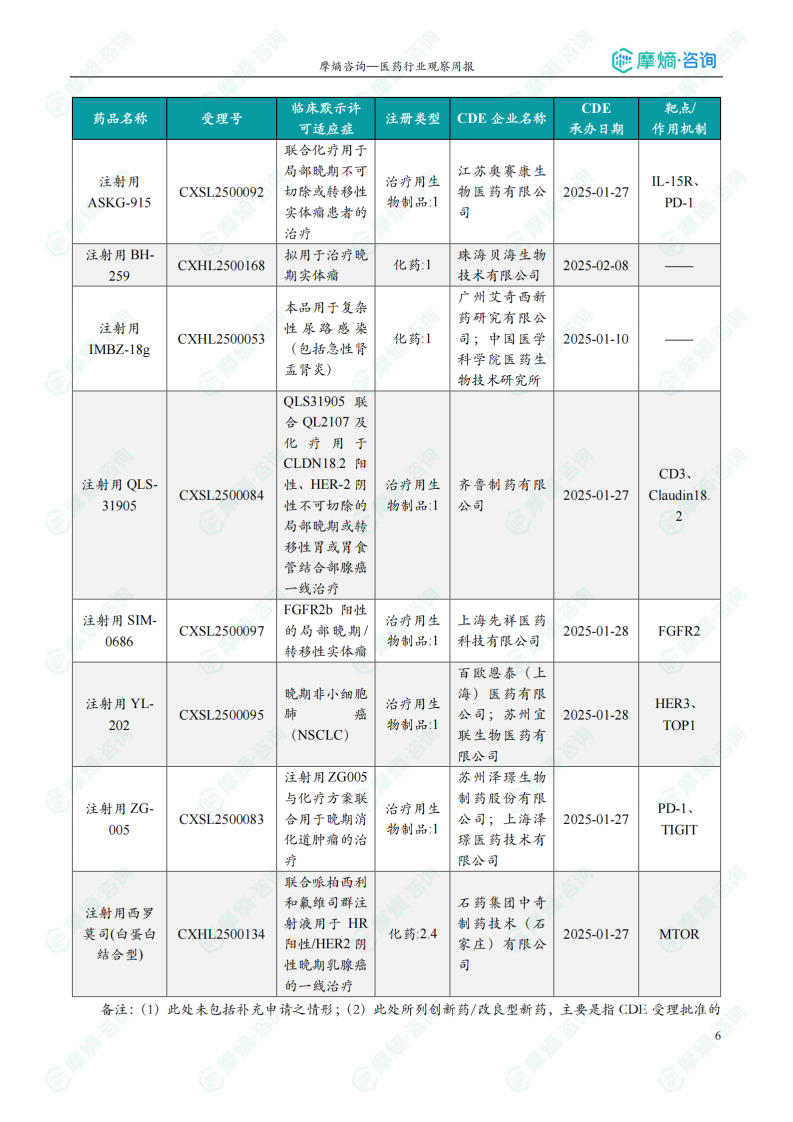
国内获批临床创新药信息速览
报告详细列出了本周获批临床的创新药/改良型新药信息,包括药品名称、受理号、注册类型、CDE企业名称、适应症、承办日期以及作用机制等关键信息。数据显示,获批临床的药物涵盖多个治疗领域,靶点多样化,体现了国内创新药研发的多元化趋势。
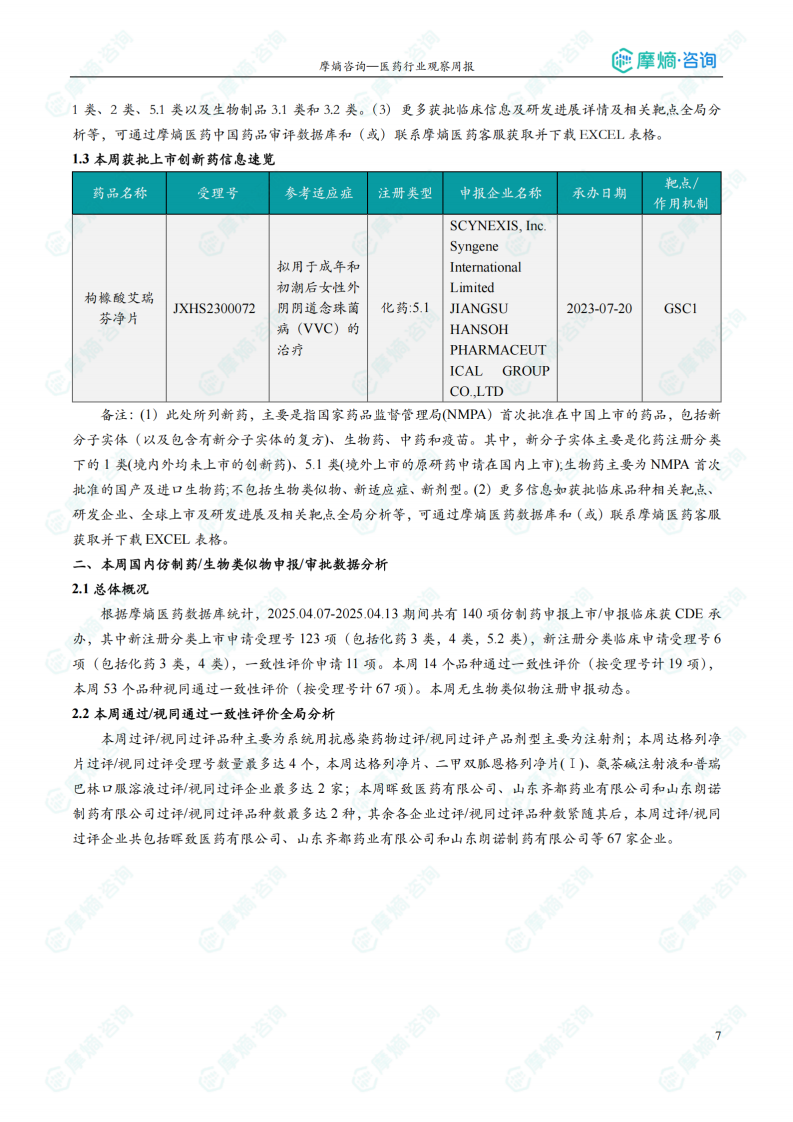
国内获批上市创新药信息速览
报告列出了本周获批上市的创新药信息,包括药品名称、受理号、适应症、注册类型、申报企业名称、承办日期以及作用机制等。本周仅枸橼酸艾瑞芬净片获批上市,该药是首个全新三萜类结构的糖原合成酶抑制剂。
国内仿制药/生物类似物申报/审批数据分析
国内仿制药申报总体概况
本周共有140项仿制药申报上市/申报临床获CDE承办,其中新注册分类上市申请受理号123项,新注册分类临床申请受理号6项,一致性评价申请11项。本周14个品种通过一致性评价(按受理号计19项),53个品种视同通过一致性评价(按受理号计67项)。
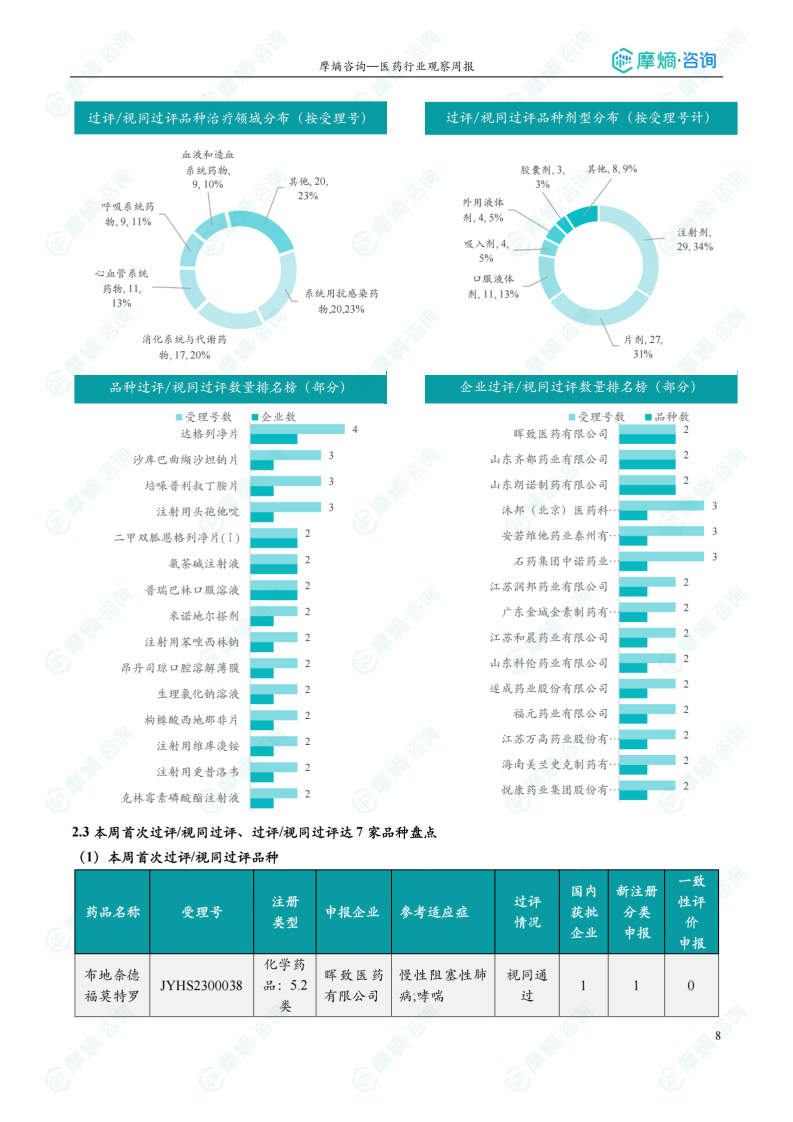
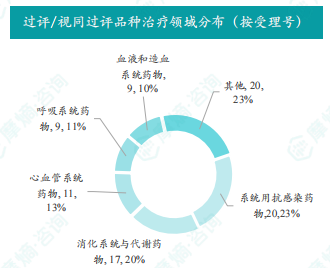
国内一致性评价全局分析
报告对本周通过/视同通过一致性评价的品种进行了全局分析,包括治疗领域分布、剂型分布以及企业排名等。数据显示,系统用抗感染药物过评/视同过评产品剂型主要为注射剂,达格列净片过评/视同过评受理号数量最多。
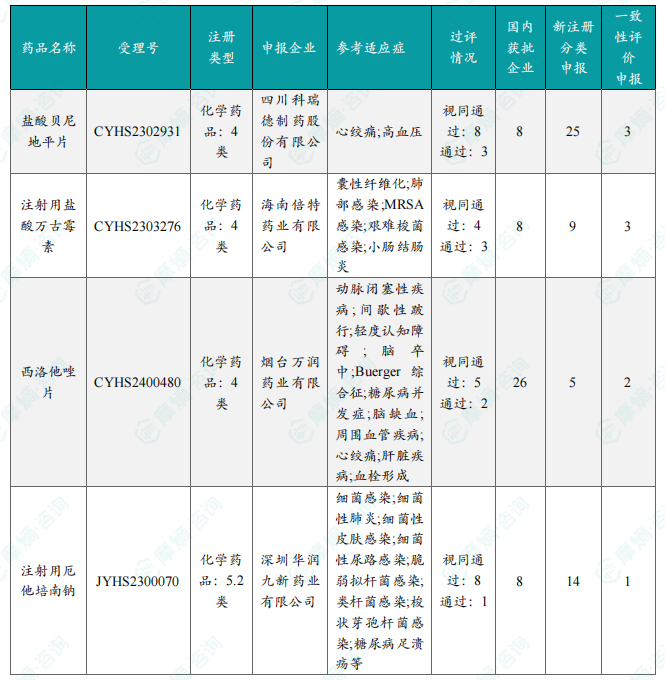
国内首次过评/视同过评品种及过评/视同过评达7家品种盘点
报告分别列出了本周首次过评/视同过评的品种以及过评/视同过评达7家企业的品种,并提供了详细的药品信息,包括药品名称、受理号、申报企业、适应症、注册分类、类型、一致性评价情况等。
国内医药大健康行业政策法规汇总
国内医药大健康行业政策法规速览
报告列出了本周发布的国内医药大健康行业政策法规,包括发布日期、标题、颁发部门以及信息分类等。
重点行业政策详细说明
报告对本周重点行业政策《医疗器械分类规则(修订草案征求意见稿)》进行了详细说明,阐述了修订草案的主要内容,包括医疗器械的风险程度判定、管理类别划分以及分类规则与分类目录的动态衔接机制等。
全球创新药研发概览
全球TOP10创新药研发进展
报告总结了本周全球TOP10创新药研发进展,包括时间、公司、产品、靶点、适应症、国家以及研发进展等信息。这些进展涵盖了多个治疗领域,例如肿瘤、心血管疾病、神经系统疾病等。
全球TOP10积极/失败临床结果
报告总结了本周全球TOP10积极/失败临床试验结果,包括时间、公司、产品、靶点、适应症以及临床数据等信息。这些结果为相关药物的研发提供了重要的参考依据。
总结
本报告基于摩熵咨询医药数据库,对2025年4月7日至13日期间中国及全球医药行业的创新药、仿制药及相关政策法规进行了数据分析。报告显示,国内创新药研发持续活跃,全球创新药研发也取得了显著进展,多个创新疗法获批临床或申报上市,多个临床试验结果公布,为相关疾病的治疗带来了新的希望。同时,国内医药监管政策也在不断完善,为医药行业健康发展提供了有力保障。 本报告的数据分析为医药行业从业者提供了重要的市场信息和参考依据。 需要注意的是,报告数据基于摩熵咨询数据库,数据完整性和准确性以数据库为准。 更多详细数据可通过摩熵医药数据库获取。
-

摩熵咨询医药行业观察周报(2026.04.27-2026.05.03)
-

2026年4月仿制药月报
-

2026年4月全球在研新药月报
-

2026年4月摩熵医药健康投融资&交易月报
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送