-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

2025年3月仿制药月报
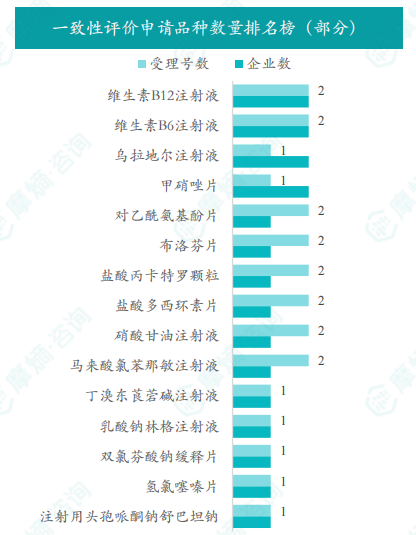
根据摩熵数据统计,2025年3月共有25个品种(按受理号计33项)一致性评价申请获CDE承办,申请品种主要为心血管系统药物,申请剂型主要为注射剂和片剂。维生素B12注射液、维生素B6注射液、乌拉地尔注射液和甲硝唑片为申请企业数最多的品种,均有2家;上海锦帝九州药业(安阳)有限公司是申请品种最多的企业,有2个品种。
本报告涉及: 相关药物:注射用头孢西丁钠, 相关适应症:感染 。
中心思想
本报告基于摩熵数据,对2025年3月中国仿制药市场进行了统计分析,核心观点如下:
一致性评价与新注册分类仿制药申请现状
3月份一致性评价和新注册分类仿制药申请数量均较大,体现了市场活跃度。申请品种主要集中在心血管系统和消化系统药物,剂型以注射剂和片剂为主。部分品种申请企业数量较多,竞争激烈。
市场获批上市及竞争格局分析
3月份共有大量仿制药获批上市,其中一致性评价过评和视同通过品种数量均显著。部分品种已有多家企业通过一致性评价,市场竞争日益加剧。首家过评和达七家过评品种的分析,揭示了市场竞争格局和潜在的市场机会。
主要内容
一、本月一致性评价/新注册分类仿制药申请信息
1.1 本月一致性评价仿制药申请信息
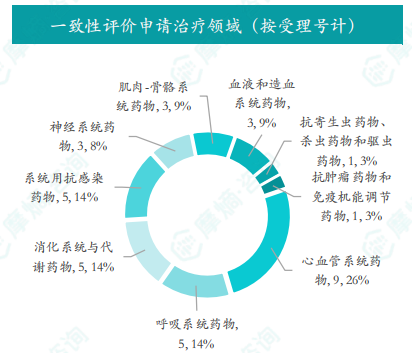
2025年3月,共有25个品种(按受理号计33项)一致性评价申请获CDE承办。申请品种主要集中于心血管系统药物,其次是消化系统和呼吸系统药物等。注射剂和片剂是主要的申请剂型。维生素B12注射液、维生素B6注射液、乌拉地尔注射液和甲硝唑片等品种的申请企业数量最多,均超过2家。上海锦帝九州药业(安阳)有限公司是申请品种最多的企业。 数据显示,心血管系统药物的一致性评价申请占比最高(26%),其次是消化系统与代谢药物(14%)。剂型方面,注射剂和片剂的占比均超过45%。
1.2 本月新注册分类仿制药申报临床/上市信息
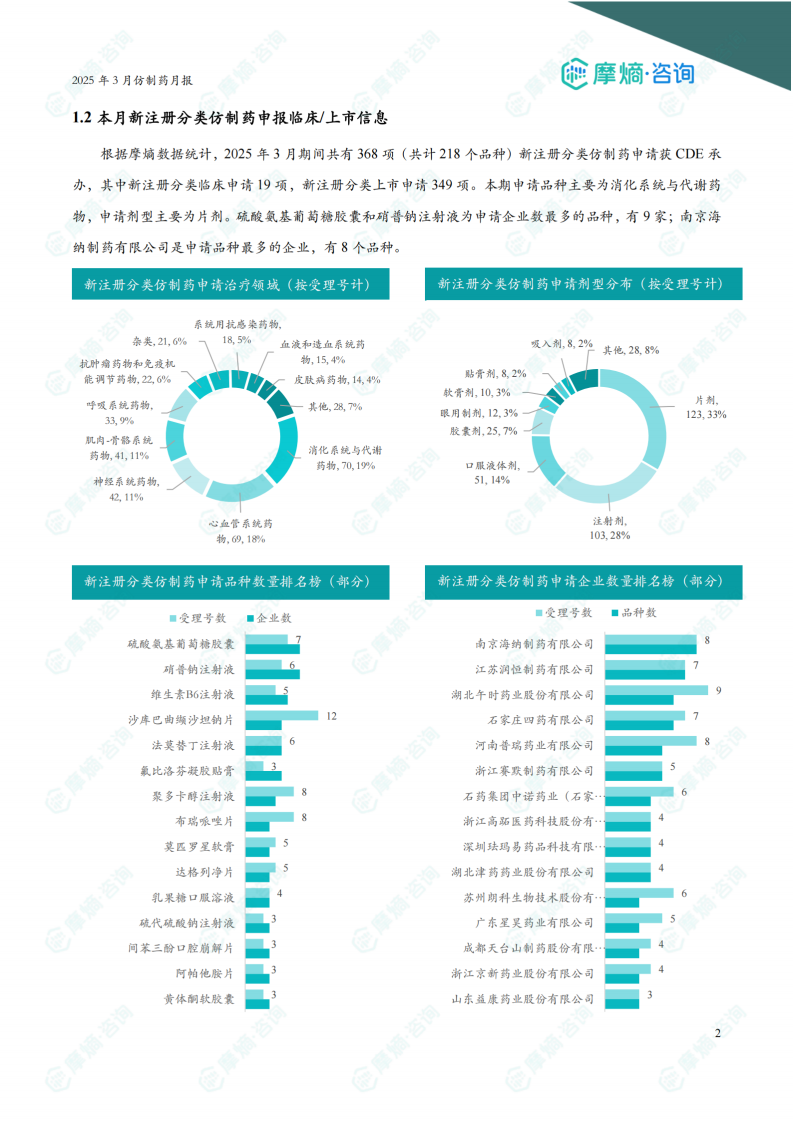
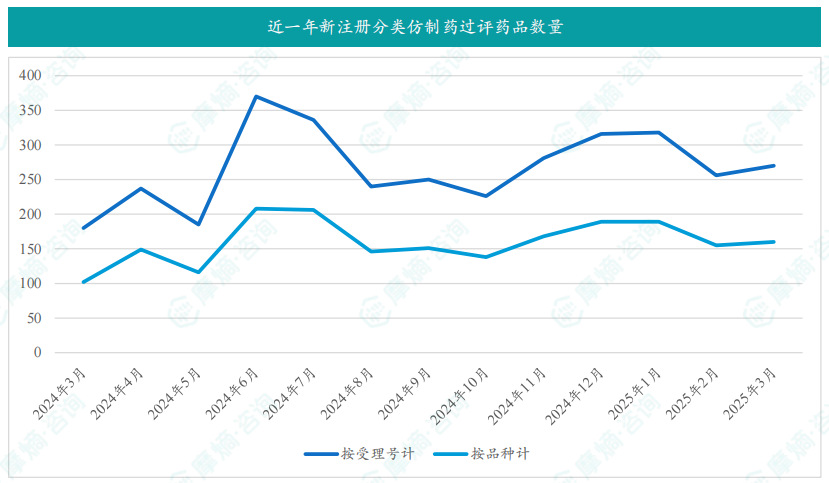
3月份共有368项(共计218个品种)新注册分类仿制药申请获CDE承办,其中临床申请19项,上市申请349项。申请品种主要为消化系统与代谢药物,片剂为主要剂型。硫酸氨基葡萄糖胶囊和硝普钠注射液申请企业数量最多,均达9家。南京海纳制药有限公司申请品种最多,达8个。数据显示,消化系统与代谢药物的新注册分类仿制药申请占比最高(19%),其次是心血管系统药物(18%)。片剂的占比超过33%,注射剂占比也接近30%。
二、本月过评/新注册分类仿制药获批上市信息
2.1 通过一致性评价信息
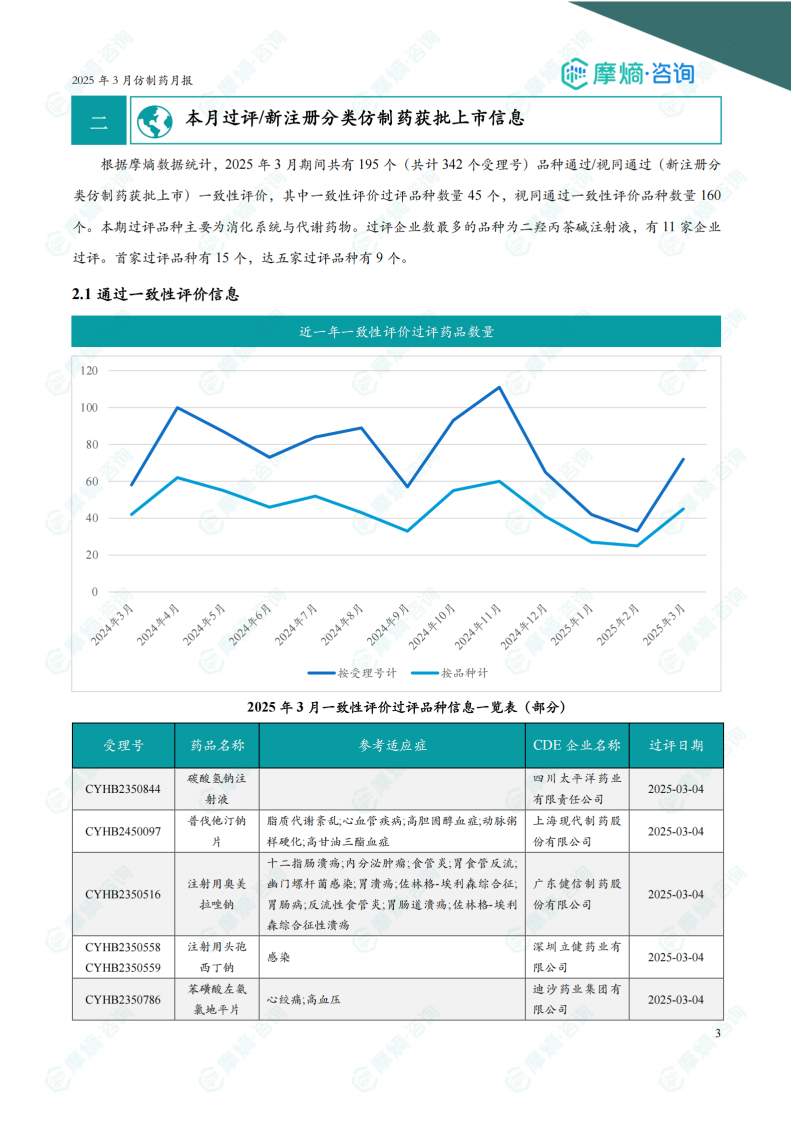
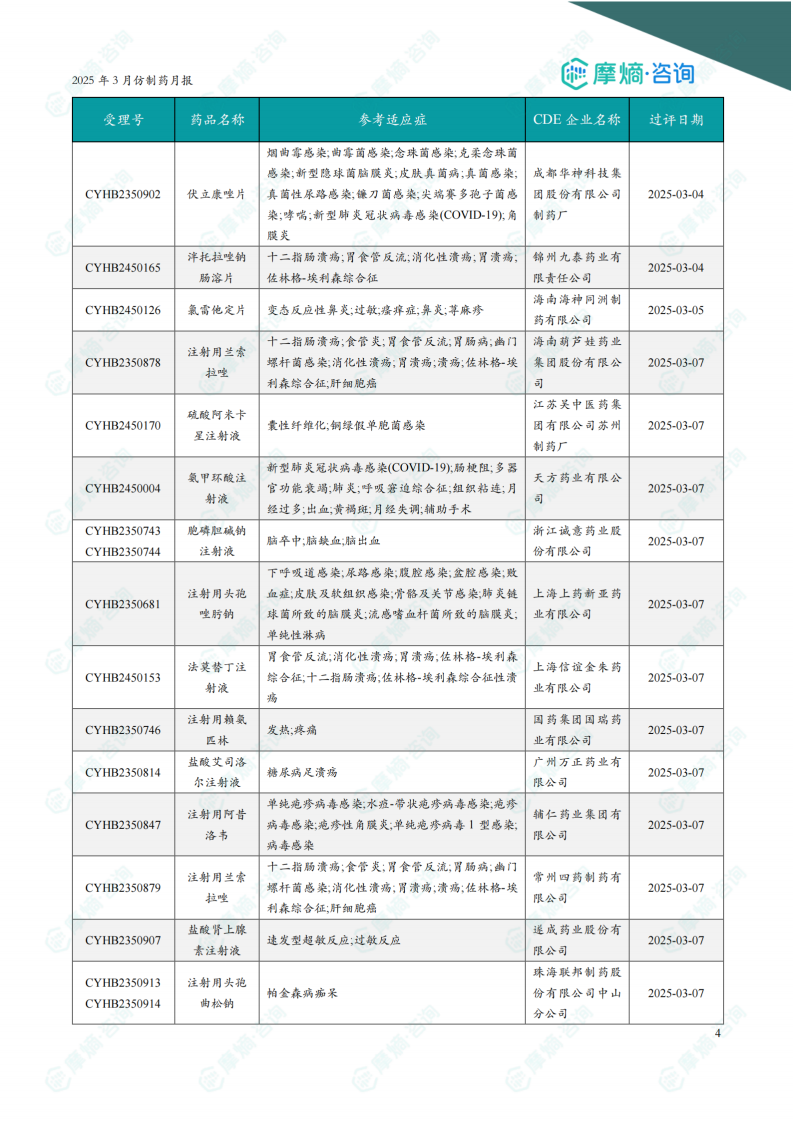
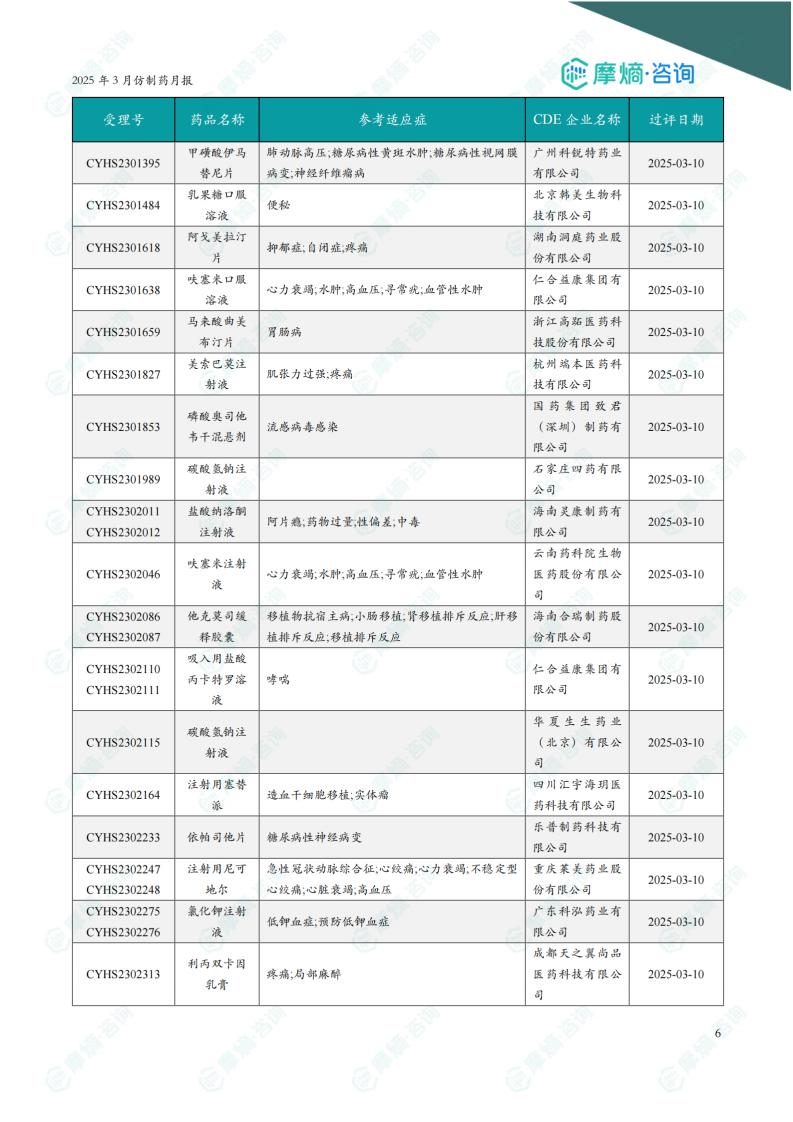
2025年3月,共有195个(共计342个受理号)品种通过/视同通过一致性评价,其中一致性评价过评品种45个,视同通过品种160个。过评品种主要为消化系统与代谢药物。二羟丙茶碱注射液过评企业数量最多,达11家。报告提供了部分过评品种的详细信息,包括受理号、药品名称、参考适应症、CDE企业名称和过评日期。图表显示,近一年一致性评价过评药品数量呈现增长趋势。
2.2 新注册分类仿制药获批上市信息
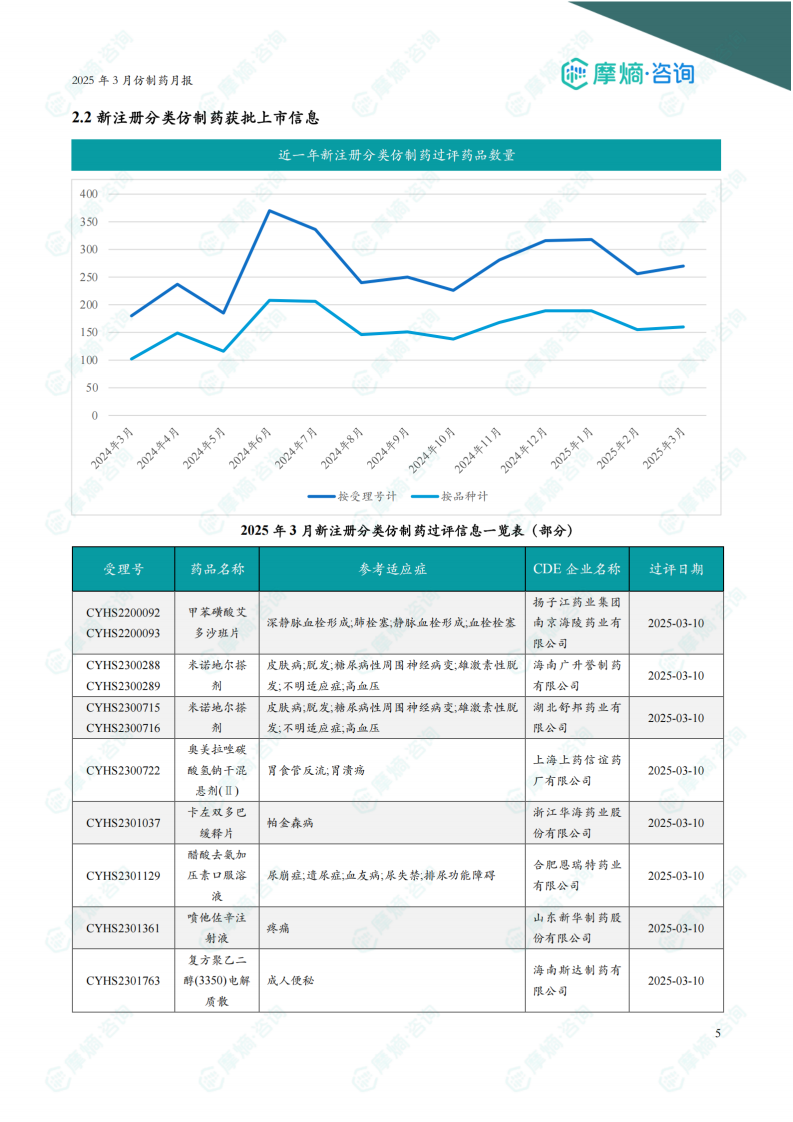
3月份共有大量新注册分类仿制药获批上市,图表显示近一年新注册分类仿制药过评数量也呈现增长趋势。报告提供了部分获批品种的详细信息,包括受理号、药品名称、参考适应症、CDE企业名称和过评日期。
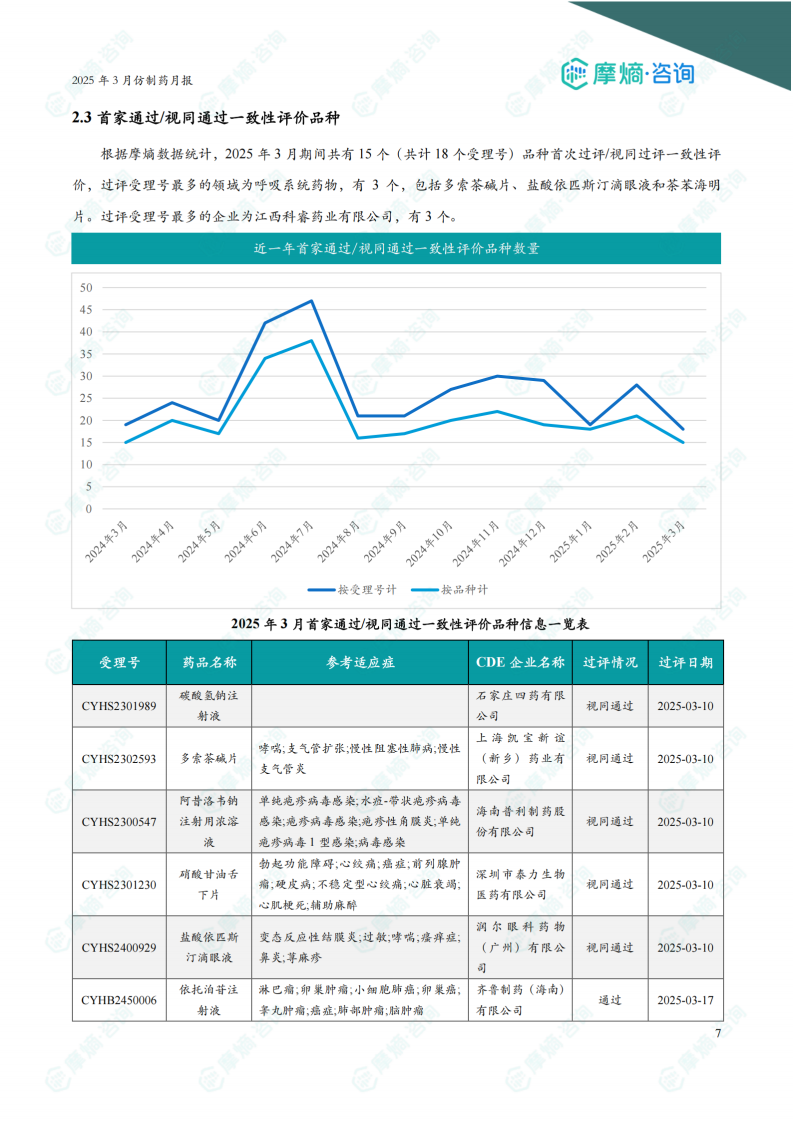
2.3 首家通过/视同通过一致性评价品种
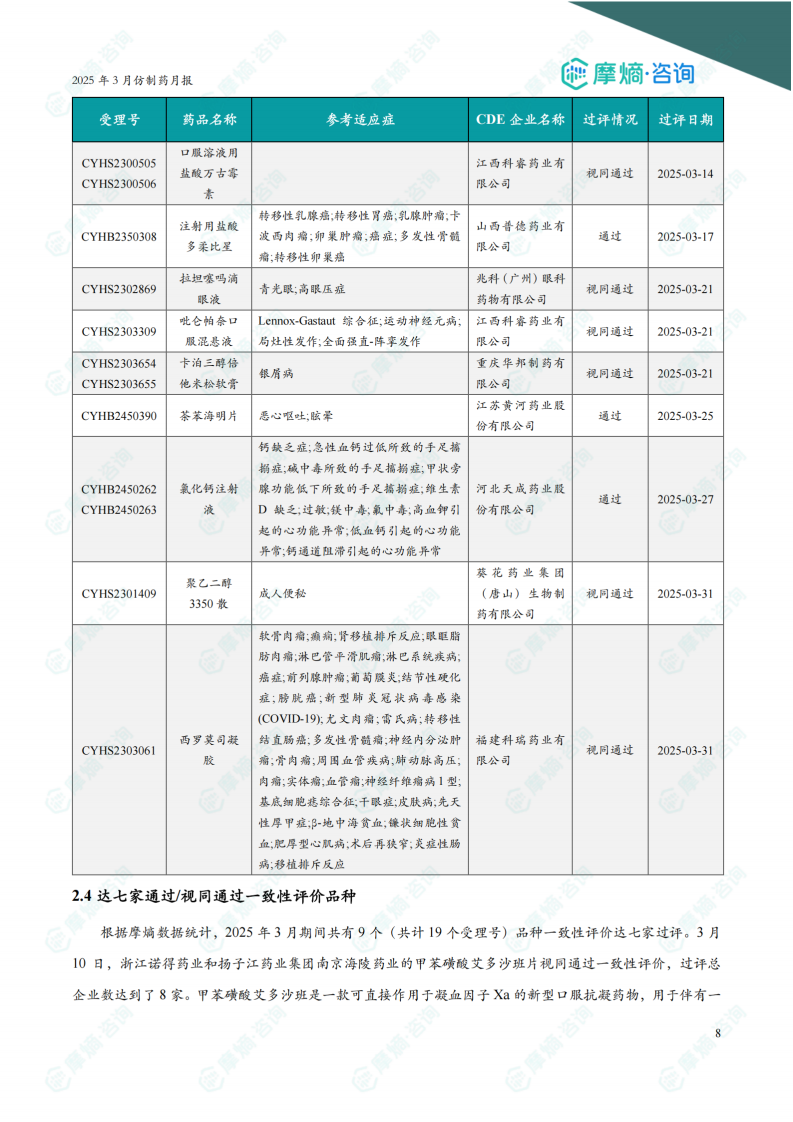
3月份共有15个(共计18个受理号)品种首次过评/视同过评一致性评价。呼吸系统药物过评受理号最多,达3个。江西科睿药业有限公司过评受理号最多,达3个。图表显示,近一年首家通过/视同通过一致性评价品种数量也呈现增长趋势。报告列出了这些品种的详细信息。
2.4 达七家通过/视同通过一致性评价品种
3月份共有9个(共计19个受理号)品种一致性评价达七家过评。报告详细分析了甲苯磺酸艾多沙班片、注射用阿糖胞苷和多巴丝肼片这三个达七家过评品种的市场竞争情况,包括其市场销售额和原研药企的市场份额。图表显示,近一年通过/视同通过达七家品种数量也呈现增长趋势。
三、仿制药最新政策速递
报告列出了3月份发布的与仿制药相关的政策文件,包括发布日期、标题、颁发部门和信息分类,涵盖了医保药品分类、基因测序试剂、药品生产质量管理规范、药品试验数据保护等多个方面。
总结
2025年3月中国仿制药市场呈现出持续活跃的态势,一致性评价和新注册分类仿制药的申请和获批数量均较大。市场竞争日益激烈,部分品种已有多家企业通过一致性评价,首家过评和达七家过评品种的分析进一步印证了这一趋势。 同时,一系列新的政策法规的出台,也对仿制药行业的发展方向和监管力度产生影响。 未来,仿制药企业需要加强研发创新,提升产品质量和竞争力,才能在激烈的市场竞争中获得可持续发展。 本报告的数据分析为企业决策提供了重要的参考依据。
-

摩熵咨询医药行业观察周报(2026.04.20-2026.04.26)
-

2025年中国临床试验数据洞察
-

摩熵咨询医药行业观察周报(2026.04.13-2026.04.19)
-

摩熵咨询医药行业观察周报(2026.04.06-2026.04.12)
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






相关专题报告
对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送