-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

摩熵咨询医药行业观察周报(2025.06.09-2025.06.15)
根据摩熵医药数据库统计,2025.06.09-2025.06.15期间共有110个创新药/改良型新药临床申请/上市申请获国家药品监督管理局药品审评中心(CDE)承办(按受理号统计,不含补充申请)。其中国产药品受理号67个,进口药品受理号43个。
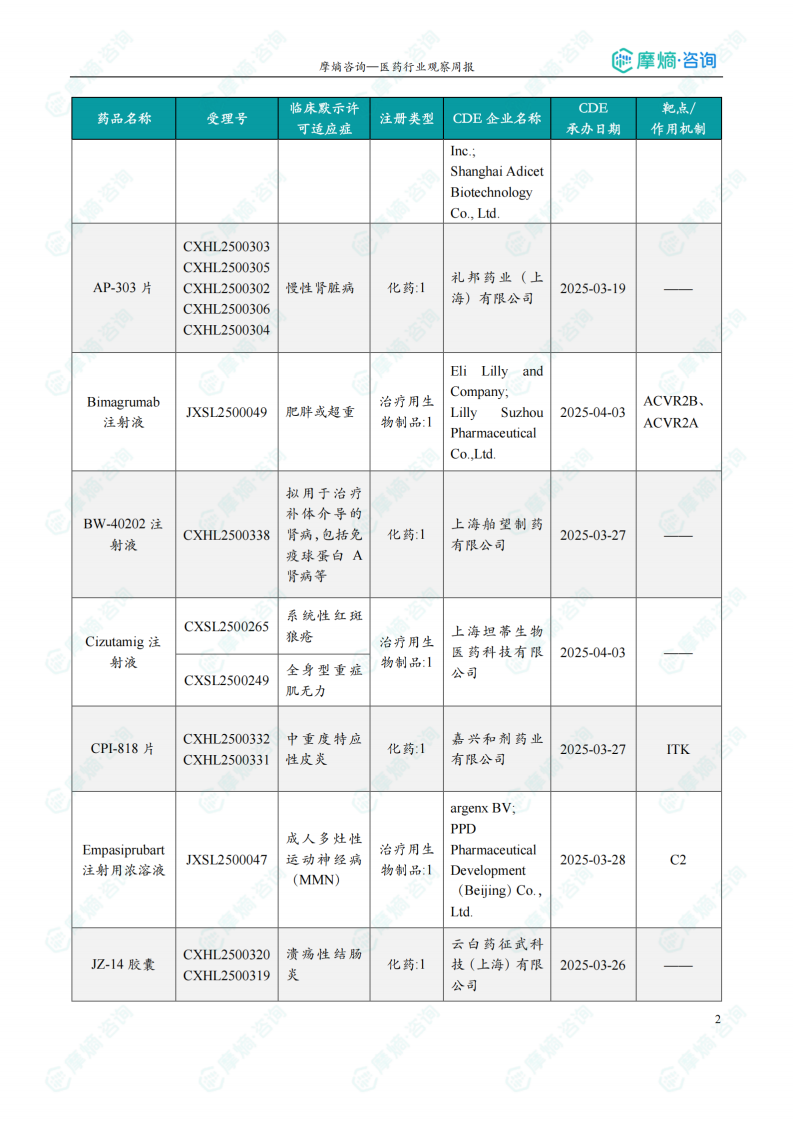
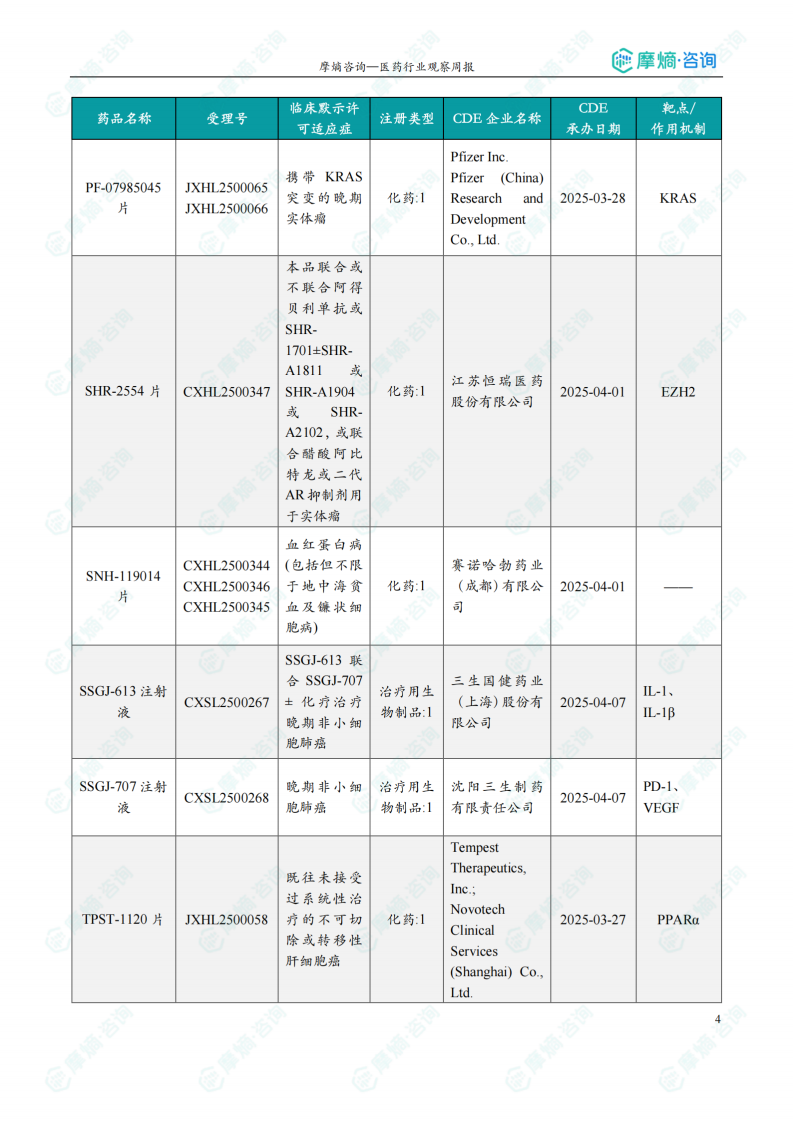
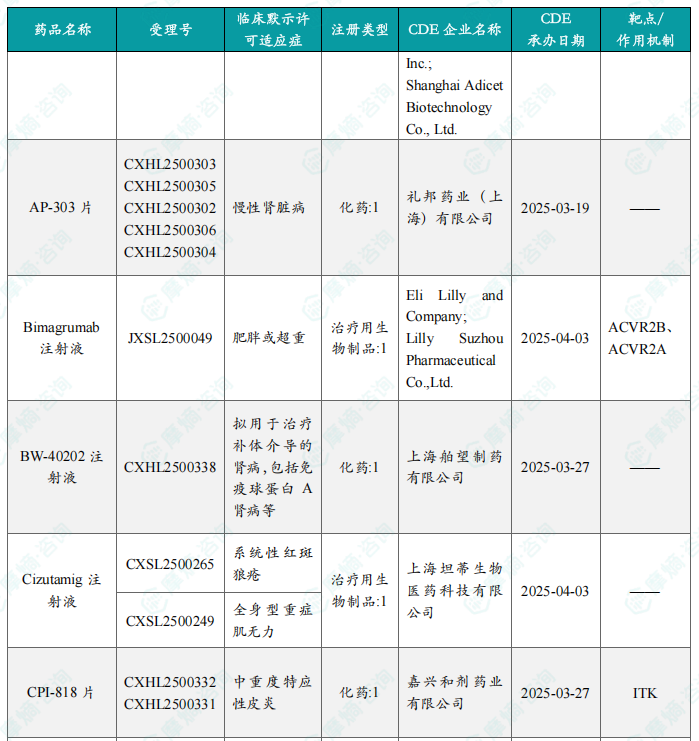
本周共计68款创新药/改良型新药临床试验申请获得“默示许可”,包括化学药34款,生物药31款,中药3款。其中值得注意的有:
(1)Empasiprubart注射用浓溶液
6月9日,CDE官网公示:argenx公司的Empasiprubart注射用浓溶液获得临床试验默示许可,用于治疗成人多灶性运动神经病(MMN)。公开资料显示,Empasiprubart注射用浓溶液是一款人源化“清除抗体”(sweeping antibodies),以pH-和Ca2+依赖的方式特异性结合C2。C2是补体级联中的一种蛋白质,empasiprubart旨在抑制C2和下游补体激活的功能,从而减少组织炎症和适应性免疫反应。
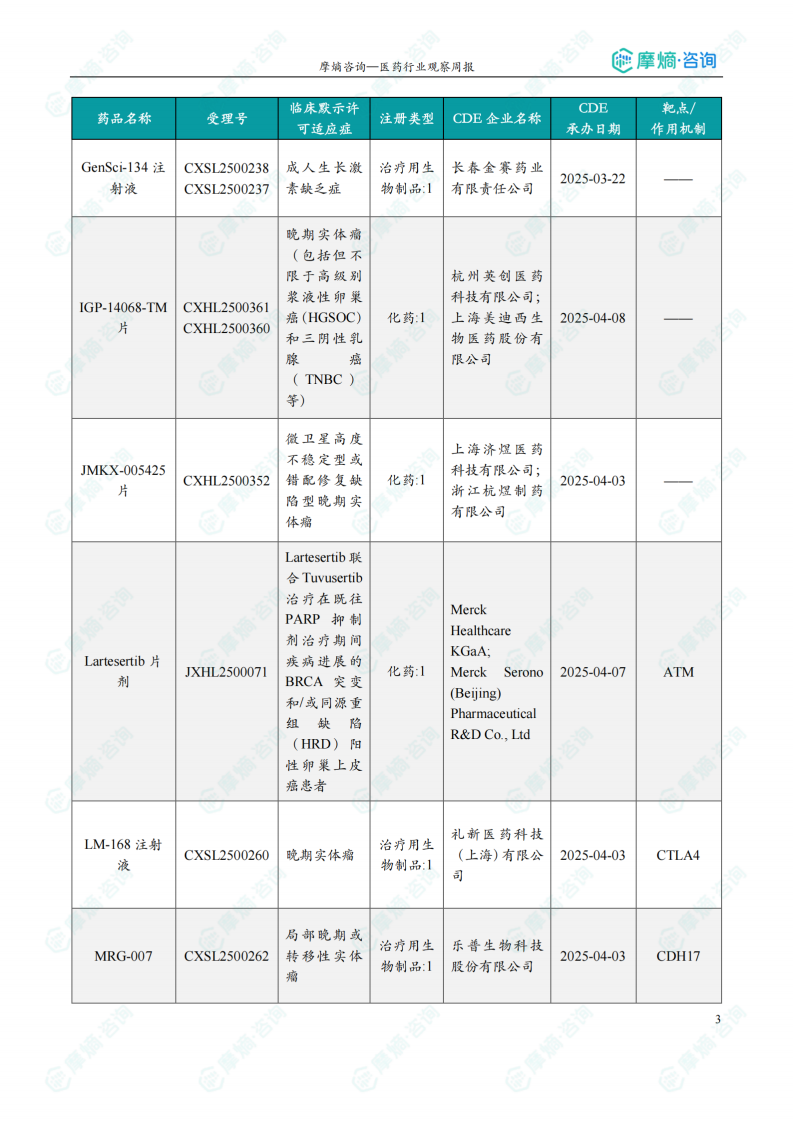
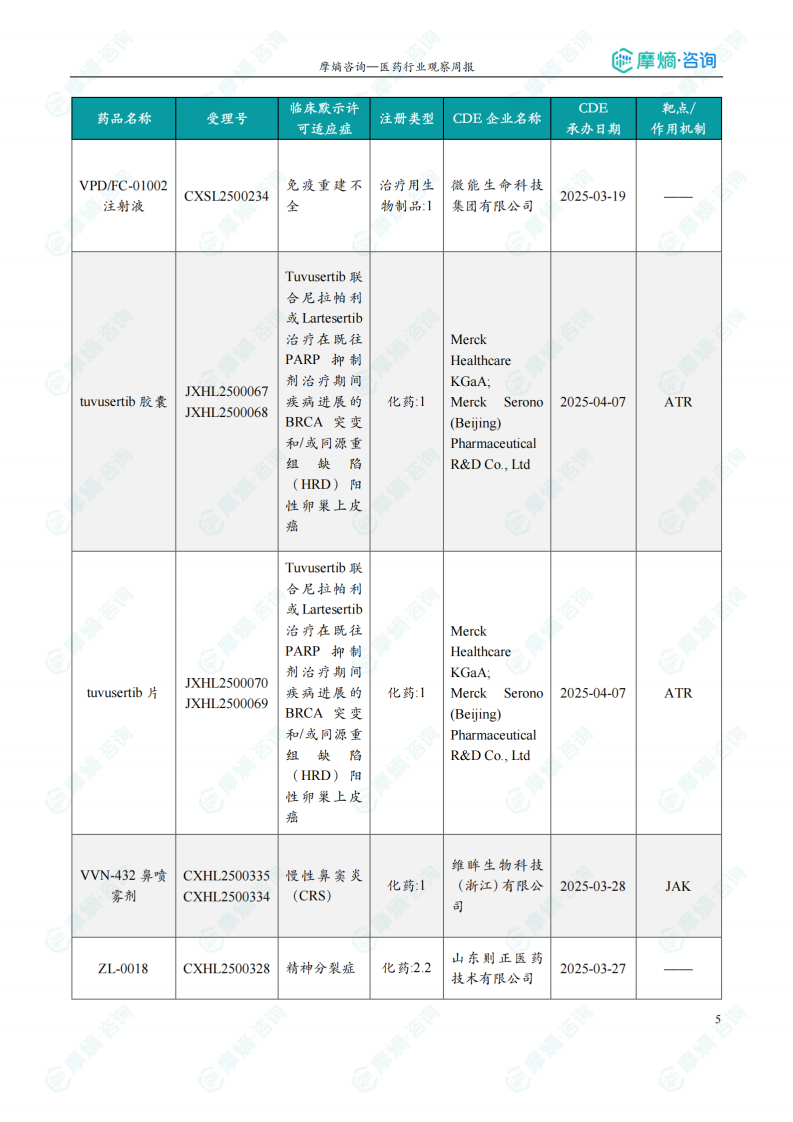
(2)Lartesertib片剂
6月13日,CDE官网公示:德国默克(Merck KGaA)的Lartesertib片剂获得临床试验默示许可,联合Tuvusertib治疗在既往PARP抑制剂治疗期间疾病进展的BRCA突变和/或同源重组缺陷(HRD)阳性卵巢上皮癌患者。公开资料显示,Lartesertib片剂是一款ATM抑制剂,研究显示,在ATM缺失的肿瘤细胞中,ATR抑制剂可以产生合成致死效应,在导致ATM缺失肿瘤细胞死亡的同时,并不影响正常细胞。
(3)LM-168注射液
6月12日,CDE官网公示:礼新医药的LM-168注射液获得临床试验默示许可,用于治疗晚期实体瘤。公开资料显示,LM-168注射液是一款抗CTLA-4抗体。该产品经过工程化改造,可在肿瘤微环境(TME)中高ATP/ADP/AMP(ANP)水平下选择性结合CTLA-4,而在健康组织中结合力较弱,从而降低“脱靶毒性”。
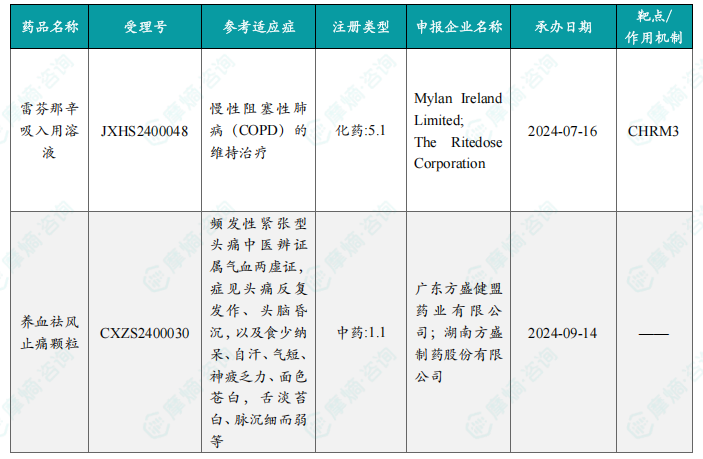
本周共2款新药获批上市,即养血祛风止痛颗粒和雷芬那辛吸入用溶液。
本报告涉及: 相关药物:雷芬那辛吸入溶液, 相关靶点:CHRM3, 相关适应症:慢性阻塞性肺病 。
中心思想
本报告基于摩熵咨询医药数据库,对2025年6月9日至15日期间中国及全球医药行业创新药、仿制药及政策法规动态进行了数据分析和解读。核心观点如下:
国内创新药研发进展迅速,但仿制药市场竞争激烈
国内创新药研发持续活跃,本周多个创新药获批临床或上市,涵盖多个治疗领域,体现了中国医药产业的创新能力。然而,仿制药市场竞争依然激烈,一致性评价成为关键竞争因素,部分品种过评/视同过评企业数量众多。
全球创新药研发取得积极进展,多个药物获批或进入后期临床阶段
全球范围内,多个创新药研发取得积极进展,部分药物获批上市,另一些药物则在临床试验中取得积极结果,展现了全球医药研发领域的蓬勃发展态势。
主要内容
国内医药市场数据分析
国内创新药/改良型新药研发概况
本周共有110个创新药/改良型新药临床申请/上市申请获CDE承办,其中国产药品67个,进口药品43个。68款创新药/改良型新药临床试验申请获得“默示许可”,包括化学药34款,生物药31款,中药3款。值得关注的是argenx公司的Empasiprubart注射用浓溶液、德国默克的Lartesertib片剂以及礼新医药的LM-168注射液等创新药物。本周共有2款新药获批上市,分别是养血祛风止痛颗粒和雷芬那辛吸入用溶液。
国内仿制药/生物类似物申报/审批数据分析
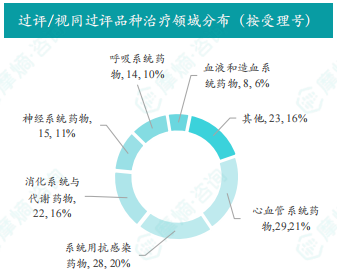
本周共有137项仿制药申报上市/申报临床获CDE承办,其中包括新注册分类上市申请114项和新注册分类临床申请6项,以及17项一致性评价申请。本周1个品种通过一致性评价,86个品种视同通过一致性评价。本周有4项生物类似物注册申报动态。数据显示,过评/视同过评品种主要为心血管系统药物,剂型主要为注射剂。注射用苯唑西林钠过评/视同过评受理号数量最多,达8个。石家庄四药有限公司和浙江高跖医药科技股份有限公司过评/视同过评品种数最多,达3种。
国内医药大健康行业政策法规汇总
本周发布的政策法规主要集中在药品审评审批、医疗设备配置和医院评审标准等方面。重点关注国家药品审评中心发布的《先进治疗药品的范围、归类和释义(征求意见稿)》,该文件旨在规范先进治疗药品的名称、范围及归类,促进相关产业高质量发展。
全球医药市场数据分析
全球创新药研发进展
本周全球TOP10创新药研发进展涵盖多个治疗领域,包括呼吸系统疾病、心血管疾病、肿瘤等。其中,默沙东的长效单抗药clesrovimab获批上市,用于预防儿童呼吸道合胞病毒感染;Alnylam Pharmaceuticals的新药vutrisiran获欧盟批准上市,用于治疗成人转甲状腺素运载蛋白淀粉样变性心肌病;丽珠医药的1类新药YJH-012临床试验申请获受理,用于治疗痛风;和誉医药的小分子癌症新药匹米替尼在中国申报上市,用于治疗腱鞘巨细胞瘤。
全球创新药临床试验结果
本周全球TOP10积极/失败临床结果显示,多个药物在临床试验中取得积极结果,例如Protagonist Therapeutics公司与武田公布的rusfertide 3期临床积极结果,以及默沙东公布的PCSK9抑制剂enlicitide decanoate双项3期试验积极结果等。这些积极结果为相关药物的进一步开发提供了有力支持。
总结
本报告对2025年6月9日至15日期间中国及全球医药行业的创新药、仿制药及政策法规动态进行了全面分析。数据显示,国内创新药研发持续活跃,但仿制药市场竞争激烈;全球创新药研发取得积极进展,多个药物获批或进入后期临床阶段。 未来,中国医药行业需要继续加强创新能力建设,同时关注仿制药市场的一致性评价,以提升市场竞争力。全球医药行业则需要持续关注创新药物的研发进展,并积极应对市场竞争和监管挑战。 本报告数据来源于摩熵医药数据库,更详细的数据和分析可通过摩熵医药数据库获取。
-

2025年中国临床试验数据洞察
-

摩熵咨询医药行业观察周报(2026.04.13-2026.04.19)
-

摩熵咨询医药行业观察周报(2026.04.06-2026.04.12)
-

摩熵咨询医药行业观察周报(2026.03.30-2026.04.05)
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






相关专题报告
对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送