-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

摩熵咨询医药行业观察周报(2025.05.05-2025.05.11)
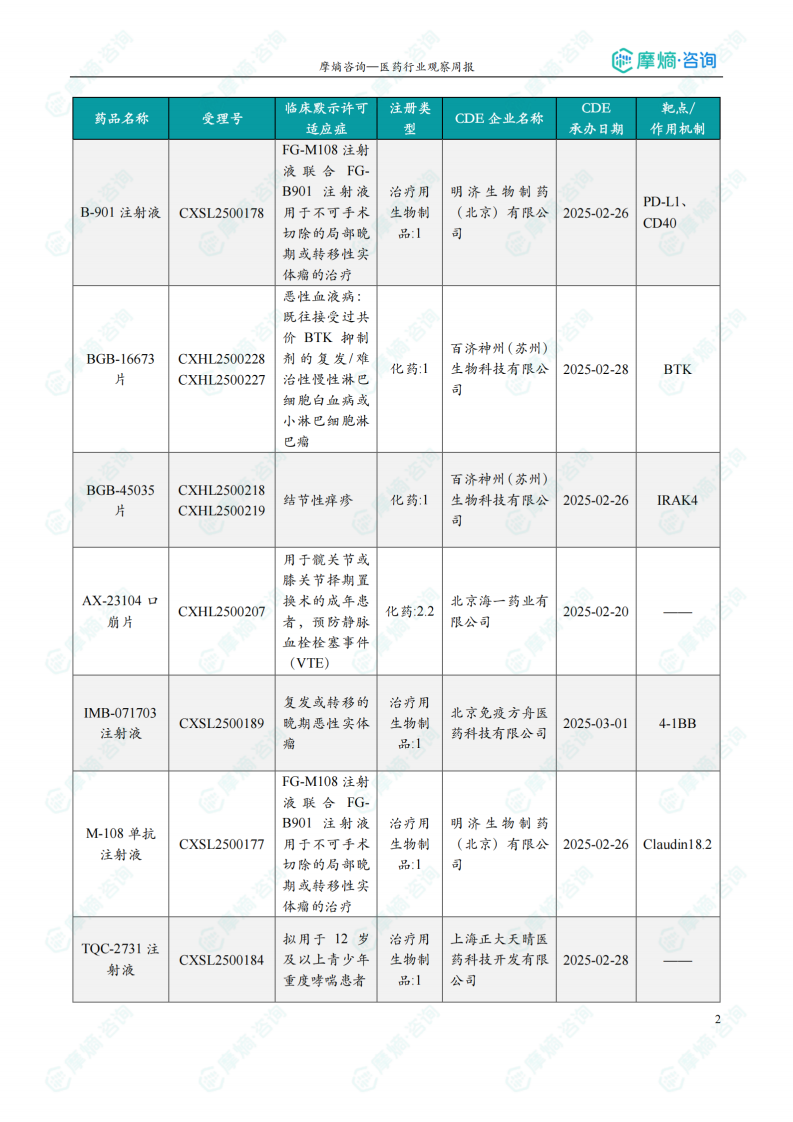
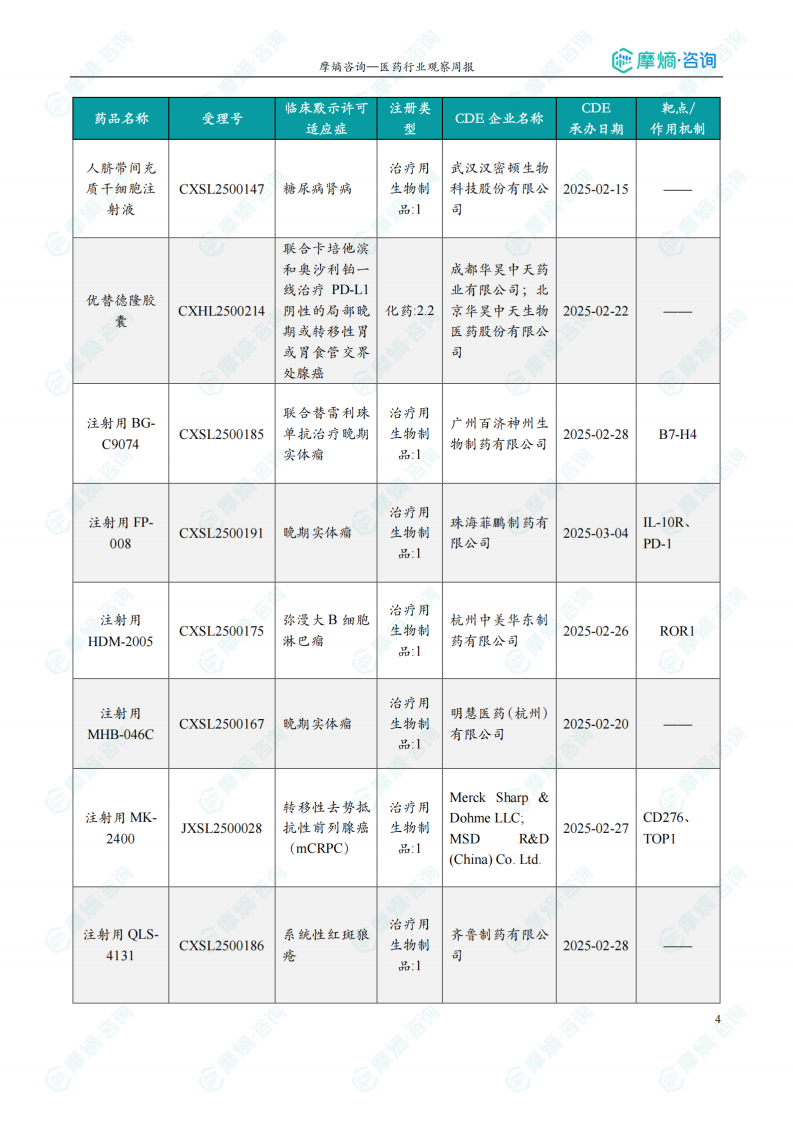
根据摩熵医药数据库统计,2025.05.05-2025.05.11期间共有52个创新药/改良型新药临床申请/上市申请获国家药品监督管理局药品审评中心(CDE)承办(按受理号统计,不含补充申请)。其中国产药品受理号43个,进口药品受理号9个。
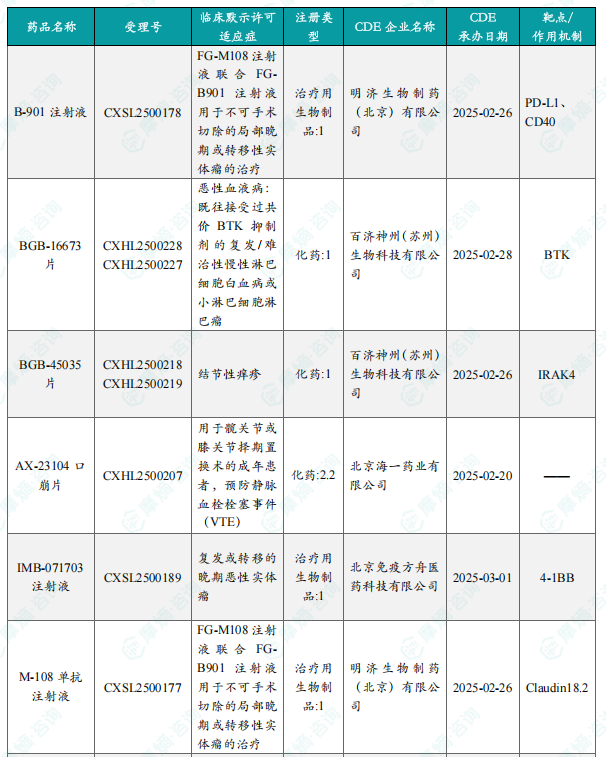
本周共计33款创新药/改良型新药临床试验申请获得“默示许可”,包括化学药14款,生物药19款,无中药。其中值得注意的有:
(1)ABBV-932胶囊
5月6日,CDE官网公示:艾伯维(AbbVie)的ABBV-932胶囊获得临床试验默示许可,用于治疗双相障碍抑郁发作。公开资料显示,ABBV-932胶囊是一款小分子新药,为一款选择性D3多巴胺受体调节剂,为DRD2和DRD3多巴胺受体调节剂。
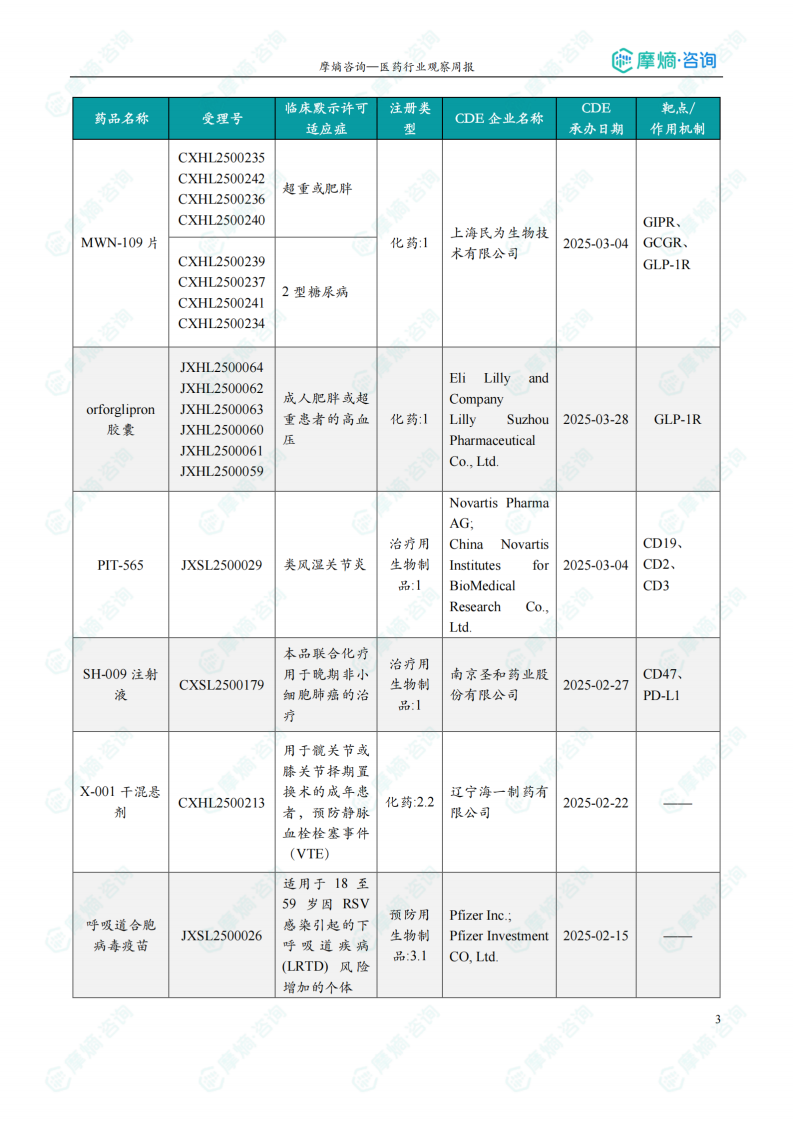
(2)注射用FP-008
5月8日,CDE官网公示:菲鹏制药的注射用FP-008获得临床试验默示许可,用于治疗晚期实体瘤。公开资料显示,注射用FP-008是菲鹏制药First-in-Class新药,是一种IL-10M与抗PD-1抗体融合的新型融合蛋白,旨在攻克野生型IL-10毒性限制的难关,为对PD-1/PD-L1抗体耐药的人群提供新的治疗手段。
(3)MWN-109片
5月9日,CDE官网公示:乐普医疗的MWN-109片获得临床试验默示许可,用于治疗痤疮。公开资料显示,MWN-109片是一款GLP-1/GIP/GCG活性脂肪酸链修饰多肽药物,MWN109片是在MWN109注射
液基础上开发的口服剂型,作用机理为通过刺激胰岛β细胞分泌胰岛素,有效控制血糖,通过延缓胃排空和抑制胃酸分泌,增加饱腹感,减少能量摄入,同时通过促进脂肪分解,增加能量排空和基础代谢,有效降低体重。
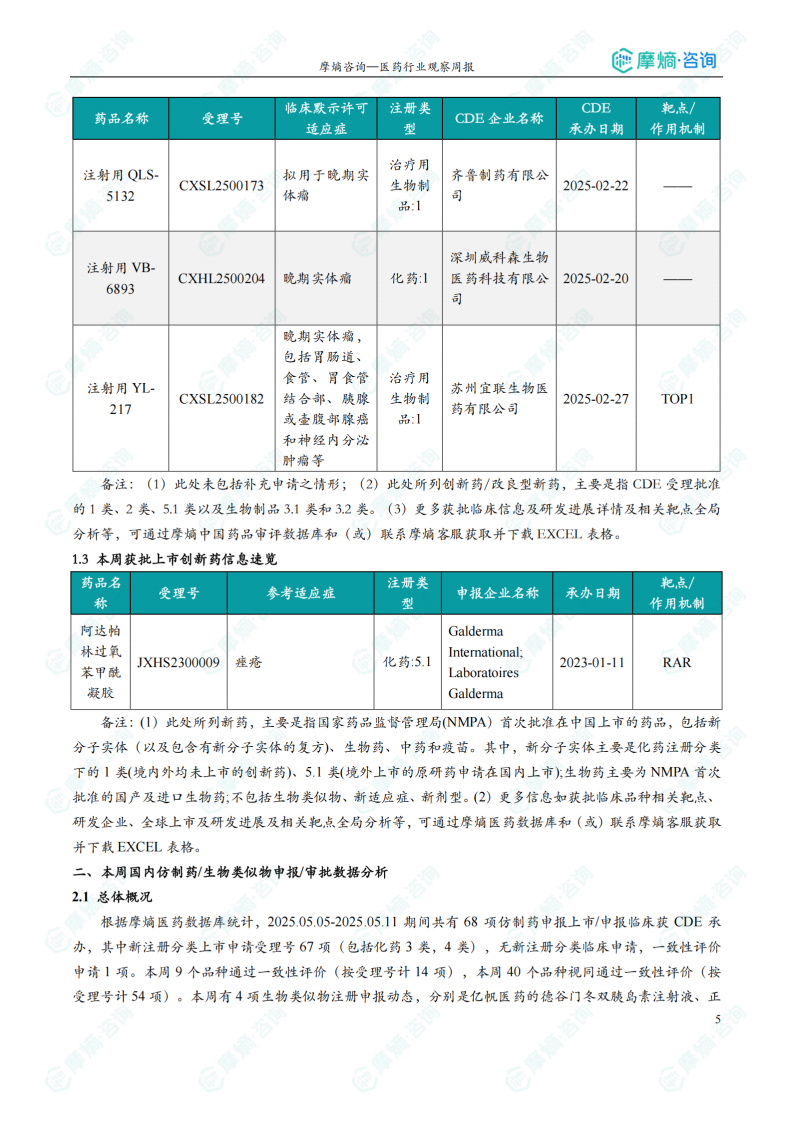
本周共1款新药获批上市,即阿达帕林过氧苯甲酰凝胶。
本报告涉及: 相关药物:阿达帕林过氧苯甲酰凝胶, 相关靶点:RAR, 相关适应症:痤疮 。
中心思想
本报告基于摩熵咨询医药数据库,对2025年5月5日至11日期间中国及全球医药行业创新药、仿制药及政策法规动态进行了数据分析,核心观点如下:
国内创新药研发进展迅速,仿制药一致性评价持续推进
国内创新药研发持续活跃,本周多个创新药获批临床,涵盖多个治疗领域,例如双相障碍、实体瘤、2型糖尿病、痤疮等。同时,阿达帕林过氧苯甲酰凝胶获批上市,为痤疮治疗提供了新的选择。仿制药方面,一致性评价工作稳步推进,多个品种通过或视同通过评价,其中法莫替丁注射液最为突出。
全球创新药研发竞争激烈,临床试验结果喜忧参半
全球范围内,多个创新药研发取得进展,例如Vanda Pharmaceuticals的Milsaperidone申请上市,百济神州的BGB-45035片获批临床,以及多个药物在临床试验中取得积极结果。然而,也有一些药物的临床试验结果未达到预期。
主要内容
国内医药市场数据分析
国内创新药/改良型新药研发动态
本周共有52个创新药/改良型新药临床申请/上市申请获CDE承办,其中国产药品43个,进口药品9个。33款创新药/改良型新药临床试验申请获得“默示许可”,包括化学药14款,生物药19款。值得关注的是艾伯维的ABBV-932胶囊(治疗双相障碍抑郁发作)、菲鹏制药的注射用FP-008(治疗晚期实体瘤)和乐普医疗的MWN-109片(治疗痤疮)。仅一款新药阿达帕林过氧苯甲酰凝胶获批上市,用于治疗痤疮。 数据显示,创新药研发在化学药和生物药领域均有较大的进展,但获批上市的创新药数量相对较少,这可能与新药审批流程的严格性有关。
国内仿制药/生物类似物申报审批动态
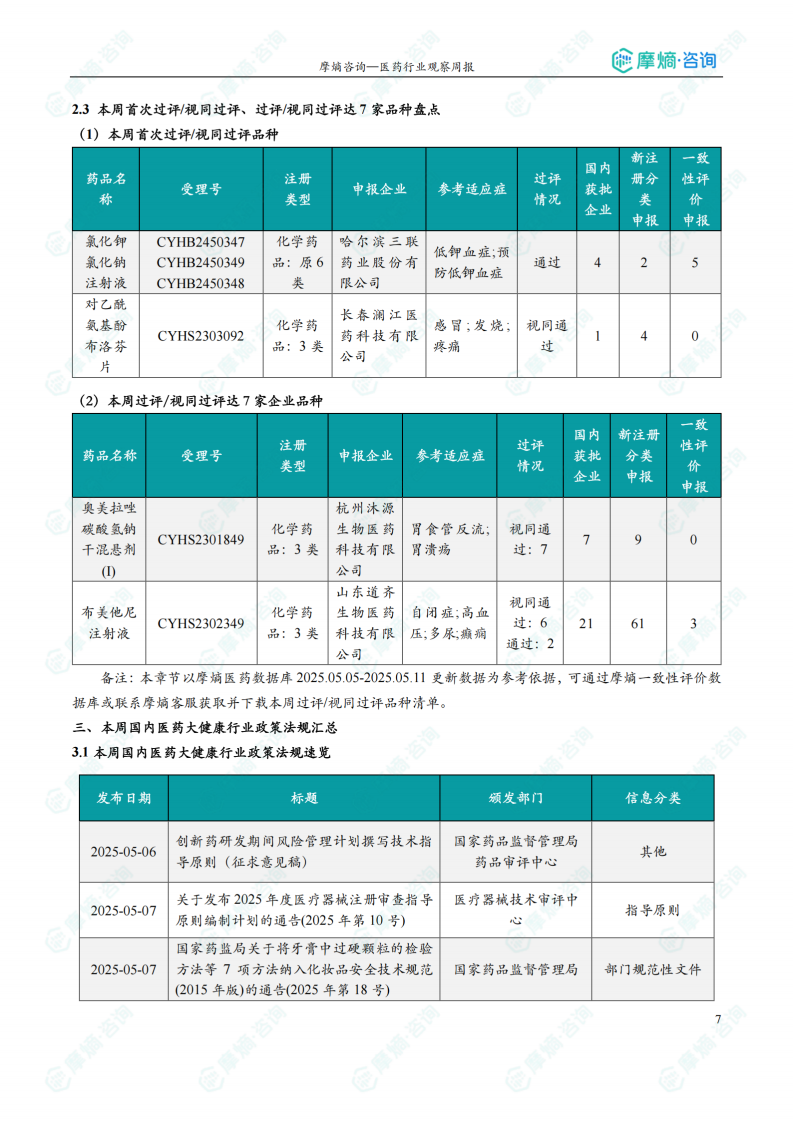
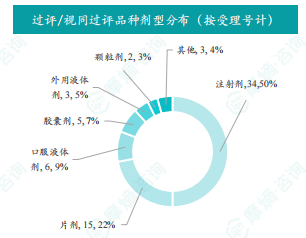
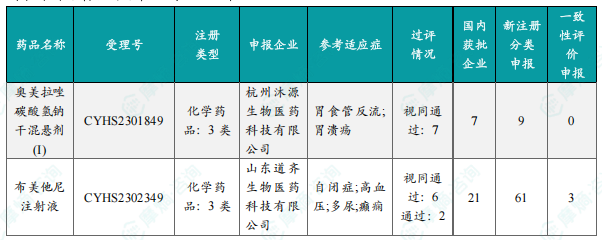
本周共有68项仿制药申报上市/申报临床获CDE承办,其中新注册分类上市申请受理号67项,一致性评价申请1项。9个品种通过一致性评价,40个品种视同通过一致性评价。本周有4项生物类似物注册申报动态。数据显示,仿制药市场竞争激烈,一致性评价是推动仿制药市场规范化发展的重要举措。消化系统与代谢药物以及注射剂是过评/视同过评品种的主要类别。法莫替丁注射液过评/视同过评受理号数量最多,过评/视同过评企业也最多。
国内医药大健康行业政策法规
本周主要政策法规包括国家药监局发布的《创新药研发期间风险管理计划撰写技术指导原则(征求意见稿)》等,这些政策法规的出台,旨在规范医药行业发展,保障药品安全有效。
全球医药市场数据分析
全球创新药研发进展
本周全球TOP10创新药研发进展涵盖多个国家和地区,涉及多个治疗领域,包括精神疾病、肿瘤、皮肤病等。多个创新药获批临床或上市,也有一些药物进入优先审评程序。这反映了全球医药研发竞争的激烈程度。
全球创新药临床试验结果
本周全球TOP10积极/失败临床结果显示,部分药物临床试验取得积极结果,例如Avacta Therapeutics公司的AVA6000、Coherus BioSciences公司的CHS-114、Immutep公司的eftilagimod alfa等,这些积极结果为相关疾病的治疗带来了新的希望。但也有一些药物的临床试验结果未达到预期,这提醒我们医药研发存在风险,需要谨慎对待。
总结
本报告通过对2025年5月5日至11日期间中国及全球医药行业数据的分析,展现了国内外医药市场创新药研发和仿制药一致性评价的最新动态,以及全球创新药研发竞争的激烈程度和临床试验结果的复杂性。国内创新药研发进展迅速,但获批上市数量相对较少;仿制药一致性评价持续推进,市场竞争激烈;全球创新药研发竞争激烈,临床试验结果喜忧参半。 这些信息为医药企业制定研发战略、投资决策以及监管部门制定相关政策提供了重要的参考依据。 未来,持续关注创新药研发进展、仿制药一致性评价以及相关政策法规动态,将有助于更好地把握医药市场发展趋势。
-

2025年中国临床试验数据洞察
-

摩熵咨询医药行业观察周报(2026.04.13-2026.04.19)
-

摩熵咨询医药行业观察周报(2026.04.06-2026.04.12)
-

摩熵咨询医药行业观察周报(2026.03.30-2026.04.05)
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






相关专题报告
对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送