-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

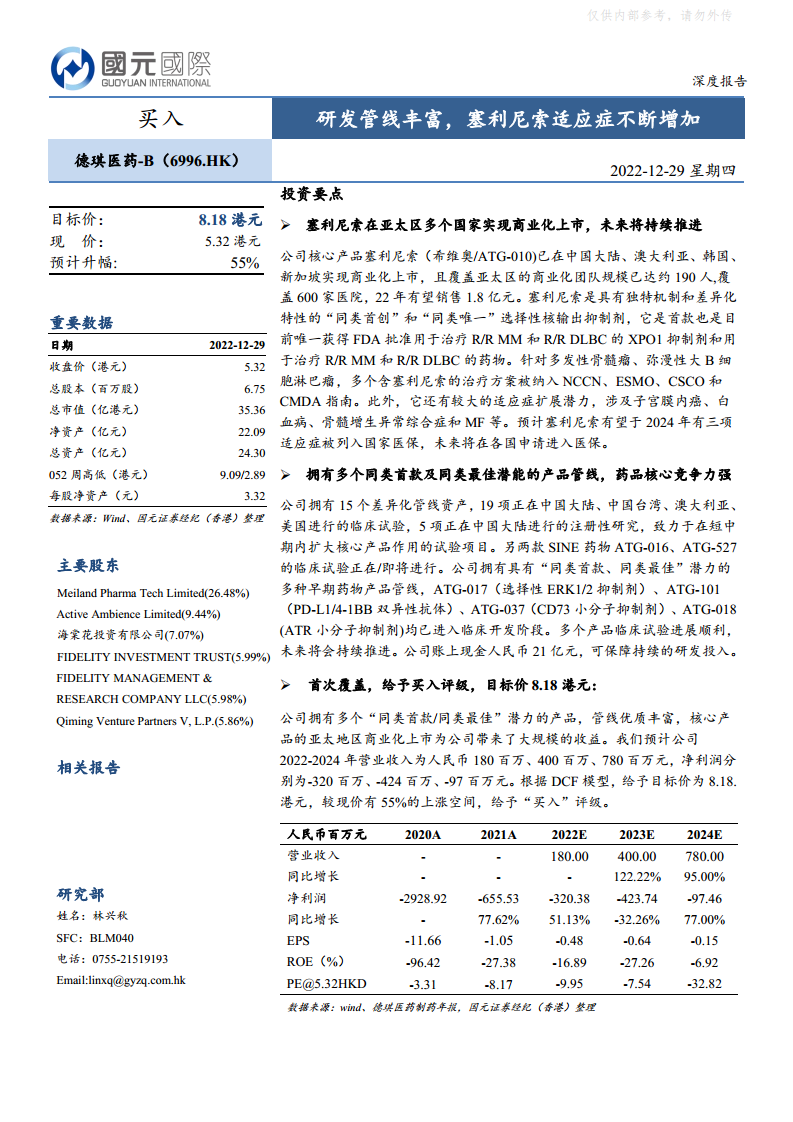
德琪医药B(6996.HK)研发管线丰富,塞利尼索适应症不断增加
德琪医药B(6996.HK)研发管线丰富,塞利尼索适应症不断增加
-
下载次数:
883 次
-
发布机构:
国元国际控股
-
发布日期:
2022-12-29
-
页数:
36页
中心思想
德琪医药:创新管线驱动亚太市场增长
德琪医药作为一家领先的亚太地区临床阶段生物制药公司,凭借其丰富的研发管线和核心产品塞利尼索在亚太市场的成功商业化,展现出强劲的增长潜力和市场竞争力。公司致力于开发“同类首创”、“同类唯一”及“同类最佳”疗法,尤其在肿瘤治疗领域,通过差异化的产品策略和一体化的全产业链布局,有望在未来实现显著的业绩增长和盈利能力提升。
塞利尼索:核心产品与广阔的适应症扩展前景
核心产品塞利尼索(希维奥/ATG-010)作为全球首款且目前唯一获得FDA批准用于治疗复发/难治性多发性骨髓瘤(R/R MM)和复发/难治性弥漫性大B细胞淋巴瘤(R/R DLBCL)的XPO1抑制剂,已在中国大陆、澳大利亚、韩国、新加坡实现商业化上市,并被纳入多个权威指南推荐。其独特的机制和差异化特性,以及在子宫内膜癌、白血病、骨髓增生异常综合症等多种适应症上的巨大扩展潜力,预示着其未来市场份额的持续扩大,预计2024年将有三项适应症被列入国家医保,进一步推动销售增长。
主要内容
1. 公司概况
1.1 公司简介
德琪医药是一家专注于发现、开发全球同类首款、同类唯一及/或同类最优疗法的亚太地区临床阶段生物制药公司。自2017年以来,公司已构建了一条由15款肿瘤药物组成的研发管线,并采用“组合、互补”的研发策略。核心产品包括希维奥(塞利尼索片/ATG-010),已在中国、澳大利亚、韩国和新加坡获批用于治疗复发/难治性多发性骨髓瘤及复发/难治性弥漫大B细胞淋巴瘤;以及口服双靶点mTORC1/2抑制剂ATG-008。公司与Bristol Myers Squibb、AstraZeneca、Karyopharm等多家知名公司合作,拥有超过400名员工,有效推动了国际化和商业化进程。
1.2 公司股权结构
公司最大股东为Meiland Pharma Tech Limited,持有总股本的26.48%。其他主要股东包括Active Ambience Limited (9.44%)、海棠花投资有限公司 (7.07%)、FIDELITY INVESTMENT TRUST (5.99%)、FIDELITY MANAGEMENT & RESEARCH COMPANY LLC (5.98%)和Qiming Venture Partners V, L.P. (5.86%)。
1.3 业务概要
德琪医药专注于创新抗肿瘤药物研发,涵盖血液瘤和实体瘤,产品管线包含新型肿瘤免疫药物和靶向药物,旨在实现更多新型联合疗法。其创新性体现在:
- 协同潜力作用机制:联合SINE、TKI、I/O三者。
- 多重靶点覆盖:贯连细胞膜靶点、胞内靶点、核内靶点。
- 多样化药物种类:涉及小分子药物、单抗药物、双特异性抗体。 公司核心产品塞利尼索已在中国大陆、新加坡、澳大利亚、韩国等地区商业化上市,并计划进入各国医保。ATG-008是口服双靶点mTORC1/2抑制剂,处于多项临床试验中。公司有4款全球权益资产(ATG-017、ATG-101、ATG-037、ATG-018)进入临床开发阶段,并推出了3个自主发现的新型小分子药物(ATG-031、ATG-032、ATG-041)靶向巨噬细胞。此外,还有5个管线品种(ATG-018、ATG-022、ATG-012、ATG-031、ATG-027)处于IND准备阶段。公司已与百时美施贵宝、Calithera Bioscience、Legochem Bioscience等公司达成合作,并在绍兴和杭州建立了生产基地和研发及产业化基地。
2. 行业概况
2.1 肿瘤药物市场全面概况及发展趋势分析
全球癌症发病率持续上升,2020年全球新发癌症病例达1930万例,较2015年的1670万例有所增加。中国在2020年新发癌症病例457万例,占全球总数的23.7%,位居全球第一。预计到2040年,全球新发癌症将达到2840万例。肺癌、结直肠癌、胃癌等十种癌症占2020年中国新发癌症总数的78%。 受发病率上升、人口老龄化等因素驱动,肿瘤药物市场需求旺盛。2019年全球肿瘤市场规模为1435亿美元,占全球医药市场的10.8%;预计到2030年将达到3657亿美元,占比18.3%。中国肿瘤药物市场规模在2019年为264亿美元,占中国医药市场的11.2%,预计到2030年将达到887亿美元,占比20.3%,增速将高于同期美国、欧盟及全球市场。 癌症治疗主要包括外科手术、放疗、化疗、分子靶向疗法及免疫疗法。其中,分子靶向疗法和免疫疗法是创新型治疗方式。2015年至2019年,FDA批准的57种新型肿瘤药物均为分子靶向疗法或免疫疗法。2019年,分子靶向疗法在全球肿瘤药物市场中占比最大,达62.6%,预计到2030年,分子靶向疗法及免疫疗法将共占肿瘤市场的90%以上。
2.2 特定肿瘤药物市场概况
德琪医药的核心产品塞利尼索主要针对多发性骨髓瘤和弥漫性大B细胞瘤。
2.2.1 多发性骨髓瘤
多发性骨髓瘤是全球第二常见的血液系统恶性肿瘤。亚太地区新发病例数从2019年的15.69万例预计增至2030年的41.01万例,年复合增长率为10.4%(2019-2024年)。中国新发病例数从2019年的2.07万例预计增至2030年的2.77万例;患病人数从2019年的10.19万例预计增至2030年的26.63万例。 中国多发性骨髓瘤药物市场规模在2019年为人民币57亿元,预计到2024年将达到人民币147亿元(年复合增长率20.7%),并进一步增至2030年的人民币267亿元。目前,中国多发性骨髓瘤的靶向治疗方案主要分为IMiD、蛋白酶体抑制剂及抗CD38单抗。塞利尼索作为具有全新作用机制的XPO1抑制剂,对于现有疗法难治的复发/难治性多发性骨髓瘤患者提供了重要治疗选择。
2.2.2 弥漫性大B细胞瘤(DLBCL)
弥漫性大B细胞瘤是最常见的非霍奇金氏淋巴瘤(NHL)类型,约占全球NHL病例总数的25.5%,中国NHL病例总数的45.8%。亚太地区DLBCL新发病例数从2019年的5.44万例预计增至2030年的6.98万例,年复合增长率为2.4%(2019-2024年);患病人数从2019年的13.55万例预计增至2030年的18.73万例,年复合增长率为4.7%(2019-2024年)。中国DLBCL新病例数从2019年的3.53万例预计增至2030年的4.53万例;患病人数从2019年的19.91万例预计增至2030年的29.93万例。 中国DLBCL药物市场规模在2019年为人民币58亿元,预计到2024年将达到人民币186亿元(年复合增长率26.2%),并进一步增至2030年的人民币369亿元。尽管一线治疗主要采用“R-CHOP”疗法,但约15%的患者会出现原发耐药。塞利尼索作为XPO1抑制剂,有望成为治疗复发/难治性弥漫性大B细胞淋巴瘤患者的重要疗法,以满足未被满足的市场需求。
3. 重点产品介绍
3.1 塞利尼索(ATG-010)
塞利尼索是“同类首创”和“同类唯一”的选择性核输出抑制剂,是首款也是目前唯一获FDA批准用于治疗R/R MM和R/R DLBCL的XPO1抑制剂。该药物已在中国大陆、澳大利亚、韩国和新加坡获批,并获得NCCN和CSCO指南推荐。临床研究如BOSTON、STORM、STOMP、SADAL等均证实了其在MM和DLBCL治疗中的临床获益。BOSTON研究显示,即使65%的患者接受了剂量下调,仍获得了16.6个月的PFS。目前,塞利尼索有12个在研项目,涉及9个适应症,并具有巨大的适应症扩展潜力,包括子宫内膜癌、白血病、骨髓增生异常综合症和骨髓纤维化等。 公司还拥有两款SINE药物:ATG-016(第二代XPO1抑制剂),具有更好的药理特性和更低的血脑屏障渗透性,用于治疗高危MDS患者;ATG-527(第三代XPO1抑制剂),用于非肿瘤适应症,如CAEBV及SLE。
3.1.2 竞争格局
塞利尼索是全球首款且唯一获认可的XPO1抑制剂,具有经验证的新作用机制、改善的疗效、口服给药、降低剂量频率及联合疗法的潜力,在多发性骨髓瘤治疗方面具有显著竞争优势。其sNDA(联合硼替佐米与地塞米松用于治疗二线多发性骨髓瘤)已被FDA接受。2021年,塞利尼索在韩国上市约半年后,产品收入达2880万元。截至2022年6月30日,在中国内地推出后,公司收入达5396万元,预计2022年全年销售额将达1.8-2亿元,覆盖600家医院。目前中国尚无其他XPO1抑制剂获批上市。在DLBCL治疗方面,塞利尼索同样具有竞争优势,中国目前尚无其他XPO1抑制剂处于临床开发阶段。
3.2 ATG-008(mTORC1/2 抑制剂)
ATG-008是“同类首款”的第二代口服双靶点mTORC1/2抑制剂,用于治疗肝癌、非小细胞肺癌、胃癌等晚期实体瘤及血液系统恶性肿瘤。它能同时抑制mTORC1及mTORC2,阻断PI3K/AKT信号通路的反馈激活,在临床及临床前研究中展现出广泛的抗肿瘤活性。ATG-008还具有与SINE化合物、ERK1/2抑制剂(ATG-017)联用的潜力。其TORCH-2研究预计于2022年第三季度完成剂量扩展部分(宫颈癌),并于第四季度与CDE沟通注册性研究方案,目前处于II期临床阶段。
3.3 ATG-017(ERK1/2抑制剂)
ATG-017是一款具有“同类最佳”潜力的ERK1/2抑制剂,强效高选择性靶向作用于细胞外调节激酶1和2,适用于RAS/MAPK通路异常导致的血液系统恶性肿瘤和实体肿瘤,如非小细胞肺癌、胰腺癌、结肠癌、黑色素瘤等,并可与免疫药物联用。其优势包括领先的临床开发进度(I期首次人体试验ERASER已启动)、广泛的治疗潜力及与ATG-012、ATG-101联用的潜在协同效应。在同类产品竞争中,ATG-017展现出更强效力、双重IoC和PoA活性、缓慢脱速率动力学特性、更低的起效剂量和更高的多提升剂量/剂量比。
3.4 ATG-101(PD-L1/4-1BB双特异性抗体)
ATG-101是独特且具有“同类最佳”潜力的PD-L1/4-1BB双特异性抗体,能同时阻断PD-L1/PD-1结合并激活4-1BB共刺激信号,从而激活抗肿瘤免疫效应细胞。在PD-L1过表达肿瘤细胞存在时,ATG-101表现出显著的PD-L1交联依赖的4-1BB激动剂活性,有望在提高治疗效果的同时减轻肝毒性。PROBE(澳大利亚、美国)和PROBE-CN(中国)研究正在进行中。ATG-101可结合塞利尼索、ATG-017、ATG-037、
-

李宁(2331.HK)优先提升渠道健康度,期待未来轻装上阵
-

友芝友生物B(2496.HK)IPO申购指南
-

亚盛医药B(6855.HK)奥雷巴替尼放量在即,重磅新药临床进展顺利
-

东曜药业-B(1875.HK)与智核生物合作进入核药领域,CDMO空间广阔
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送