-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

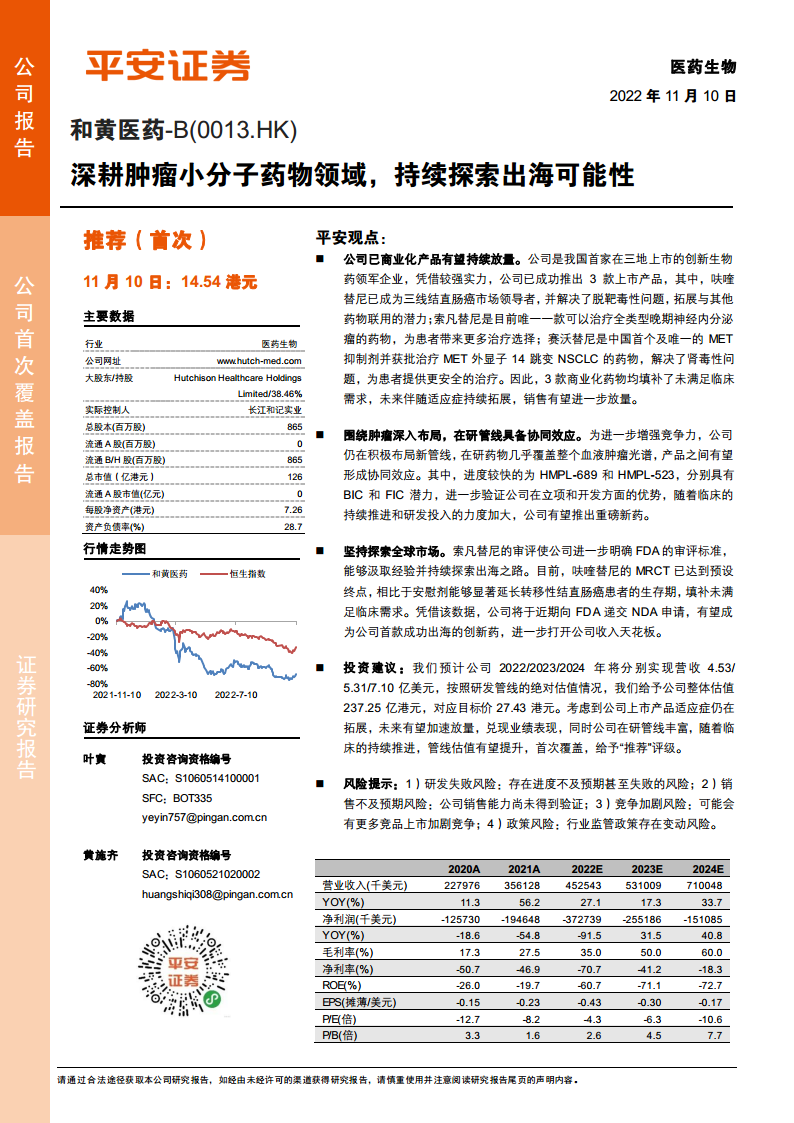
和黄医药-B(0013.HK)深耕肿瘤小分子药物领域,持续探索出海可能性
和黄医药-B(0013.HK)深耕肿瘤小分子药物领域,持续探索出海可能性
-
下载次数:
660 次
-
发布机构:
平安证券
-
发布日期:
2022-11-10
-
页数:
27页
中心思想
创新药企的商业化与全球化战略
和黄医药-B(0013.HK)作为一家在中美两地布局并已在三地上市的创新生物药领军企业,正凭借其强大的自主研发平台和差异化的产品管线,加速推进商业化进程并积极拓展全球市场。公司已成功推出三款创新肿瘤药物——呋喹替尼、索凡替尼和赛沃替尼,这些产品均填补了未满足的临床需求,并在各自细分市场中展现出领先地位或独特优势。通过持续的适应症拓展和医保准入,这些商业化产品有望实现销售额的快速增长。
多维度驱动增长:产品放量、管线深化与出海拓展
公司未来的增长将由多个维度驱动:首先,现有商业化产品将通过适应症的持续拓展和市场渗透率的提升实现放量;其次,公司围绕肿瘤领域构建的丰富在研管线,特别是血液肿瘤领域,具备显著的协同效应和BIC/FIC潜力,有望带来新的重磅产品;最后,公司坚持探索全球市场,通过国际多中心临床试验(MRCT)和与国际药企的合作,逐步打开海外收入天花板,实现从中国创新走向全球创新的战略目标。尽管公司目前仍处于亏损阶段,但充足的现金储备和高效的销售团队为其长期发展提供了坚实基础。
主要内容
一、在中美两地布局的创新生物药企业
1.1 公司是三地上市的创新生物药领军企业之一
- 公司概况与定位: 和黄医药成立于2000年,专注于癌症及免疫性疾病领域的药物发现、开发及商业化。公司凭借强大的研发实力,已成功推出3款创新肿瘤药物:呋喹替尼、索凡替尼和赛沃替尼。
- 上市地位: 公司于2006年在伦敦证券交易所AIM上市,2016年在纳斯达克上市,并于2021年登陆港交所,是首家在三地上市的创新生物药领军企业之一。
- 管理团队与股权结构: 公司核心高管团队经验丰富,首席执行官兼首席科学官苏慰国博士、总经理及首席医学官Marek KANIA医生、首席运营官安凯伦以及研发负责人兼首席医学官石明博士均在各自领域拥有深厚背景,有望提升公司的全球临床推进能力和商业化效率。截至2022年上半年,长江和记实业有限公司通过其附属公司持有公司38.5%的股权,为公司单一最大股东,股权结构稳定。
1.2 管线丰富具备差异化,进一步开拓全球市场
- 财务表现与研发投入: 公司目前尚未实现盈利,但营收持续增长。2021年和2022年上半年,公司分别实现销售收入9850万美元和8740万美元,同比增长192%和82%(2022年上半年增速受疫情影响有所下降)。加上研发服务及里程碑收入,2021年和2022年上半年总营收分别为3.56亿美元和2.02亿美元。同期,研发投入持续增加,2021年达到2.99亿美元,同比增长71%。截至2022年上半年,公司账面现金储备达8.26亿美元,为研发和商业化提供支持。
- 商业化产品销售情况: 公司已商业化的3款产品(呋喹替尼、索凡替尼、赛沃替尼)具有差异化优势,填补了未满足的临床需求。其中,呋喹替尼是主要收入来源,2022年上半年销售额达0.5亿美元,占产品总收入的57.6%。赛沃替尼在未进入医保的情况下也实现了快速放量。
- 销售团队效率: 截至2022年上半年,公司销售团队规模达820人,覆盖约3000家肿瘤医院和约30000名肿瘤医生。2021年和2022年上半年的销售费用率分别为31.63%和24.40%,显著低于同行业可比公司平均水平(47.42%和58.97%)。同期,人均创收分别达到395.70万元和172.48万元,显著高于同行业可比公司平均水平(230.11万元和82.53万元),显示出较高的销售效率。
- 研发管线与全球布局: 公司已开发出13款产品,其中7款同时在美国和欧洲进行临床试验,展现出全球化布局的战略。产品管线围绕肿瘤主要信号通路进行开发,有望形成协同作用,其中6款药物几乎覆盖整个血液肿瘤光谱,发展战略清晰。
二、上市药物持续拓展适应症和海外市场
2.1 呋喹替尼:有望成为全球最佳靶点选择性的VEGFR抑制剂
- 作用机制与市场潜力: 呋喹替尼是一种具有优异激酶选择性的VEGFR抑制剂,通过抑制肿瘤新生血管形成来发挥抗肿瘤作用,且脱靶毒性问题较少。全球VEGFR疗法市场规模巨大,2020年已达200亿美元,预计2030年将增至521亿美元。
- 中国市场表现: 呋喹替尼于2018年11月获批用于三线结直肠癌(CRC),并于2020年纳入国家医保目录,实现快速放量。2021年中国销售额达7100万美元,同比增长111%。根据IQVIA数据,2022年第二季度呋喹替尼在中国30大城市(主要为三甲医院)的市场占有率已达43%,处于市场领导地位。
- 适应症拓展与临床数据: 呋喹替尼正在开展多种实体瘤的临床试验,包括中国二线胃癌和二线子宫内膜癌的III期临床。针对三线结直肠癌的中国III期FRESCO研究显示,治疗组中位总生存期(mOS)为9.3个月,安慰剂组为6.6个月;中位无进展生存期(mPFS)为3.7个月,安慰剂组为1.8个月,疗效显著。与同类药物瑞戈非尼相比,呋喹替尼在疗效和安全性方面均展现出优势。
- 全球化进展: 呋喹替尼治疗三线及以上结直肠癌的全球III期注册临床FRESCO-2已达到预设终点,数据显示治疗组mOS为7.4个月,安慰剂组为4.8个月;mPFS为3.7个月,安慰剂组为1.8个月,且安全性良好。公司预计近期将向FDA递交新药上市申请(NDA),有望成为公司首款成功出海的创新药。
2.2 索凡替尼:具有独特抗肿瘤血管生成和免疫侵袭的双靶点
- 作用机制与市场需求: 索凡替尼是一种多靶点抑制剂,同时靶向VEGFR1/2/3、FGFR1和CSF-1R,通过抑制血管生成并促进免疫应答来发挥抗肿瘤活性。神经内分泌瘤(NET)患者数量较多,中国2020年新增患者约7.13万名,其中非胰腺病例6.11万例,胰腺病例0.91万例。中国NET市场规模预计将从2020年的60亿美元增长至2030年的215亿美元。
- 中国市场表现与适应症: 索凡替尼于2020年和2021年在中国获批两项适应症,分别为非胰腺神经内分泌瘤(npNET)和胰腺神经内分泌瘤(pNET),是目前唯一一款可以治疗所有类型晚期NETs的药物。2022年1月纳入国家医保目录后,价格下降52%,患者可及性大幅提升,2022年上半年治疗患者数量同比增长约280%,销售收入达1360万美元,同比增长69%。
- 临床数据: 针对npNET的中国III期SANET-ep研究显示,索凡替尼组mPFS为9.2个月,安慰剂组为3.8个月。针对pNET的中国III期SANET-p研究显示,索凡替尼组mPFS为10.9个月,安慰剂组为3.7个月,均展现出显著疗效和良好的安全性。
- 全球化进展: 索凡替尼已获得FDA“孤儿药资格”和2项“快速通道资格”。尽管2022年5月FDA因数据包不足拒绝了上市申请,但公司正与监管部门沟通全球多中心临床试验(MRCT)的设计,有望再次尝试出海。
2.3 赛沃替尼:中国同类首创且唯一的选择性MET抑制剂
- 作用机制与市场潜力: 赛沃替尼是一种强效且选择性的MET抑制剂,针对MET外显子14跳变等异常活化机制,在肿瘤增殖、转移和耐药性中发挥关键作用。肺癌是全球最常见的癌症,MET突变在NSCLC患者中占4.0%至6.0%,且约20%的EGFR耐药患者存在MET突变。全球小分子MET抑制剂市场预计将从2020年的16亿美元增长至2030年的162亿美元,中国市场预计将从2.3亿美元增长至48.5亿美元。
- 中国市场地位与适应症: 赛沃替尼于2021年获批上市,是中国首个用于治疗MET外显子14跳变NSCLC患者的高选择性口服MET抑制剂,具有显著的先发优势。公司正在国内开展4项注册性临床研究,包括治疗三代EGFR耐药NSCLC,有望在2024年提交NDA。
- 临床数据与安全性: 赛沃替尼在中国II期临床研究中,客观缓解率(ORR)为42.9%,中位总生存期(mOS)为12.5个月,与同类可比药物(如卡马替尼、特泊替尼)数据具有可比性,且在入组患者基线更差的情况下仍表现良好。赛沃替尼在迄今为止的研究中未显示任何肾毒性,解决了第一代选择性MET抑制剂的肾毒性问题,具有更好的安全性和耐受性。
- 全球化合作: 公司已将赛沃替尼的全球权益授予阿斯利康,目前正在开展3项全球注册研究,有望进一步探索海外市场。
三、在研药物完善肿瘤靶点布局
3.1 安迪利塞(HMPL-689):有潜力成为BIC的PI3Kδ抑制剂
- 靶点与市场挑战: PI3K是肿瘤治疗领域的热门靶点,尤其PI3Kδ在B细胞介导的恶性肿瘤和多种免疫疾病中发挥关键作用。然而,全球已上市的5款PI3K抑制剂普遍存在严重的毒副作用,部分甚至收到FDA的黑框警告或撤销适应症上市申请。
- 产品优势与临床进展: HMPL-689对PI3Kδ亚型具有优异的选择性,且保留PI3Kα和PI3Kγ活性,在临床前研究中显示出相比同类药物更高的效力(效力较Zydelig强约五倍)和更强的选择性。其I期临床已初步验证了良好的安全性,3级以上不良事件发生率和因不良事件中断治疗的患者比例均远低于其他PI3K抑制剂,具有Best-in-Class(BIC)潜力。
- 适应症与上市计划: HMPL-689正在中国开展针对r/r滤泡性淋巴瘤(FL)、r/r边缘区淋巴瘤(MZL)和霍奇金淋巴瘤(HL)以及非霍奇金淋巴瘤(NHL)的临床试验,并在美国开展r/r NHL的临床。2021年9月,HMPL-689在中国获纳入突破性治疗药物品种,用于治疗r/r滤泡性淋巴瘤。中国II期临床试验正在进行中,预计2023年上半年完成MZL队列患者招募,有望于2023年递交上市申请。
3.2 索乐匹尼布(HMPL-523):有潜力成为首种治疗血液癌症的选择性Syk抑制剂
- 作用机制与靶点: HMPL-523是一种新型、高选择性靶向Syk的口服抑制剂。Syk是B细胞信号通路的关键酪氨酸激酶,在B细胞增殖、分化和免疫反应中发挥重要作用,同时涉及非淋巴细胞的信号传导。Syk已成为多种B细胞淋巴瘤和自身免疫疾病的热门治疗靶点。
- 临床进展与产品优势: HMPL-523正在澳洲、美国、欧洲及中国进行单药疗法的多项临床试验,同时布局自身免疫性疾病和血液肿瘤领域。免疫性血小板减少症(ITP)注册研究已在中国启动,并获纳入突破性治疗药物品种。HMPL-523在开发时注重安全性,具有独特的药代动力学特质,在临床前研究中展现出良好的耐受性。针对r/r ITP的I/II期研究结果显示,患者总应答率为80%,持续应答率为40%,有望为患者带来更多治疗选择。预计HMPL-523有望于2023年递交上市申请。
四、投资建议和盈利预测
4.1 绝对估值
- 峰值销售预测: 根据对公司已上市和临床后期核心产品管线的假设,预计公司峰值销售收入将在2030年达到约70亿元人民币(约10.99亿美元)。其中,呋喹替尼、索凡替尼、赛沃替尼和安迪利塞的峰值销售额预计分别为23.01亿元、6.53亿元、14.58亿元和0.16亿元人民币。
- DCF估值: 采用DCF估值模型,关键假设包括无风险利率3.0%、市场预期回报率8.0%、债务成本10.0%、债务资本比重10%、永续增长率1.5%,加权平均资本成本(WACC)为10.00%。基于此,估算公司当前合理市值为215.68亿元人民币(约237.25亿港元),对应总股本8.65亿股的合理价值约为27.43港元/股。
- 敏感性分析: 在WACC 9.07%至11.42%和永续增长率1.36%至1.66%的范围内,公司合理估值范围为206.35亿至226.06亿元人民币(约226.99亿至248.67亿港元),对应合理股价范围为26.24至28.75港元/股。
4.2 相对估值
- P/S估值: 考虑到公司仍处于亏损状态,不适用传统P/E估值方法,因此采用P/S作为相对估值方式。选取百济神州、信达生物、君实生物、荣昌生物和诺诚健华等已商业化的港股生物创新药公司作为可比公司。可比公司的P/S平均值为17.30x,中值为17.90x。而和黄医药当前的P/S为5.11x(以11月10日收盘价计算),处于可比公司中的低位水平。
4.3 投资建议
- 评级与目标价: 综合绝对估值和相对估值情况,给予公司整体估值237.25亿港元,对应目标价27.43港元,首次覆盖给予“推荐”评级。
- 短期驱动因素:
- 商业化产品放量: 呋喹替尼、索凡替尼和赛沃替尼三款已商业化产品有望持续放量。其中,呋喹替尼已成为三线结直肠癌市场领导者,三甲医院市占率超40%,且其安全性优势有望推动联合疗法和前线治疗。索凡替尼是目前唯一可治疗所有类型晚期神经内分泌瘤的药物,进入医保后患者数量和销售额均大幅增长。赛沃替尼作为中国首个获批治疗MET外显子14跳变NSCLC的MET抑制剂,解决了肾毒性问题,安全性良好,并有多个注册性临床研究正在推进。
- 中长期驱动因素:
- 丰富在研管线: 公司持续围绕肿瘤深入布局,在研药物几乎覆盖整个血液肿瘤光谱,产品之间有望形成协同效应。HMPL-689(安迪利塞)和HMPL-523(索乐匹尼布)分别具有BIC和FIC潜力,随着临床持续推进和研发投入加大,有望推出重磅新药。
- 积极布局全球市场: 呋喹替尼的全球III期MRCT已达到预设终点,有望近期向FDA递交NDA,成为公司首款成功出海的创新药。赛沃替尼在合作伙伴阿斯利康的推动下,也正在开展3项全球注册研究,有望进一步探索海外自由定价市场。索凡替尼虽此前出海受挫,但公司已明确FDA审评标准,正积极沟通并计划开展新的MRCT。
五、风险提示
5.1 研发失败风险
公司多数产品仍处于研发阶段,新药研发受资金、政策、技术等多因素影响,存在进度不及预期甚至失败的可能。
5.2 销售不及预期
公司刚步入商业化元年,销售能力尚需进一步验证,存在销售不及预期的风险。
5.3 竞争加剧风险
未来可能会有更多企业的同类产品上市,导致市场竞争加剧。
5.4 政策风险
作为新兴技术领域,行业监管政策存在发生变动的风险。
总结
和黄医药-B作为创新生物药领域的领军企业,凭借其在中美两地的深厚布局和三地上市的独特地位,展现出强劲的增长潜力。公司已成功商业化的三款肿瘤创新药——呋喹替尼、索凡替尼和赛沃替尼,通过解决未满足的临床需求、持续拓展适应症和优化医保准入,已在中国市场取得显著进展,并有望持续放量。其中,呋喹替尼已成为三线结直肠癌市场的领导者,索凡替尼是唯一可治疗所有类型晚期神经内分泌瘤的药物,而赛沃替尼则以其独特的选择性和安全性优势,填补了MET外显子14跳变NSCLC治疗的空白。
在中长期发展方面,公司拥有丰富的在研管线,尤其在血液肿瘤领域,HMPL-689和HMPL-523等产品具备成为BIC或FIC的潜力,有望为公司带来新的增长点。同时,公司积极推进全球化战略,呋喹替尼的全球多中心临床试验成功,预示着其有望成为公司首款成功出海的创新药,将显著拓宽收入来源。尽管索凡替尼的出海之路面临挑战,但公司正积极调整策略,持续探索海外市场。
综合来看,和黄医药-B目前估值处于行业相对低位,但其强大的研发实力、高效的商业化能力和清晰的全球化战略,预示着未来业绩增长和管线价值提升的巨大空间。基于对公司研发管线的绝对估值和相对估值分析,我们给予公司“推荐”评级,目标价为27.43港元。然而,投资者仍需关注研发失败、销售不及预期、竞争加剧以及政策变动等潜在风险。
-

生物医药行业:2025年首次新增商保目录,医保及商保目录预计今年10-11月公布结果
-

国产新药闪耀ASCO2025,关注相关企业投资机遇
-

皓元医药(688131):前端业务促使业绩增长,利润率延续改善状态
-

“大家一起找不同”之医药基金经理篇
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送