-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

再鼎医药(09688):重磅数据将在ASCO发表,多个产品今年获批或报产
再鼎医药(09688):重磅数据将在ASCO发表,多个产品今年获批或报产
-
下载次数:
1573 次
-
发布机构:
德邦证券
-
发布日期:
2023-05-19
-
页数:
4页
中心思想
商业化盈利能力显著提升
再鼎医药在2023年第一季度展现出强劲的商业化能力,产品收入实现快速增长,并首次实现单季度商业化盈利,标志着公司在财务健康方面迈出了重要一步。
多重催化剂驱动未来增长
公司未来增长潜力巨大,主要得益于肿瘤电场治疗(Optune)LUNAR研究在ASCO大会上即将公布的重磅数据,以及多个创新产品管线密集兑现里程碑,包括艾加莫德α、KarXT等,这些都将成为公司短期和中长期的重要增长驱动力。
主要内容
财务表现与盈利能力分析
22023年Q1业绩点评:收入快速增长,已实现单季度商业化盈利
- 产品收入增长强劲: 2023年第一季度,公司产品收入达到6,280万美元,同比增长36.2%。
- 核心产品贡献:
- 则乐(Zejula)销售收入为4,270万美元,同比增长44.3%。
- 爱普盾(Optune)销售收入为1,330万美元,同比增长3.9%。
- 擎乐(QINLOCK)销售收入为130万美元。
- 纽再乐(NUZYRA)销售收入为550万美元,同比增长高达685.7%。
- 实现商业化盈利: 2023年第一季度总收入6,280万美元已超过销售、管理及行政(SG&A)开支6,250万美元,表明公司已实现单季度商业化盈利。
- 现金储备充足: 截至2023年3月31日,公司拥有9.314亿美元的现金储备,为后续发展提供坚实保障。
盈利预测与投资建议
- 收入预测: 德邦研究所预计公司2023/2024/2025年将实现收入分别为3.11/4.91/8.70亿美元,显示出持续高速增长的预期。
- 投资评级: 鉴于公司商业化产品销售高速增长以及多款在研管线蓄势待发,维持“买入”评级。
- 风险提示: 临床失败风险、竞争恶化风险、销售不及预期风险、行业政策风险等。
核心产品线进展与市场展望
关注2023ASCO大会,电场治疗数据或为短期最重要催化
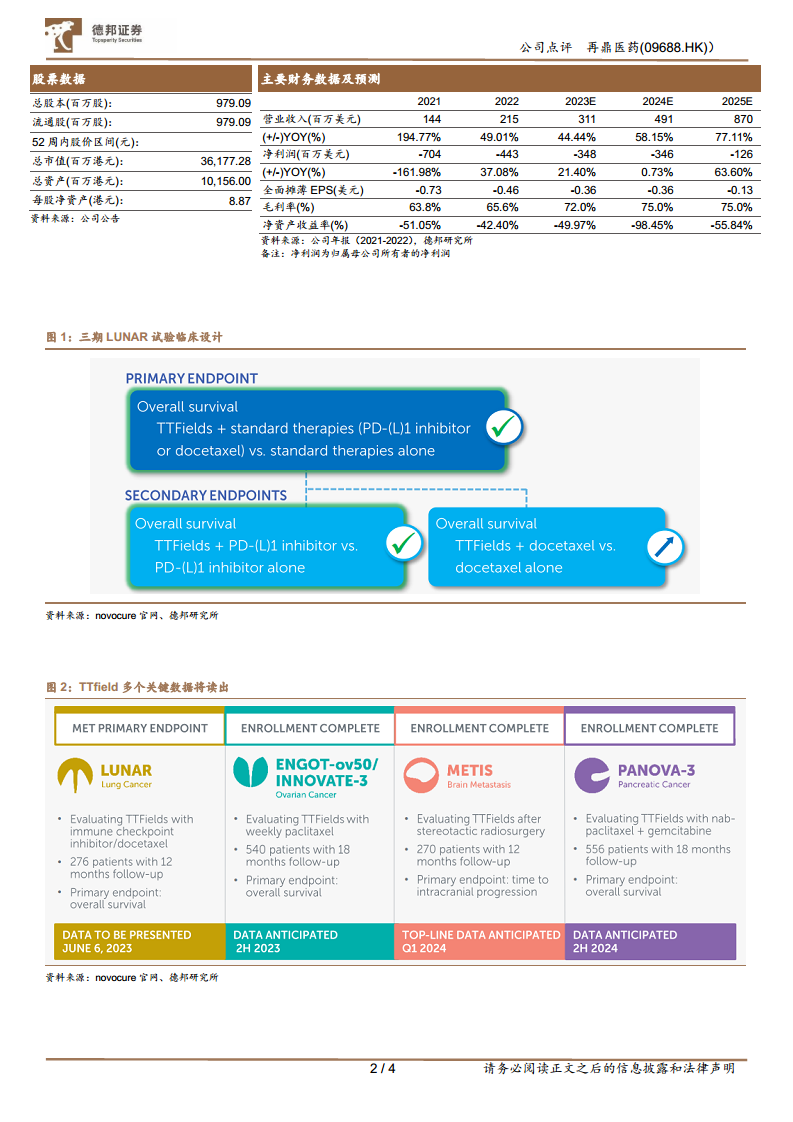
- LUNAR研究进展: 公司宣布肿瘤电场治疗(Optune)用于转移性非小细胞肺癌(NSCLC)的III期临床研究LUNAR的结果将于2023年6月初举行的美国临床肿瘤学会(ASCO)年会上首次公布。
- 积极结果: Novocure已于今年年初宣布LUNAR研究达到了主要终点,与单独使用标准药物治疗相比,在标准药物治疗中联合肿瘤电场治疗,总生存期在统计学上有显著且具有临床意义的改善。
- 报告形式: LUNAR研究数据将以完整口头报告(LBA)形式在北京时间6月7日凌晨在ASCO转移性非小细胞肺癌会议环节中汇报,预计将引起市场高度关注。
多个重磅产品里程碑将密集兑现
- 艾加莫德α (Efgartigimod alfa):
- 治疗全身型重症肌无力(gMG)注射液预计年内在大陆获批。
- 皮下注射剂型预计今年年中提交生物制品许可申请(BLA),美国有望在第二季度获批。
- 今年7月将公布慢性炎症性脱髓鞘性多发性神经病(CIDP)三期数据。
- 今年下半年将公布天疱疮和免疫性血小板减少症的三期数据。
- KarXT:
- 公司将于2023年年中在中国启动KarXT针对精神分裂症的桥接研究。
- 合作伙伴Karuna将于2023年第三季度向FDA提交新药申请(NDA)。
- SUL-DUR:
- 治疗鲍曼不动杆菌感染,新药申请(NDA)已于2月获受理。
- 擎乐、纽再乐:
- 已被纳入国家医保目录,2023年有望实现销量的显著增长。
- TF-ADC (TIVDAK®):
- 引进自Seagen,三期确证性研究目标患者入组已完成。
- 有望在2023年年底前公布关键性数据解读。
- 再鼎医药正在参与大中华区进行的扩展研究。
- KRAS抑制剂:
- 美国已获批。
- 合作伙伴计划年底向FDA递交用于三线以上结直肠癌(CRC)的补充新药申请(sNDA)。
- FGFR2b抑制剂:
- 2023年3月,再鼎医药获得三期研究FORTITUDE-101的临床试验申请批准,用于FGFR2b过度表达的胃癌一线治疗。
- CD20XCD3双抗:
- 合作伙伴再生元计划2023年下半年向FDA提交用于治疗复发/难治性弥漫性大B细胞淋巴瘤(R/R DLBCL)和复发/难治性滤泡性淋巴瘤(R/R FL)的生物制品许可申请(BLA)。
- ROS1 TKI:
- 公司2023年将向国家药品监督管理局(NMPA)提交用于治疗ROS1阳性晚期非小细胞肺癌(NSCLC)的新药申请(NDA)。
总结
业绩稳健增长,商业化能力凸显
再鼎医药在2023年第一季度实现了产品收入的显著增长,同比增长36.2%,并首次实现单季度商业化盈利,这表明公司在将创新产品转化为实际市场价值方面取得了重要进展。则乐和纽再乐等核心产品的强劲销售表现,以及总收入超越SG&A开支,共同印证了公司商业化战略的有效性及其日益增强的盈利能力。
创新管线驱动长期价值
公司未来发展前景广阔,主要得益于其丰富的创新产品管线和即将密集兑现的多个重磅里程碑。特别是肿瘤电场治疗LUNAR研究在ASCO大会上即将公布的积极数据,预计将成为短期内最重要的市场催化剂。此外,艾加莫德α、KarXT、SUL-DUR等多个产品的审批进展和临床数据公布,以及擎乐、纽再乐纳入医保,都将为公司带来持续的增长动力和长期价值。尽管存在临床失败、市场竞争和政策风险,但公司凭借其强大的研发实力和商业化执行力,有望在未来几年实现收入的持续高速增长。
-

涨价主线!关注活性染料、生物柴油等
-

医药行业周报:美股医疗AI龙头股价反弹,关注AI快速落地的企业
-

博瑞医药:专注代谢药物研发,管线新增口服BGM0504与Amylin类似物
-

医药行业周报:生命科学产业链,需求端逐步回暖,关税战进一步催化国产替代
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






最新报告
- 大化工周报:《双碳综合评价考核办法办法》发布,细分行业供需格局有望优化
- 医药行业周报:竞争内卷中寻找新增量
- 医药生物行业跟踪周报:中国创新药再次闪耀2026ASCO,LBA数量创历史新高,关注康方生物、科伦博泰等
- 2025年报&2026一季报点评:降本增效成果显著,非药盈利能力提升
- 25年国内业务收入增速快于国外业务,26Q1收入增速超26%
- 2025年报&2026一季报点评:净利率持续改善,看好2026重启扩张
- TYK2抑制剂具BIC潜力,在研管线&商业化双突破
- 26Q1经营势头良好,奠定全年向好基调
- 化工行业周报:国际油价上涨,氦气、制冷剂R22价格上涨
- 基础化工:政策定调绿色转型,节能降碳工作获新指引
对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送