-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用
立即咨询
产品矩阵


摩熵数科产品矩阵
查看详情
{{ item.category }}
{{ product.info.desc }}

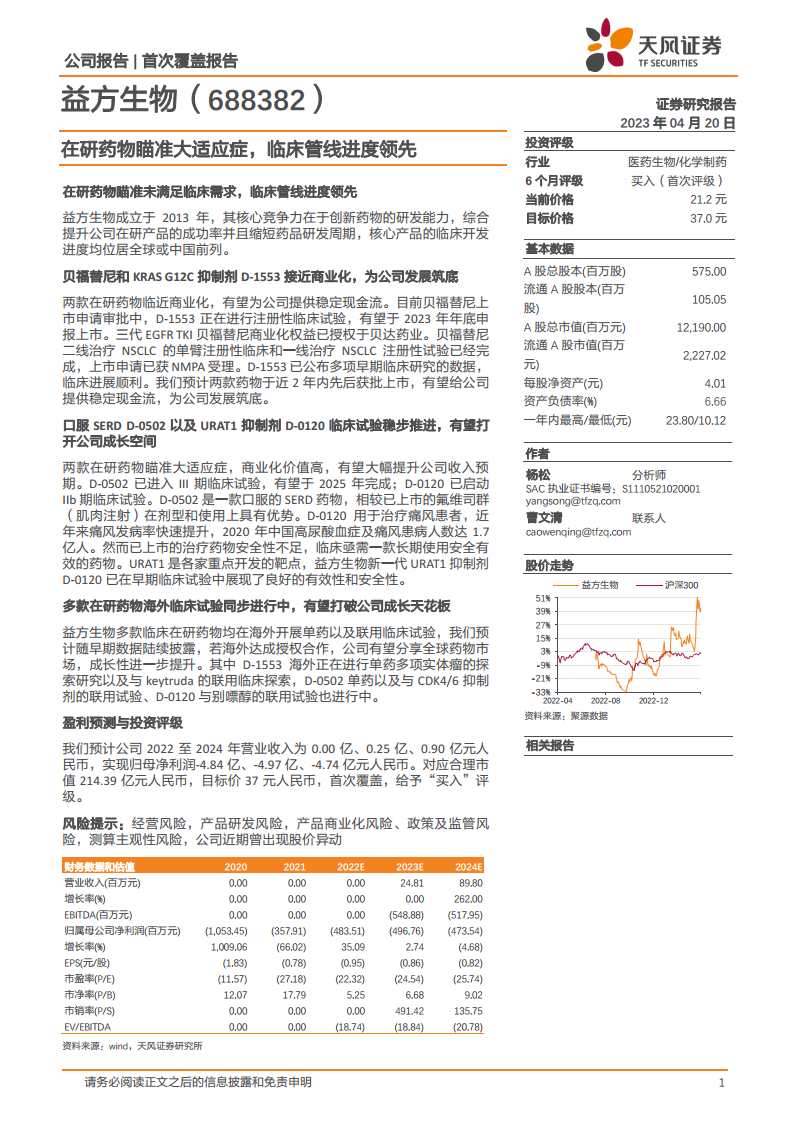
益方生物(688382):在研药物瞄准大适应症,临床管线进度领先
研报
益方生物(688382):在研药物瞄准大适应症,临床管线进度领先
中心思想
创新研发驱动,管线布局前瞻
益方生物作为一家成立于2013年的创新药企业,其核心竞争力在于卓越的创新药物研发能力,旨在提升在研产品的成功率并缩短研发周期。公司通过精准的药物靶点筛选、分子设计及临床方案开发,使其核心产品的临床开发进度位居全球或中国前列。
公司战略性地瞄准肿瘤和代谢性疾病等大适应症领域中未被满足的临床需求,构建了多条高价值的研发管线。其中,贝福替尼和KRAS G12C抑制剂D-1553已接近商业化,有望为公司提供稳定的现金流并奠定发展基础。
此外,口服SERD D-0502和URAT1抑制剂D-0120等创新药物的临床试验稳步推进,具有巨大的商业化潜力,有望显著拓宽公司的成长空间。公司积极开展多款在研药物的海外临床试验,旨在通过国际合作分享全球市场,进一步提升公司的成长性。
核心产品临近商业化,成长空间广阔
贝福替尼作为第三代EGFR TKI,其商业化权益已授权给经验丰富的贝达药业,目前上市申请正在审批中,一线治疗适应症也已提交NDA。其在NSCLC一线治疗中展现出最长的中位无进展生存期(mPFS),在二线治疗中也显示出显著的临床疗效,有望在广阔的EGFR TKI市场中占据重要地位。
KRAS G12C抑制剂D-1553作为国内首个自主研发并进入临床试验阶段的同类药物,已获得突破性疗法认定并进入注册性II期临床。其在早期临床中展现出良好的有效性和安全性,尤其在肝毒性方面优于已上市竞品,有望填补中国市场的空白。
口服SERD D-0502和URAT1抑制剂D-0120分别针对乳腺癌和痛风/高尿酸血症两大快速增长的适应症。D-0502的口服剂型相较注射剂型具有显著优势,且临床进度领先;D-0120则有望解决现有痛风治疗药物的安全性问题,两者均具备巨大的市场潜力。
主要内容
公司概况与研发实力
益方生物:研发立项精准,管线推进高效
益方生物科技(上海)股份有限公司(688382.SH)成立于2013年,专注于肿瘤、代谢性疾病等重大疾病领域的创新药研发。公司核心竞争力在于其创新药研发能力,通过精准靶点筛选、分子设计、药理及转化医学、化学合成工艺及制剂开发和临床方案设计等环节,提升在研产品成功率并缩短研发周期。
公司核心管理层拥有丰富的行业经验,平均超过20年的跨国药企(MNC)新药研发及团队管理经验,确保了研发团队的专业性和高效性。
截至2022年6月,公司产品管线中4个核心产品均已获批开展II期/III期临床试验,研发进度在全球或中国处于领先地位。公司研发费用持续处于较高水平,2018年至2021年分别为0.96亿元、1.33亿元、10.08亿元和3.15亿元,剔除股权激励费用后呈逐年增长趋势,显示出公司对研发的持续投入。
核心管线深度解析与市场潜力
核心临床管线:布局未满足临床需求,瞄准大适应症
贝福替尼:商业化权益授予贝达药业,有望成为三代EGFR格局中重要角色
市场广阔与竞争格局: 非小细胞肺癌(NSCLC)在中国新发患者人数持续增长,2020年达79万,其中EGFR敏感突变患者约26万。第三代EGFR TKI市场潜力巨大,已有奥希替尼、阿美替尼、伏美替尼等3款产品在中国上市。
临床进度与疗效: 贝福替尼一线治疗EGFR突变NSCLC的III期临床数据显示,中位无进展生存期(mPFS)达22.1个月,优于对照药埃克替尼的13.8个月。二线治疗NSCLC的II期临床数据显示,mPFS达16.6个月,中位缓解持续时间(mDOR)达18.0个月,均优于已上市的奥希替尼(mPFS 9.7个月,mDOR 9.9个月)、阿美替尼(mPFS 12.4个月,mDOR 15.1个月)和伏美替尼(mPFS 9.6个月,mDOR 8.3个月)(非头对头比较)。
商业化前景: 贝福替尼的中国权益已授权给拥有丰富EGFR TKI开发与商业化经验的贝达药业,有助于其快速上市放量。目前,二线治疗适应症的NDA已提交并稳步推进,一线治疗适应症的NDA也于2023年1月获NMPA受理。
KRAS G12C抑制剂D-1553:中国暂无同类药物获批,益方生物进度领先
市场需求: KRAS突变广泛分布于多种癌种,在中国11951例肿瘤样本中,16.6%的患者存在KRAS突变,其中G12C突变占14.5%,常见于肺癌(4.3%)、结直肠癌(2.5%)。全球仅安进Sotorasib和Mirati Adagrasib两款KRAS G12C抑制剂获批上市。
临床进度与疗效: D-1553是国内首个自主研发并进入临床试验阶段的KRAS G12C抑制剂,已于2022年6月获得CDE突破性疗法认定,并进入注册性II期临床试验。I期临床数据显示,在NSCLC患者中,客观缓解率(ORR)达40.5%,中位无进展生存期(PFS)达8.2个月,优于Sotorasib的6.8个月和Adagrasib的6.5个月(非头对头)。
安全性优势: D-1553在I期临床试验中耐受性良好,未观察到严重肝毒性。相比之下,已上市的Sotorasib和Adagrasib均显示出一定肝毒性,Adagrasib肝毒性发生率为37%(三级/四级7%),Sotorasib为1.7%(三级1.4%)。D-1553的良好安全性有望成为其市场竞争优势。
口服SERD D-0502:SERD药物具有优势,口服剂型有望带动销售放量
市场潜力: 乳腺癌已成为全球第一大癌症,中国每年新发患者约42万人。选择性雌激素受体降解剂(SERD)是HR阳性乳腺癌的重要治疗手段。目前全球唯一获批上市的SERD是阿斯利康的氟维司群(注射剂),其在中国终端市场销售额从2015年的3238万元增长至2020年的4.54亿元,年复合增长率达69.57%。口服SERD相较注射剂型具有显著的依从性和使用优势。
临床进度与疗效: D-0502已进入注册性III期临床试验,在国内研发进度领先。I期临床数据显示其生物利用度高,口服吸收好,并已观察到肿瘤部分缓解(PR)和完全缓解(CR)病例。
安全性优势: D-0502在临床研究中未出现同类在研产品(如赛诺菲Amcenestrant、罗氏Giredestrant)曾报告的视力障碍、心跳过缓或骨髓抑制等副作用,显示出良好的安全性。
URAT1抑制剂D-0120:已上市URAT1安全性较差,URAT1在研药物有望解决安全性问题
市场需求: 高尿酸血症及痛风患病人数快速增长,2020年中国患病人数达1.7亿,预计2030年将达2.4亿。现有治疗药物如苯溴马隆存在肝脏毒性风险,非布司他存在心血管安全性问题,市场亟需长期安全有效的治疗药物。
临床进度与疗效: D-0120已在中国和美国进行多个临床试验,中国试验已进入IIb期。IIa期临床数据显示,D-0120在目标剂量下患者血尿酸达标率达80%,高于国内部分竞品(如恒瑞SHR4640 5mg组32.5%,海创HP501 40mg组32%)。
安全性优势: D-0120在I期和IIa期临床试验中均显示出良好的安全性和耐受性,未报告死亡或严重不良事件,不良事件多为1、2级,有望解决现有药物的安全性痛点。
多款在研药物海外临床试验同步进行中,有望打破公司成长天花板
益方生物的D-1553、D-0502和D-0120均在海外开展国际多中心临床试验,探索单药及联用方案。若未来达成海外授权合作,公司有望分享全球药物市场,进一步提升成长性。
盈利预测与估值
预计公司2022年至2024年营业收入分别为0.00亿、0.25亿、0.90亿元人民币,主要由贝福替尼的销售分成贡献(假设分成比例15%)。
同期归母净利润预计为-4.84亿、-4.97亿、-4.74亿元人民币,主要由于高额的研发投入(2022-2024年研发费用预计分别为4.80亿、5.25亿、5.51亿元)。
采用EVA估值法,给予2%永续增长率和10.5%的加权平均资本成本(WACC),公司合理估值214.39亿元人民币,对应目标价37元人民币,首次覆盖给予“买入”评级。
风险因素
公司面临经营风险(盈利不及预期、流动性、合作方商业化不确定性、商业化团队组建不确定性、退市风险)、产品研发风险(研发进程及结果不确定性)、产品商业化风险(上市不确定性、市场竞争激烈及销售不及预期、上市后商业化不确定性)、政策及监管风险(差异化监管政策)以及测算主观性风险。
总结
益方生物凭借其强大的创新研发能力和经验丰富的管理团队,已成功构建了聚焦肿瘤和代谢性疾病的多元化高价值研发管线。
公司核心产品贝福替尼和KRAS G12C抑制剂D-1553已进入商业化冲刺阶段,其中贝福替尼已授权贝达药业,D-1553则有望填补国内市场空白,两者均展现出优异的临床数据和市场潜力,将为公司带来早期收入。
D-0502(口服SERD)和D-0120(URAT1抑制剂)等处于临床中后期的创新药物,针对乳腺癌和痛风等大适应症,有望凭借剂型优势、更优的疗效和安全性,解决现有治疗方案的痛点,打开公司长期成长空间。
公司积极推进多款药物的国际多中心临床试验,为未来全球商业化合作奠定基础,有望分享更广阔的国际市场。尽管当前公司处于高研发投入阶段,尚未实现盈利,但其领先的临床管线进度和巨大的市场潜力,支撑了其长期投资价值,首次覆盖给予“买入”评级。
报告专题:
-
下载次数:
254 次
-
发布机构:
天风证券
-
发布日期:
2023-04-20
-
页数:
34页
下载全文
定制咨询
AI精读报告
中心思想
创新研发驱动,管线布局前瞻
- 益方生物作为一家成立于2013年的创新药企业,其核心竞争力在于卓越的创新药物研发能力,旨在提升在研产品的成功率并缩短研发周期。公司通过精准的药物靶点筛选、分子设计及临床方案开发,使其核心产品的临床开发进度位居全球或中国前列。
- 公司战略性地瞄准肿瘤和代谢性疾病等大适应症领域中未被满足的临床需求,构建了多条高价值的研发管线。其中,贝福替尼和KRAS G12C抑制剂D-1553已接近商业化,有望为公司提供稳定的现金流并奠定发展基础。
- 此外,口服SERD D-0502和URAT1抑制剂D-0120等创新药物的临床试验稳步推进,具有巨大的商业化潜力,有望显著拓宽公司的成长空间。公司积极开展多款在研药物的海外临床试验,旨在通过国际合作分享全球市场,进一步提升公司的成长性。
核心产品临近商业化,成长空间广阔
- 贝福替尼作为第三代EGFR TKI,其商业化权益已授权给经验丰富的贝达药业,目前上市申请正在审批中,一线治疗适应症也已提交NDA。其在NSCLC一线治疗中展现出最长的中位无进展生存期(mPFS),在二线治疗中也显示出显著的临床疗效,有望在广阔的EGFR TKI市场中占据重要地位。
- KRAS G12C抑制剂D-1553作为国内首个自主研发并进入临床试验阶段的同类药物,已获得突破性疗法认定并进入注册性II期临床。其在早期临床中展现出良好的有效性和安全性,尤其在肝毒性方面优于已上市竞品,有望填补中国市场的空白。
- 口服SERD D-0502和URAT1抑制剂D-0120分别针对乳腺癌和痛风/高尿酸血症两大快速增长的适应症。D-0502的口服剂型相较注射剂型具有显著优势,且临床进度领先;D-0120则有望解决现有痛风治疗药物的安全性问题,两者均具备巨大的市场潜力。
主要内容
公司概况与研发实力
- 益方生物:研发立项精准,管线推进高效
- 益方生物科技(上海)股份有限公司(688382.SH)成立于2013年,专注于肿瘤、代谢性疾病等重大疾病领域的创新药研发。公司核心竞争力在于其创新药研发能力,通过精准靶点筛选、分子设计、药理及转化医学、化学合成工艺及制剂开发和临床方案设计等环节,提升在研产品成功率并缩短研发周期。
- 公司核心管理层拥有丰富的行业经验,平均超过20年的跨国药企(MNC)新药研发及团队管理经验,确保了研发团队的专业性和高效性。
- 截至2022年6月,公司产品管线中4个核心产品均已获批开展II期/III期临床试验,研发进度在全球或中国处于领先地位。公司研发费用持续处于较高水平,2018年至2021年分别为0.96亿元、1.33亿元、10.08亿元和3.15亿元,剔除股权激励费用后呈逐年增长趋势,显示出公司对研发的持续投入。
核心管线深度解析与市场潜力
核心临床管线:布局未满足临床需求,瞄准大适应症
- 贝福替尼:商业化权益授予贝达药业,有望成为三代EGFR格局中重要角色
- 市场广阔与竞争格局: 非小细胞肺癌(NSCLC)在中国新发患者人数持续增长,2020年达79万,其中EGFR敏感突变患者约26万。第三代EGFR TKI市场潜力巨大,已有奥希替尼、阿美替尼、伏美替尼等3款产品在中国上市。
- 临床进度与疗效: 贝福替尼一线治疗EGFR突变NSCLC的III期临床数据显示,中位无进展生存期(mPFS)达22.1个月,优于对照药埃克替尼的13.8个月。二线治疗NSCLC的II期临床数据显示,mPFS达16.6个月,中位缓解持续时间(mDOR)达18.0个月,均优于已上市的奥希替尼(mPFS 9.7个月,mDOR 9.9个月)、阿美替尼(mPFS 12.4个月,mDOR 15.1个月)和伏美替尼(mPFS 9.6个月,mDOR 8.3个月)(非头对头比较)。
- 商业化前景: 贝福替尼的中国权益已授权给拥有丰富EGFR TKI开发与商业化经验的贝达药业,有助于其快速上市放量。目前,二线治疗适应症的NDA已提交并稳步推进,一线治疗适应症的NDA也于2023年1月获NMPA受理。
- KRAS G12C抑制剂D-1553:中国暂无同类药物获批,益方生物进度领先
- 市场需求: KRAS突变广泛分布于多种癌种,在中国11951例肿瘤样本中,16.6%的患者存在KRAS突变,其中G12C突变占14.5%,常见于肺癌(4.3%)、结直肠癌(2.5%)。全球仅安进Sotorasib和Mirati Adagrasib两款KRAS G12C抑制剂获批上市。
- 临床进度与疗效: D-1553是国内首个自主研发并进入临床试验阶段的KRAS G12C抑制剂,已于2022年6月获得CDE突破性疗法认定,并进入注册性II期临床试验。I期临床数据显示,在NSCLC患者中,客观缓解率(ORR)达40.5%,中位无进展生存期(PFS)达8.2个月,优于Sotorasib的6.8个月和Adagrasib的6.5个月(非头对头)。
- 安全性优势: D-1553在I期临床试验中耐受性良好,未观察到严重肝毒性。相比之下,已上市的Sotorasib和Adagrasib均显示出一定肝毒性,Adagrasib肝毒性发生率为37%(三级/四级7%),Sotorasib为1.7%(三级1.4%)。D-1553的良好安全性有望成为其市场竞争优势。
- 口服SERD D-0502:SERD药物具有优势,口服剂型有望带动销售放量
- 市场潜力: 乳腺癌已成为全球第一大癌症,中国每年新发患者约42万人。选择性雌激素受体降解剂(SERD)是HR阳性乳腺癌的重要治疗手段。目前全球唯一获批上市的SERD是阿斯利康的氟维司群(注射剂),其在中国终端市场销售额从2015年的3238万元增长至2020年的4.54亿元,年复合增长率达69.57%。口服SERD相较注射剂型具有显著的依从性和使用优势。
- 临床进度与疗效: D-0502已进入注册性III期临床试验,在国内研发进度领先。I期临床数据显示其生物利用度高,口服吸收好,并已观察到肿瘤部分缓解(PR)和完全缓解(CR)病例。
- 安全性优势: D-0502在临床研究中未出现同类在研产品(如赛诺菲Amcenestrant、罗氏Giredestrant)曾报告的视力障碍、心跳过缓或骨髓抑制等副作用,显示出良好的安全性。
- URAT1抑制剂D-0120:已上市URAT1安全性较差,URAT1在研药物有望解决安全性问题
- 市场需求: 高尿酸血症及痛风患病人数快速增长,2020年中国患病人数达1.7亿,预计2030年将达2.4亿。现有治疗药物如苯溴马隆存在肝脏毒性风险,非布司他存在心血管安全性问题,市场亟需长期安全有效的治疗药物。
- 临床进度与疗效: D-0120已在中国和美国进行多个临床试验,中国试验已进入IIb期。IIa期临床数据显示,D-0120在目标剂量下患者血尿酸达标率达80%,高于国内部分竞品(如恒瑞SHR4640 5mg组32.5%,海创HP501 40mg组32%)。
- 安全性优势: D-0120在I期和IIa期临床试验中均显示出良好的安全性和耐受性,未报告死亡或严重不良事件,不良事件多为1、2级,有望解决现有药物的安全性痛点。
- 多款在研药物海外临床试验同步进行中,有望打破公司成长天花板
- 益方生物的D-1553、D-0502和D-0120均在海外开展国际多中心临床试验,探索单药及联用方案。若未来达成海外授权合作,公司有望分享全球药物市场,进一步提升成长性。
- 贝福替尼:商业化权益授予贝达药业,有望成为三代EGFR格局中重要角色
盈利预测与估值
- 预计公司2022年至2024年营业收入分别为0.00亿、0.25亿、0.90亿元人民币,主要由贝福替尼的销售分成贡献(假设分成比例15%)。
- 同期归母净利润预计为-4.84亿、-4.97亿、-4.74亿元人民币,主要由于高额的研发投入(2022-2024年研发费用预计分别为4.80亿、5.25亿、5.51亿元)。
- 采用EVA估值法,给予2%永续增长率和10.5%的加权平均资本成本(WACC),公司合理估值214.39亿元人民币,对应目标价37元人民币,首次覆盖给予“买入”评级。
风险因素
- 公司面临经营风险(盈利不及预期、流动性、合作方商业化不确定性、商业化团队组建不确定性、退市风险)、产品研发风险(研发进程及结果不确定性)、产品商业化风险(上市不确定性、市场竞争激烈及销售不及预期、上市后商业化不确定性)、政策及监管风险(差异化监管政策)以及测算主观性风险。
总结
- 益方生物凭借其强大的创新研发能力和经验丰富的管理团队,已成功构建了聚焦肿瘤和代谢性疾病的多元化高价值研发管线。
- 公司核心产品贝福替尼和KRAS G12C抑制剂D-1553已进入商业化冲刺阶段,其中贝福替尼已授权贝达药业,D-1553则有望填补国内市场空白,两者均展现出优异的临床数据和市场潜力,将为公司带来早期收入。
- D-0502(口服SERD)和D-0120(URAT1抑制剂)等处于临床中后期的创新药物,针对乳腺癌和痛风等大适应症,有望凭借剂型优势、更优的疗效和安全性,解决现有治疗方案的痛点,打开公司长期成长空间。
- 公司积极推进多款药物的国际多中心临床试验,为未来全球商业化合作奠定基础,有望分享更广阔的国际市场。尽管当前公司处于高研发投入阶段,尚未实现盈利,但其领先的临床管线进度和巨大的市场潜力,支撑了其长期投资价值,首次覆盖给予“买入”评级。
如果您有其他需求,请点击
定制服务咨询
天风证券最新报告
-

迪瑞医疗(300396):国内短期承压,海外市场呈现良好增长态势
-

特步国际(01368):索康尼延续高质量成长
-

新天药业(002873):业绩短期承压,增资汇伦医药强化创新研发
-

金达威(002626):再论辅酶Q10全球龙头的大健康全球化之路
关于摩熵咨询
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案
1W+
医药行业研究报告
200+
真实项目案例
1300+
业内高端专家资源

市场洞察与营销赋能
分析市场现状,洞察行业趋势,依托数据分析和深度研究,辅助商业决策。

立项评估及管线规划
提供疾病领域品种调研、专家访谈、品种立项、项目交易整套服务。

产业规划及研究服务
以数据为基础,为组织、园区、企业提供科学的决策依据和趋势线索。

多渠道数据分析及定制服务
帮助客户深入了解目标领域和市场情况,发现潜在机会,优化企业决策。

投资决策与交易估值
依托全球医药全产业链数据库与顶级投行级分析模型,为并购、融资、IPO提供全周期决策支持。

立即定制
对不起!您还未登录!请登陆后查看!
立即登录
您今日剩余【10】次下载额度,确定继续吗?
取消
确定
确定
获取定制报告
请填写你的需求,我们将尽快与您取得联系
姓名
{{nameTip}}
单位
{{companyTip}}
电话
{{telTip}}
验证码
{{sms_codeTip}}
{{ setTime ? `${second}s` : '获取验证码' }}
邮箱
{{emailTip}}
需求描述
{{descriptionTip}}
提交
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送