-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

创新研发聚焦痛风领域,有望迎来收获期
创新研发聚焦痛风领域,有望迎来收获期
-
下载次数:
2801 次
-
发布机构:
天风证券股份有限公司
-
发布日期:
2025-04-11
-
页数:
31页
一品红(300723)
一品红:专注儿童药与慢病药物,研发驱动不断丰富产品矩阵
一品红是一家聚焦于儿童药、慢病药领域的创新型生物医药企业。公司着力打造儿童药制剂创新研发平台,并建有慢病创新药技术中心、口服缓控释制剂研究实验室和生产技术转化中心,具备创新药全流程及多种技术类型高端口服缓控释制剂的自主研发及生产能力。公司现有26个儿童药注册批件和66个慢病药注册批件,产品结构丰富,涵盖多个疾病治疗领域。目前具有在研儿童专用药25项,在研慢病药包括全球创新药AR882等项目13个。
痛风:现有药物存在一定局限性,广阔市场需要更优药物
痛风是一种单钠尿酸盐沉积在关节所致的晶体相关性关节病,其与嘌呤代谢紊乱和/或尿酸排泄减少所致的高尿酸血症直接相关。预计2025年全球高尿酸血症患者将达到11.8亿,并将于2030年达到14.2亿;预计2025年中国高尿酸血症患者将达到2.1亿,并将于2030年达到2.4亿。痛风患者基数庞大,但现有痛风治疗药物存在一定的局限性。例如传统的降尿酸药物别嘌醇和非布司他,别嘌醇需关注HLA-B*5801基因检测以减少不良反应风险,非布司他则需警惕潜在心血管事件,其也因此被FDA黑框警告。因此现有药物无法充分满足痛风患者的临床需求,痛风患者需要新型的、疗效和安全性更好的药物。
AR882:安全性+降尿酸疗效优势,有望成为best in class
AR882是一品红与美国Arthrosi公司合作研发的1类创新药,用于治疗痛风,其通过抑制尿酸转运蛋白URAT1使尿液尿酸盐排泄正常化,从而降低血清尿酸(sUA)水平,2024年8月AR882获得美国FDA快速通道资格,目前AR882正按计划推进全球Ⅲ期临床试验。其国际临床II期试验结果显示,安全性方面,AR882表现出良好的耐受性,无任何重度不良反应发生;有效性方面,AR882在单药治疗中,AR882表现出比别嘌呤醇(↓35%)或非布司他(↓39%)更好的血清尿酸降低效果(↓53%),并且AR882在治疗6周时就体现出了卓越的有效性,75mgAR882相对非布司他已体现出了优效(P<0.001)。AR882不仅优于已有的降尿酸药物,研发进度也已在全球在研痛风创新药中领先,其III期入组迅速,全球III期临床试验有望2026年上半年完成。
盈利预测与估值:我们预计公司2024-2026年营业收入分别为16.28、20.27、23.52亿元,归母净利润分别为-4.96、1.91、3.30亿元。我们看好公司进入加速发展阶段,给予公司2025年8倍PS,对应目标价35.88元,首次覆盖,给予“买入”评级。
风险提示:药品研发风险,药品价格下降风险,产品质量风险,行业政策风险,技术人员流失风险,原材料价格波动风险,股价波动的风险。
中心思想
创新研发驱动与痛风领域突破
一品红药业集团股份有限公司(300723)作为一家专注于儿童药和慢病药领域的创新型生物医药企业,正通过其强大的研发实力和前瞻性战略布局,在痛风治疗领域取得突破性进展。公司与美国Arthrosi公司合作研发的1类创新药AR882,作为新一代URAT1抑制剂,在国际和国内临床试验中展现出卓越的降尿酸疗效和安全性优势,有望成为“同类最佳”(best in class)药物,满足现有痛风治疗药物未被满足的巨大临床需求。AR882的快速推进及其在全球痛风创新药中的领先地位,预示着公司未来业绩增长的核心驱动力。
儿童慢病市场深耕与AI赋能增长
尽管公司短期内面临营收压力,但其在儿童药和慢病药传统业务领域的深耕,以及通过AI医疗技术赋能创新研发的战略,为长期发展奠定了坚实基础。公司拥有丰富的产品管线和强大的研发平台,尤其在儿童用药方面,通过剂型创新和循证医学研究,不断提升产品竞争力。同时,通过投资AI新药研发公司阿尔法分子科技,一品红积极拥抱前沿科技,探索生物计算在药物发现中的应用,为公司未来多元化增长和持续创新注入新动能。
主要内容
公司概况、战略布局与财务表现
- 公司简介与业务聚焦: 一品红药业集团股份有限公司成立于2002年,2017年上市,业务覆盖医药全产业链,以医药制造为主导。公司总部位于广州国际生物岛,拥有5万多平方米办公总部、6万多平方米创新研发基地、22万平方米符合欧盟和FDA标准的数字化智能智造基地及110亩创新原料药基地。公司拥有一支由全球资深首席科学家领衔的400余人创新研发团队,2021至2023年研发投入约13亿元,年研发投入占营收约10%。目前拥有193个药品注册批件,连续4年每年新增注册批件超过10个。公司聚焦儿童药和慢病药领域,产品涵盖化学药(含原料药和制剂)、特色中成药、生物疫苗等。现有26个儿童药注册批件和66个慢病药注册批件,在研儿童专用药25项,在研慢病药13个,其中包括全球创新药AR882。
- AR882的深度绑定: 公司参股美国Arthrosi公司22.52%股权,并通过合资公司广州瑞安博获得AR882在中国区域(含港澳台)的研发、生产及销售权益,实现了与新一代URAT1抑制剂AR882的深度绑定。AR882已于2024年8月获得美国FDA快速通道资格,全球Ⅲ期临床试验正按计划推进。
- 营业收入短期承压与复苏展望: 2024年前三季度,公司实现营业收入12.40亿元,同比下降32.98%;归母净利润为-2.47亿元。2024年业绩预告预计归母净利润为-4.72亿元至-6.80亿元。业绩下滑主要受行业政策、市场环境变化、联瑞生物医药智能制造基地爬坡阶段、研发投入加大和非经常性损益等因素影响。尽管短期承压,但随着新药研发的推进和传统业务的调整,公司有望迎来复苏。
- 股权结构与员工激励: 公司实际控制人为李捍雄先生和吴美容女士,李捍雄先生合计持有公司35.97%股份。公司实施了充分的员工股权激励计划,2025年股票期权激励计划覆盖353名核心骨干员工。考核年度为2025-2027年,业绩考核目标包括利润增长率(以2023年为基准年,2025年不低于32%,2026年不低于52%,2027年不低于75%)、新获批创新药IND数量或药品注册批件数量(每年不少于10个),旨在将股东、公司和核心团队利益相结合,促进公司长期发展。
痛风市场机遇、AR882核心优势及多元业务协同
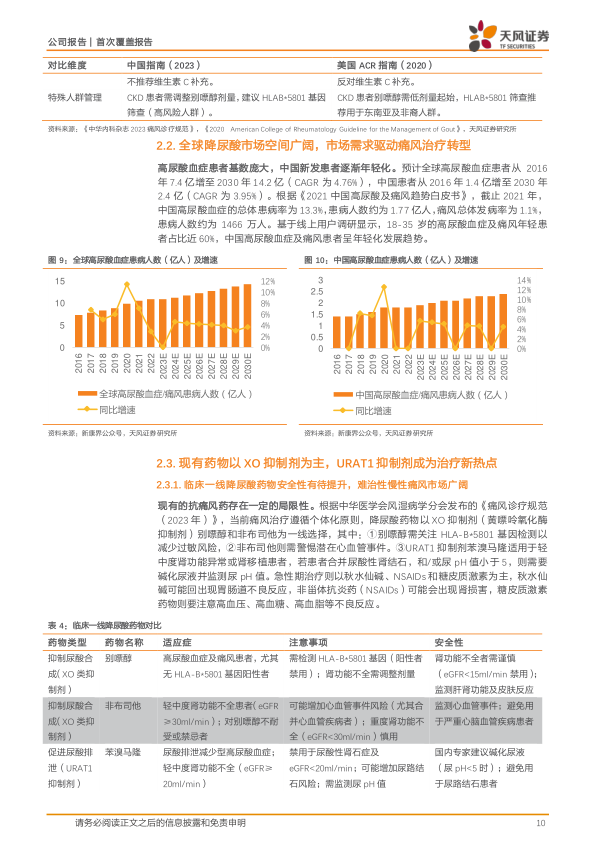
- 痛风行业扩容与未满足需求: 痛风是一种与高尿酸血症直接相关的晶体沉积性关节病。预计全球高尿酸血症患者将从2025年的11.8亿增至2030年的14.2亿;中国患者将从2025年的2.1亿增至2030年的2.4亿。中国高尿酸血症总体患病率为13.3%(约1.77亿人),痛风总体发病率为1.1%(约1466万人),且患者呈年轻化趋势(18-35岁占比近60%)。现有痛风治疗药物存在局限性,如别嘌醇需关注HLA-B*5801基因检测,非布司他有潜在心血管事件风险(FDA黑框警告),苯溴马隆有肝毒性风险,普瑞凯希(Krystexxa)虽用于难治性痛风但有过敏风险且未在中国大陆获批。这些局限性表明市场对新型、疗效和安全性更好的药物存在巨大需求。
- URAT1抑制剂成为治疗新热点: 中美痛风治疗指南均强调降尿酸治疗,目标血尿酸(sUA)<6mg/dL。现有药物以黄嘌呤氧化酶(XO)抑制剂为主,但URAT1作为尿酸代谢的关键靶点,因其对尿酸的高亲和力和转运效率,成为新的突破方向。全球范围内有超过30个URAT1靶点在研项目,其中持田制药的多替诺雷已上市,恒瑞医药的Ruzinurad处于申请上市阶段,一品红的AR882、江泰制药的Epaminurad及上海璎黎的YL-90148等处于临床III期。
- AR882的显著优势与快速进展:
- II期临床数据优异: AR882在国际II期临床试验(NCT05119686)中表现出色。在140名痛风患者中,平均基线sUA为8.6mg/dL。12周治疗后,75mg剂量组中位sUA降至3.5mg/dL(降低约304μmol/L),50mg剂量组降至5.0mg/dL(降低约215μmol/L)。75mg剂量组患者sUA达标率(<6mg/dL)高达89%,<5mg/dL达82%,<4mg/dL达63%。
- 对比现有药物更优: 在单药治疗中,AR882(↓53%)表现出比别嘌呤醇(↓35%)或非布司他(↓39%)更好的sUA降低效果。AR882与别嘌呤醇联合治疗使sUA降低66%,与非布司他联合治疗使sUA降低71%。AR882在治疗6周时就体现出卓越有效性,75mg剂量相对非布司他已体现优效(P<0.001)。
- 痛风石治疗效果显著: 在NCT05253833试验中,AR882 75mg组在6个月时有29%的患者痛风石完全消除,在6-12个月的延长期试验中,AR882 75mg组和AR882 75mg+别嘌醇组分别有50.0%和36.4%的患者痛风结石完全溶解,痛风晶体体积持续减少。
- 安全性良好: AR882在所有临床试验中均表现出良好的耐受性,无任何重度不良反应发生,轻中度不良反应包括腹泻、头痛、上呼吸道感染,且不影响患者合并症的病情管理。
- III期临床进展迅速: AR882已获得美国FDA快速通道资格。全球关键性III期试验REDUCE2(NCT06439602)已提前四个月完成全部750名受试者入组,预计2026年下半年完成。同期,国内III期临床试验(CTR20241026)也于2025年3月完成首例患者入组,由北京协和医院风湿免疫科牵头,旨在对比非布司他片评估AR882的有效性和安全性。AR882的研发进度在全球在研痛风创新药中处于领先地位。
- **传统业务稳健
-

天风医药细分领域分析与展望(2025H1):体外诊断行业及个股2025半年度回顾与展望
-

国内短期承压,海外市场呈现良好增长态势
-

基础化工行业研究周报:国家发改委,支持石化化工行业节能降碳改造,煤化工项目低碳化改造,双氧水、硫酸铵价格上涨
-

化工行业运行指标跟踪:2025年8-9月数据
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






最新报告
- 医药生物行业周报(26年第23周):ASCO会议顺利闭幕,关注具备高质量创新能力的公司
- 基础化工行业研究:R22、煤焦油等涨幅居前,建议关注进口替代、纯内需、高股息等方向
- 医疗器械行业2026年中期策略:紧扣出海创新,掘金器械复苏
- AI系列深度(十一):高频高速覆铜板有望拉动高性能硅微粉需求持续增长
- 基础化工行业周报:硫磺价格持续上涨,巨化股份超纯PFA量产
- 2025年化学制药行业经济运行报告
- 2025中医药市场研究报告
- EGFR×HER3双抗ADC iza-bren硕果频出,多管线驱动成长
- 服务价格落地,一次性高值耗材推广加速
- 北交所信息更新:NL003塞多明基注射液获批上市,填补我国CLTI临床对因治疗空白
对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送