-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

医药生物行业重大事件快评:CDE发布《人乳头瘤病毒疫苗临床试验技术指导原则(征求意见稿)》,相关产品上市有望提速
医药生物行业重大事件快评:CDE发布《人乳头瘤病毒疫苗临床试验技术指导原则(征求意见稿)》,相关产品上市有望提速
-
下载次数:
126 次
-
发布机构:
国信证券股份有限公司
-
发布日期:
2022-11-01
-
页数:
6页
事项:
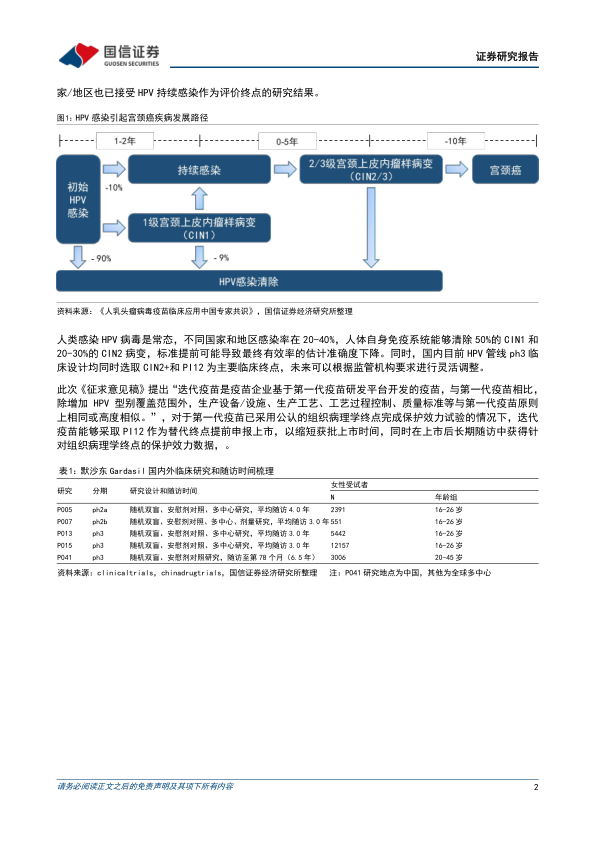
2022年10月26日,国家药品监督管理局药品审评中心发布《人乳头瘤病毒疫苗临床试验技术指导原则(征求意见稿)》,关于确证性临床试验的临床设计和有效性评价部分,《征求意见稿》提出“考虑到新增型别所致子宫颈癌等疾病的发病率可能进一步降低,以及PI是导致组织病理学改变的发病和进展机制。因此,若上一代疫苗采用公认的组织病理学终点完成保护效力试验,经评估符合要求的迭代疫苗可接受以病毒学终点12个月PI(PI12)提前申报上市,以缩短获批上市时间。此时,临床试验方案需严格制定PI12的定义,包括但不限于采样时间间隔、样本来源、检测方法、是否存在访问缺失等可能影响试验质量的因素。一般情况下,PI12定义为同一解剖部位间隔6个月或更长时间的连续3次及以上检出相同型别HPV核酸阳性。”以及“以PI12提前申报上市时,说明书【作用与用途】将注明共有型别在上一代疫苗中获批的适应症,并提示针对新增型别的CIN2+等组织病理学终点保护效力尚在研究中。上市后应继续随访以获得针对组织病理学终点的保护效力数据,并及时提交终版研究报告以充分证实其有效性和安全性。”
国信医药观点:关于HPV疫苗的临床终点选择之辩已持续多年,目前已上市的HPV疫苗上市前临床研究均使用高级别宫颈上皮内瘤变/CIN作为主要临床终点,但2014年和2016年WHO/IARC先后通过专家小组报告和立场文件等方式建议使用持续感染作为替代终点。此次《征求意见稿》提出“迭代疫苗是疫苗企业基于第一代疫苗研发平台开发的疫苗,与第一代疫苗相比,除增加HPV型别覆盖范围外,生产设备/设施、生产工艺、工艺过程控制、质量标准等与第一代疫苗原则上相同或高度相似”,对于第一代疫苗已采用公认的组织病理学终点完成保护效力试验的情况下,迭代疫苗能够采取PI12作为替代终点提前申报上市,以缩短获批上市时间,同时在上市后长期随访中获得针对组织病理学终点的保护效力数据,兼顾产品临床审批效率以及安全性&有效性。国产9价HPV目前有多家企业推进至ph3临床,其中万泰生物、瑞科生物、上海博唯和康乐卫士采用CIN2+和PI12双终点,建议关注具备迭代疫苗产品的相关企业。
风险提示:产品销售不及预期;国内竞争加剧导致产品价格大幅下降;产能项目建设不达预期;研发管线进展不达预期或失败;与合作方无法续签或协议条款内容不达预期;国家政策或疫苗推荐免疫程序发生重大变化等风险。
行业重大事件快评:CDE发布HPV疫苗临床试验技术指导原则(征求意见稿)
中心思想
- CDE发布HPV疫苗临床试验技术指导原则(征求意见稿),为迭代HPV疫苗上市提速提供政策支持。 意见稿允许迭代疫苗以持续感染(PI12)作为替代终点提前申报上市,同时在上市后长期随访中获得针对组织病理学终点的保护效力数据,兼顾了产品临床审批效率和安全性、有效性。
- 国产HPV疫苗研发加速,多家企业进入临床III期。 报告指出,多家国产9价HPV疫苗已推进至临床III期,其中部分企业采用CIN2+和PI12双终点,为市场带来新的增长潜力。
- HPV疫苗市场前景广阔,建议关注具备迭代疫苗产品的相关企业。 报告分析了HPV疫苗市场的积极因素,并建议关注具备迭代疫苗产品的相关企业,以把握市场机遇。
主要内容
## HPV疫苗临床试验技术指导原则解读
- 临床终点选择: 报告分析了HPV疫苗临床试验中关于临床终点的争议,即癌前病变(CIN)与持续感染(PI)的选择。目前已上市的HPV疫苗主要采用高级别宫颈上皮内瘤变/CIN作为主要临床终点。WHO/IARC曾建议使用持续感染作为替代终点。
- 迭代疫苗的定义与优势: 《征求意见稿》明确了迭代疫苗的定义,即基于第一代疫苗研发平台开发的疫苗,在增加HPV型别覆盖范围的同时,生产设备、工艺、质量标准等与第一代疫苗原则上相同或高度相似。对于第一代疫苗已采用公认的组织病理学终点完成保护效力试验的情况下,迭代疫苗能够采取PI12作为替代终点提前申报上市,从而缩短获批上市时间。
- 上市后随访要求: 尽管迭代疫苗可以PI12提前申报上市,但上市后仍需进行长期随访,以获得针对组织病理学终点的保护效力数据,并及时提交终版研究报告。
## 国内HPV疫苗研发进展
- 国产9价HPV疫苗研发格局: 报告指出,目前国内有多家企业推进9价HPV疫苗至临床III期。
- 临床终点选择: 其中,万泰生物、瑞科生物、上海博唯和康乐卫士采用CIN2+和PI12双终点,沃森生物Ph3临床采用中和抗体滴度和阳转率的血清学终点。
- 其他HPV疫苗研发管线: 报告还列举了其他不同类型的HPV疫苗研发管线,包括3价、4价和11价HPV疫苗,以及14价HPV疫苗。
## 投资建议与风险提示
- 市场前景: 报告认为,国内HPV疫苗产品推广充分,消费者接种意愿高,市场空间广阔。
- 竞争格局: 短期内,2进口+2国产的格局稳定。默沙东/智飞生物代理协议采购额维持高增速、万泰生物产能逐步释放,有望快速抢占各自目标市场份额。
- 投资建议: 建议关注具备迭代疫苗产品的相关企业。
- 风险提示: 报告提示了产品销售不及预期、国内竞争加剧、产能项目建设不达预期、研发管线进展不达预期、合作方无法续签或协议条款内容不达预期、疫苗推荐免疫程序发生重大变化等风险。
总结
本报告重点分析了CDE发布的《人乳头瘤病毒疫苗临床试验技术指导原则(征求意见稿)》对HPV疫苗行业的影响。该指导原则为迭代HPV疫苗上市提速提供了政策支持,推动了国产HPV疫苗的研发进程。报告指出,国内HPV疫苗市场前景广阔,建议关注具备迭代疫苗产品的相关企业,并提示了相关风险。
-

医药生物行业周报(26年第18周):26Q1公募基金医药持仓分析
-

26Q1业绩端改善显著,经营全面变革开启发展新篇章
-

医药行业快评:ASCO年会标题发布,多个国产创新药研究成果入选口头报告
-

2025年年报点评:在手订单充沛,新兴业务强势增长
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送