-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

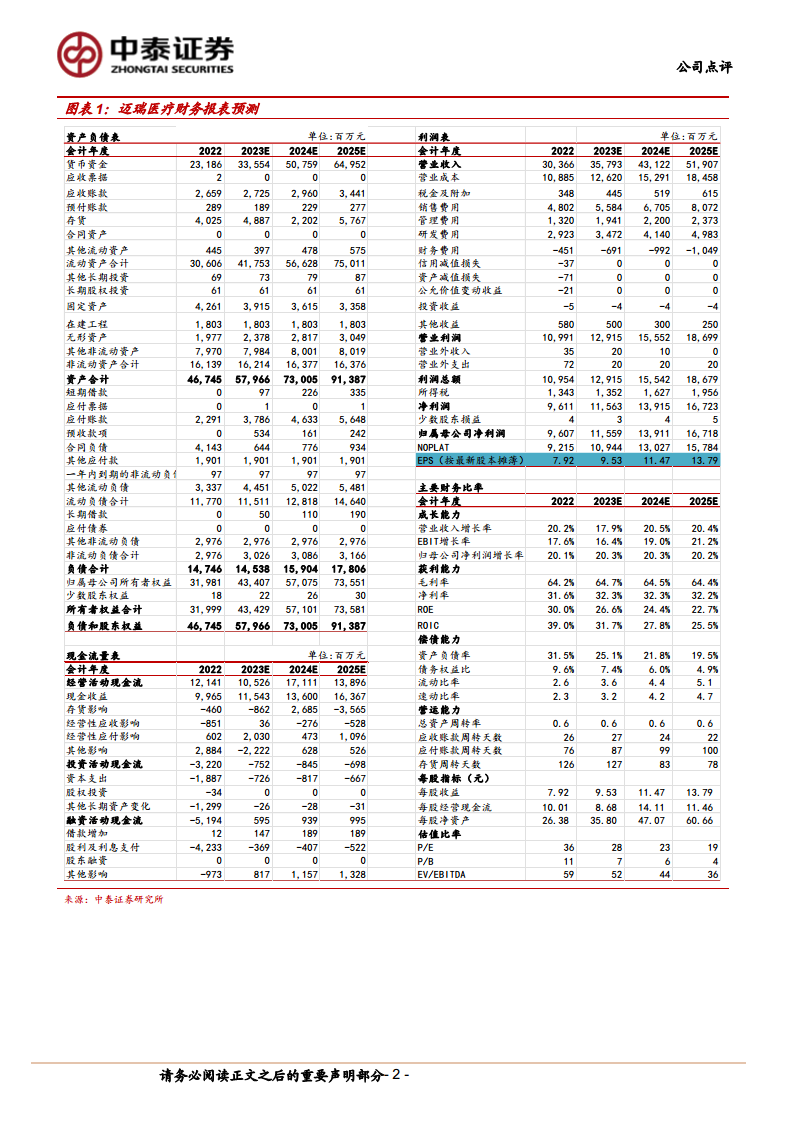
迈瑞医疗(300760):收购心血管介入国产龙头,有望助力公司综合竞争力提升
迈瑞医疗(300760):收购心血管介入国产龙头,有望助力公司综合竞争力提升
-
下载次数:
2083 次
-
发布机构:
中泰证券
-
发布日期:
2024-01-30
-
页数:
3页
中心思想
创新驱动与市场活力持续
本周医药行业在创新药研发、仿制药一致性评价及全球投融资方面均展现出活跃态势。国内创新药注册申报持续增长,多款新药获批临床或上市,尤其在肿瘤、罕见病等领域取得进展。仿制药市场通过一致性评价的品种数量可观,进一步提升了药品质量和市场竞争力。
研发多元化与国际合作深化
全球创新药研发进展涵盖CAR-T、双特异性蛋白、ADC、基因疗法等多种前沿技术,适应症广泛。临床试验结果积极,尤其在肿瘤、神经退行性疾病等领域取得突破性进展。医药企业间的BD交易和战略合作活跃,聚焦基因编辑、AI制药等新兴技术,推动行业协同发展。
主要内容
本周医药行业核心数据回顾
国内新药注册与上市概览
- 创新药/改良型新药注册申报分析:
- 2024年1月15日至1月21日期间,国家药品审评中心(CDE)共承办56个创新药/改良型新药注册申请(不含补充申请),其中国产药品受理号43个,进口药品受理号13个。
- 本周共有41款创新药/改良型新药临床试验申请获得“默示许可”,包括化学药23款、生物药17款、中药1款。
- 值得关注的获批临床新药包括:百吉生物BRL03注射液(靶向EBV阳性晚期实体瘤的基因修饰TCR-T细胞制品)、凌意生物LY-M001注射液(治疗I型或III型戈谢病的腺相关病毒基因治疗药物)、神州细胞SCTC21C注射液(靶向CD38的单克隆抗体)。
- 本周有1款新药获批上市,即惠升生物申报的1类新药加格列净片,作为钠-葡萄糖协同转运蛋白2(SGLT2)抑制剂,用于改善成人2型糖尿病患者的血糖控制。
- 仿制药/生物类似物注册申报分析:
- 本周CDE共承办87项仿制药注册申请,其中新注册分类上市申请受理号85项,新注册分类临床申请受理号2项。本周无生物类似物注册申报动态。
- 通过一致性评价全局分析: 本周共有14个品种(按受理号计17项)通过一致性评价,主要为系统用抗感染药(占比47%),剂型以注射剂为主(占比71%)。盐酸非索非那定片、注射用美罗培南与注射用亚胺培南西司他丁钠过评受理号数量最多,均为2个。海口奇力制药股份有限公司过评品种数最多,为2种。
- 视同通过一致性评价全局分析: 本周共有46个品种(按受理号计65项)视同通过一致性评价,其中抗肿瘤药和免疫机能调节药占比约22%。剂型主要为注射剂和片剂。艾曲泊帕乙醇胺片、非布司他片和麦考酚钠肠溶片受理号数量最多。石家庄四药有限公司、浙江华海药业股份有限公司、江苏奥赛康药业有限公司和成都通德药业有限公司过评品种数最多,均有2种。
- 首次过评/视同过评及过评/视同过评达5家品种盘点: 本周首次通过一致性评价的品种包括碳酸锂片(湖南千金湘江药业)和他克莫司胶囊(杭州中美华东制药)。艾曲泊帕乙醇胺片本周有4家企业视同通过,累计达到5家过评企业。富马酸比索洛尔片和泊沙康唑肠溶片也达到或接近5家过评企业。
全球投融资与研发动态
- 全球医药大健康行业投融资事件盘点:
- 2024年1月15日至1月21日期间,全球医药大健康行业共发生投融资事件55起,较上周减少5起。其中,创新药类融资20起(占比37%),医疗器械耗材投资热度较高,为17起(占比31%)。
- 国内医药大健康行业共发生投融资事件17起,较上周减少6起。医疗器械耗材占比最高(47%,8起),创新药占比29%(5起)。
- 大额投融资事件包括:精准放疗软件公司Manteia数据科技有限公司完成1.1亿元B轮融资;专注新一代脑机接口底层技术研发的阶梯医疗完成数亿元人民币A轮融资。
- 全球创新药研发进展:
- 肿瘤治疗领域: 科济药业靶向GPC3的CAR-T产品CT011获批临床,针对肝细胞癌;石药集团双特异性融合蛋白JMT106在美国获批临床,靶向GPC3阳性实体瘤;荣昌生物ADC(RC88)与信达生物PD-1抑制剂(信迪利单抗)联合用药获批临床,治疗晚期恶性实体瘤;诺诚健华BCL2抑制剂ICP-248在美国获批临床,用于血液肿瘤;齐鲁制药ALK/ROS1抑制剂伊鲁阿克获批新适应症,一线治疗非小细胞肺癌;康方生物CD47单抗AK117三联疗法获批临床,治疗急性髓系白血病;神州细胞抗PD-1单抗(SCT-I10A)联合贝伐珠单抗(SCT510)申报上市,一线治疗肝细胞癌;正大天晴TIM-3单抗TQB2618启动临床,一线治疗肝细胞癌;元宋生物溶瘤病毒新药YSCH-01申报临床,具有双重抗肿瘤作用。
- 其他疾病领域: 齐鲁制药雷珠单抗生物类似药QL1205在欧盟获批,用于多种眼科疾病;奥赛康药业注射用右兰索拉唑获批上市,用于治疗伴有出血的胃、十二指肠溃疡;恩凯赛药非基因修饰NK细胞药物NK010在美国获批临床,首选卵巢癌适应症;拜耳sGC激动剂BAY 3283142片在中国获批临床,针对慢性肾病;维亚臻生物siRNA新药VSA003注射液拟纳入突破性治疗品种,针对纯合子型家族性高胆固醇血症;百济神州抗PD-1单抗替雷利珠单抗递交第15项适应症上市申请,用于可切除非小细胞肺癌围术期治疗;阿斯利康“first-in-class”口服小分子Voydeya(danicopan)获日本批准,作为C5抑制剂的附加疗法治疗PNH患者的血管外溶血。
- 本周全球积极/失败临床结果:
- 肿瘤治疗: Theralase光敏化合物TLD-1433治疗非肌肉浸润性膀胱癌2期临床90天时达62%完全缓解;罗氏TIGIT单抗tiragolumab联合疗法一线治疗食管鳞状细胞癌3期试验达双主要终点(PFS和OS显著改善);国鼎生技RAS靶向小分子Hocena一线治疗转移性胰腺癌2期临床中位总生存期达14.1个月;MD安德森CAR-NK细胞疗法治疗耐药癌症总缓解率48.6%,1年总生存率68%;MAIA小分子THIO联合PD-1抑制剂治疗非小细胞肺癌疾病控制率达100%;阿斯利康PD-L1抑制剂Imfinzi联合TACE和贝伐珠单抗一线治疗肝细胞癌3期临床PFS达15个月,较对照组(8.2个月)显著延长。
- 其他疾病: 和其瑞医药单抗HMI-115治疗雄激素性脱发1b期临床获积极成果,平均目标区域非毳毛数量增加14根/平方厘米;Immunity Pharma药品IPL344治疗肌萎缩侧索硬化(ALS)2a期试验减缓疾病进展48%;REGENXBIO眼科基因疗法ABBV-RGX-314治疗湿性年龄相关性黄斑变性2期临床显示,最高剂量组患者对后续抗VEGF治疗需求降低达80%。
- 全球医药企业BD交易/战略合作事件盘点:
- Genevant Sciences与Tome Biosciences达成超1亿美元合作和非独家许可协议,结合脂质纳米颗粒(LNP)技术与可编程基因组整合(PGI)技术,开发体内基因编辑疗法治疗罕见单基因肝脏疾病。
- 德睿智药与上海复宏汉霖生物技术股份有限公司达成战略合作,共同研发AI赋能的抗体偶联药物(ADC)和抗衰老疗法平台。
总结
本周医药行业整体呈现出稳健的创新发展态势,尤其在肿瘤、罕见病和慢性病领域,国内外均有显著的研发进展和临床突破。创新药的临床前推和上市审批持续活跃,仿制药一致性评价工作稳步推进,有助于提升药品可及性和质量。尽管全球投融资事件数量略有下降,但大额交易和对前沿技术(如基因编辑、AI制药、脑机接口)的投资热情不减,预示着未来行业将继续向高科技、高附加值方向发展。临床试验结果积极,为多种难治性疾病带来了新的治疗希望,特别是肿瘤免疫疗法和基因疗法展现出巨大潜力。战略合作和BD交易的活跃,也反映了行业内对技术整合和协同创新的需求。
-

金域医学(603882):产品组合持续优化,数据要素价值逐步释放
-

安图生物(603658):政策影响下阶段性承压,装机加速+创新+出海支撑中长期成长
-

迈瑞医疗(300760):拐点已现,海外提速驱动业绩基本面逐季改善
-

医药生物行业11月月报暨2025三季报总结:Q3总结:环比改善延续,创新药行情有望重燃
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送