-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

阿尔茨海默病行业研究:老龄化趋势下的流行病学特征与产业布局分析
阿尔茨海默病行业研究:老龄化趋势下的流行病学特征与产业布局分析
-
下载次数:
1414 次
-
发布机构:
未知机构
-
发布日期:
2024-12-09
-
页数:
19页
中心思想
阿兹海默症负担加剧与诊疗创新驱动市场增长
随着全球人口老龄化趋势的加剧,阿尔茨海默病(AD)的流行病学负担持续上升,我国AD患病率、发病率和死亡率均高于全球平均水平,且呈现显著的增长趋势,尤其在老年女性群体中更为突出。这一严峻的公共卫生挑战,正强力驱动着AD诊疗市场的创新与发展。
靶向Aβ药物突破与诊断技术进步重塑产业格局
近年来,AD药物研发在靶向β淀粉样蛋白(Aβ)领域取得了突破性进展,Lecanemab和Donanemab等新一代单抗药物的上市,为早期AD患者带来了延缓认知衰退的希望,尽管其安全性和有效性仍需持续关注。同时,影像学(如Aβ-PET)和体液学(如血液P-tau)诊断技术的不断成熟与商业化,正逐步解决AD早期诊断的难题,为精准用药奠定基础,共同重塑AD产业的未来格局。
主要内容
一、老龄化背景下,阿兹海默流行病学呈上升趋势
全球与中国AD流行病学现状及趋势
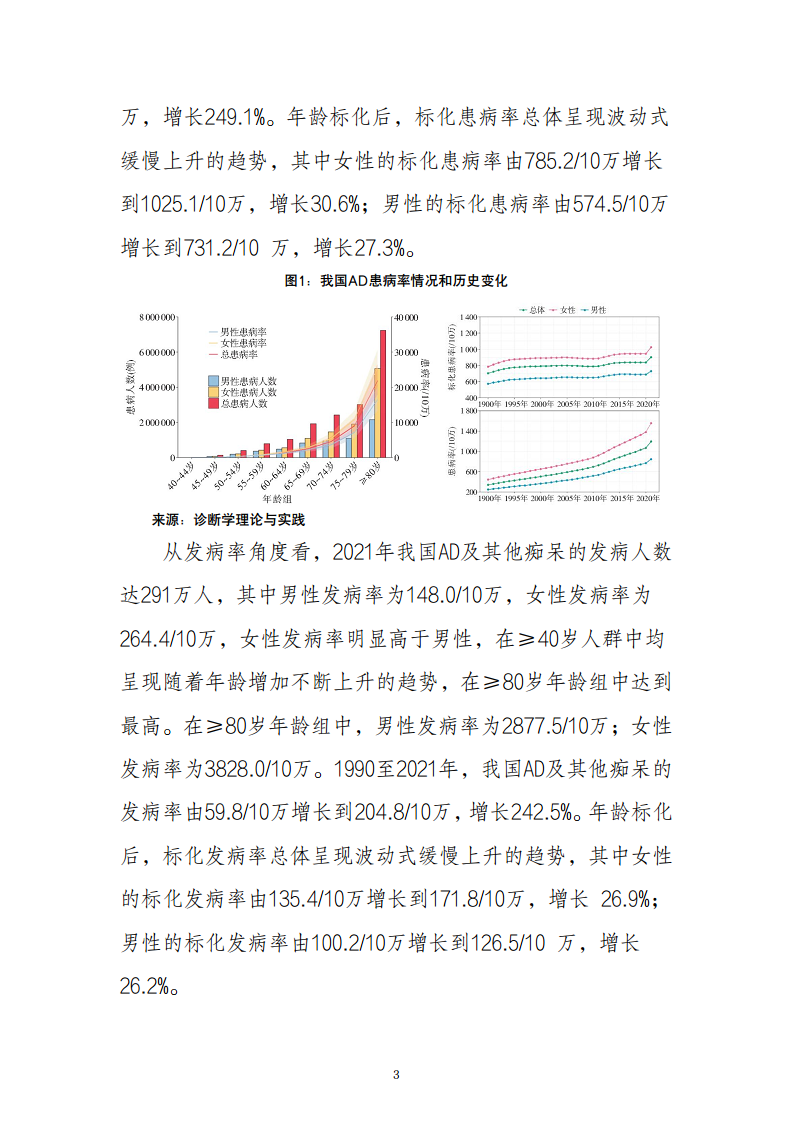
阿尔茨海默病(AD)作为一种渐进性神经退化性疾病,严重影响患者生活质量。2021年,全球AD及其他痴呆患病人数达5700万,其中中国以1699万例占据全球总数的29.8%。全球年龄标化患病率为696.0/10万,而我国高达900.8/10万,显著高于全球平均水平。从患病率来看,2021年我国女性患病率(1558.9/10万)明显高于男性(846.3/10万),年龄标化后女性患病率(1025.1/10万)仍高于男性(731.2/10万)。患病人数和患病率在≥40岁人群中随年龄增长而上升,在≥80岁年龄组达到峰值,男性患病率为16517.7/10万,女性为25527.2/10万。1990年至2021年,我国AD及其他痴呆的总患病率从342.1/10万增长至1194.2/10万,增幅达249.1%。年龄标化患病率总体呈波动式缓慢上升,其中女性增长30.6%,男性增长27.3%。
AD发病率与死亡率的持续攀升
2021年,我国AD及其他痴呆发病人数达291万人,女性发病率(264.4/10万)高于男性(148.0/10万),且在≥40岁人群中随年龄增长而上升,≥80岁年龄组达到最高。1990年至2021年,我国AD及其他痴呆发病率从59.8/10万增长至204.8/10万,增幅242.5%。年龄标化发病率亦呈缓慢上升趋势。 在死亡率方面,2021年全球因AD及其他痴呆导致的死亡人数达195.6万例,我国占25.2%(49.3万例)。全球年龄标化死亡率为25.2/10万,我国为30.9/10万,高于全球平均。女性死亡率(47.4/10万)显著高于男性(22.5/10万),且随年龄增长而上升。1990年至2021年,我国AD及其他痴呆总死亡率从10.2/10万增长至34.6/10万,增幅239.2%。AD已成为我国主要疾病死因之一,2019年位列第五,随着老龄化进程,AD患者数量预计将进一步攀升。
二、阿兹海默药物的研发进展
现有治疗手段与发病机制假说
AD的治疗主要分为药物治疗和非药物治疗。药物治疗包括改善认知症状(如胆碱酯酶抑制剂、NMDA受体拮抗剂、银杏叶提取物、甘露特钠胶囊)和控制精神行为症状(如非典型抗精神病药、5-羟色胺类药)。AD发病机制复杂,业界认可的假说包括β淀粉样蛋白(Aβ)异常沉积、Tau蛋白磷酸化和胆碱能损伤等,其中靶向淀粉样蛋白一直是新药开发的重要方向。
(一) β药物研发进展
Aducanumab的争议与退市: 美国FDA于2021年6月加速批准首款靶向Aβ单抗Aducanumab上市,但其三期临床数据(301和302研究)在改善认知效果上存在不确定性(302有效而301无效),导致FDA委员会投票否决上市申请。尽管FDA力排众议批准,但因疗效不确定和高定价(56000美元/年),Medicare拒绝覆盖,最终百健于2024年1月停止了Aducanumab的销售和开发。 Lecanemab的积极进展: 百健的另一款Aβ药物Lecanemab进展顺利。2024年阿尔茨海默病协会国际会议公布的三年临床ClarityAD最新结果显示,Lecanemab组在临床痴呆评级-框架总和(CDR-SB)评分上,与安慰剂组相比平均减少0.45分,且在三年治疗中认知衰退幅度平均减少0.95分。安全性方面,未观察到新的安全问题,淀粉样蛋白相关成像异常水肿/积液(ARIA-E)多发生在治疗前六个月,且多为轻度至中度、无症状并可自行消退。Lecanemab与可溶性低聚物(原纤维)的结合能力强于Aducanumab,这可能解释了其不同的临床表现。 Donanemab的获批上市: 2024年7月,礼来宣布新一代抗Aβ单抗Donanemab获FDA批准上市,用于AD所致的轻度认知障碍及轻度AD。其三期临床TRAILBLAZER-ALZ2研究显示,在中低tau蛋白水平受试者中,主要终点指标iADRS延缓认知功能下降达35%,CDR-SB评分延缓36%;在所有受试者中,分别下降22%和29%。安全性方面,Donanemab组不良事件发生率89%,包括ARIA-E(24%)和ARIA-H(18%)。 Lecanemab与Donanemab的对比: 两款主流Aβ单抗的III期临床入组人数、多中心试验结果和ApoE E4基因携带分布相似。Donanemab的入组病人基线认知障碍程度相对更严重,给药频率较低(Q4W vs Q2W)。在CDR-SB改善方面,两者与安慰剂组均有显著差异(Donanemab 29% vs Lecanemab 27%)。安全性方面,Donanemab引起的严重不良事件(17.4% vs 14.0%)和ARIA-E比例(24% vs 12.6%)略高,但输注反应较少。两者引起的ARIA-E大部分为轻度至中度、无症状且可自行缓解。总体而言,两款药物的有效性和安全性差异不大。
(二) 全球药物研发进展
AD药物研发管线概览: 根据Jeffrey Cummings教授等人2024年1月发布的数据,全球共有164项针对AD预防、MCI及痴呆症阶段的临床试验正在进行,涵盖127款药物,数量较2023年有所缩减。其中,III期临床48项(32款药物),II期临床90项(81款药物),I期临床26项(25款药物)。在研药物几乎涵盖AD发生过程中的所有可能靶点,主要集中在神经递质受体(22%)、神经炎症(20%)和β淀粉样蛋白相关过程(18%)。 基因与细胞疗法崭露头角: 基因和细胞疗法是AD研发的重要方向。Sangamo公司基于锌指蛋白平台靶向Tau蛋白基因MAPT,通过AAV衣壳穿越血脑屏障。LEXEO Therapeutics公司的基因疗法LX1001通过递送APOE2转基因,在初步数据中显示患者脑脊液中Tau蛋白和磷酸化Tau蛋白水平下降。Longeveron公司的Lomecel-B获得FDA再生医学先进疗法(RMAT)认定,是首个获此认定的AD细胞疗法。NKGen Biotech的NK细胞疗法SNK01在临床试验中显示90%患者的AD综合评分改善或保持稳定。 研发挑战与国内进展: 尽管有诸多药物在研,但AD药物研发进展相对缓慢,多款药物以失败告终,如诺华的Umibecestat、卫材的Elenbecestat和礼来的Lanabecestat等III期临床失败。国内在研品种多为传统化药的改构或剂型改良,创新药主要聚焦Aβ,其中恒瑞医药进展较快。中医药治疗AD的临床试验也正在进行,包括益智清心方、黄芪等中药及针灸等疗法。
三、AD 诊断是用药的前提
诊断方法多样性与影像学进展
临床AD诊断主要包括神经影像学、分子影像学、体液检测学和神经心理测评。 影像学诊断: 磁共振成像(MRI)和计算机体层成像(CT)是神经影像学检查的主要方式,MRI因对脑组织成像更清晰而作为首选。功能MRI因图像异质性大、缺乏统一流程和泛化能力不佳而限制了临床应用。 PET技术在AD诊断中的关键作用: 2018年美国国立老化研究所与阿尔茨海默病协会明确了正电子发射型计算机断层显像(PET)技术在AD全病程诊断中的重要作用。AD相关的PET检查主要包括β淀粉样蛋白-PET(Aβ-PET)、Tau-PET和氟代脱氧葡萄糖(FDG)-PET。尽管PET检查费用昂贵且尚未纳入医保,国内具有Aβ-PET、Tau-PET检查能力的医院数量有限,但其诊断价值日益凸显。 Aβ-PET与Tau-PET的国内突破: Aβ-PET因能显示Aβ在脑中的分布并进行半定量评价而尤为重要,其诊断AD的灵敏度可达80%-100%。2023年9月,先通医药的欧韦宁(氟[18F]贝他苯注射液)获NMPA批准,成为国内首个获批的AD诊断Aβ-PET示踪剂,东诚药业旗下安迪科的氟[18F]洛贝平注射液也已申报上市。Tau-PET针对病理性错误折叠的Tau蛋白,我国首个Tau蛋白示踪剂产品18F-APN-1607已进入3期临床试验。脑FDG-PET则通过检测脑葡萄糖代谢异常来提示神经元和星形胶质细胞的代谢受损。
体液学诊断的便捷性与精准性提升
理想的AD体液标志物需具备高灵敏度、特异度,能反映病程发展,且临床可实践性好。现有脑脊液、血液和尿液三种来源。 脑脊液标志物: 国内记忆门诊已常规进行脑脊液Aβ、总蛋白(T-tau)和磷酸化蛋白(P-tau)检测。脑脊液Aβ42/Aβ40比值降低对鉴别AD与其他神经疾病有良好灵敏度和特异度。脑脊液T-tau和P-tau(尤其是P-tau181和P-tau217)升高更能反映AD病理变化,联合应用Aβ42、Aβ42/Aβ40比值、T-tau和P-tau181可实现更高准确率。然而,脑脊液检测的侵入性限制了其临床运用。 血液学标志物的崛起: 血浆总Aβ或Aβ42水平在家族性AD患者中增高,在散发性AD患者中早期增高,随后Aβ42/Aβ40比值下降。血浆P-tau181及P-tau217在AD临床研究中表现出良好诊断价值,有望作为潜在标志物纳入未来AD诊断标准,甚至可在认知障碍出现前多年预测AD。诺唯赞在AD血液学检测上处于龙头地位,其Aβ42/40、p-Tau217等标志物已获批。 其他潜在标志物与基因检测: 外周血神经源性外泌体突触蛋白、尿液中AD7C神经丝蛋白、血浆神经丝轻链(NfL)等也都是潜在的AD标志物。基因学检测在AD中推荐级别不高,主要针对家族性AD的致病基因(PSEN1、PSEN2、APP)和易感基因(ApoE4)。 随着Aβ药物的上市,市场对AD的关注度不断提升。作为临床未满足的重大疾病领域,新药研发和诊断方法学的进步将带来巨大的市场机遇。目前诊断方法昂贵、患者接受度低,但随着技术发展,AD市场前景广阔。
四、关注标的
诺唯赞:血液学检测龙头
诺唯赞聚焦酶、抗原、抗体等生命科学上游产品,并拓展至体外诊断领域。在AD血液学检测方面,公司处于龙头地位,临床认可的Aβ42/40、p-Tau217等标志物仅诺唯赞获批,具有显著先发优势。预计随着血液学诊断的推广,有望逐步替代脑脊液甚至部分影像学检测,血液学检测市场规模预计达20-30亿,诺唯赞有望快速进院并抢占先机。
东诚药业:核药与PET诊断先锋
东诚药业是国内核药龙头,在AD的PET检测中具备较强的先发优势。其引进的18F-APN-1607是一种阿尔茨海默症诊断制剂,能与脑内积蓄的Tau蛋白特异性结合,实现更早诊断。该产品已完成III期临床入组并正在进行NDA资料整理,有望随着AD药物渗透率提升带动检测端的放量。
恒瑞医药:国产Aβ药物研发领先者
恒瑞医药作为国内创新药龙头,目前针对Aβ的药物研发进展处于国产前列。公司有望依托其固有的临床推进和商业化优势,实现Aβ药物的快速上市放量,成为未来增长的重要引擎。
通化金马:新型胆碱酯酶抑制剂蓄势待发
通化金马经过多年研发,其核心产品琥珀八氢氨吖啶片(一种新型胆碱酯酶抑制剂)已获得NMPA上市申请受理,用于轻、中度阿尔茨海默病的治疗,有望为现有治疗方案提供新的选择。
总结
本报告深入分析了阿尔茨海默病(AD)在全球及中国的流行病学趋势、药物研发进展、诊断技术现状及市场机遇。在老龄化背景下,AD患病率、发病率和死亡率持续攀升,尤其在中国,其流行病学负担高于全球平均水平,凸显了巨大的未满足临床需求。
药物研发方面,靶向β淀粉样蛋白(Aβ)的单抗药物取得了突破性进展,Lecanemab和Donanemab的上市为早期AD患者带来了延缓认知衰退的希望,尽管Aducanumab的失败也警示了研发的复杂性。全球AD药物研发管线丰富,基因与细胞疗法等新兴方向正崭露头角。国内创新药研发也在积极推进,恒瑞医药等企业在Aβ药物领域取得进展。
诊断技术是AD精准治疗的前提。影像学诊断(特别是Aβ-PET和Tau-PET)和体液学诊断(脑脊液和血液标志物,尤其是血浆P-tau)的进步,正逐步实现AD的早期、精准诊断。国内在Aβ-PET示踪剂和血液学检测领域已取得重要突破,诺唯赞和东诚药业等公司在此领域占据领先地位。
综合来看,AD市场正迎来药物创新和诊断技术进步的双重驱动。随着新药的不断上市和诊断方法的普及,AD的早期筛查、诊断和干预将成为可能,从而带来巨大的市场机遇。相关企业如诺唯赞、东诚药业、恒瑞医药和通化金马等,凭借其在各自领域的优势,有望抓住这一市场先机,实现快速发展。
-

宠物保险研究报告
-

AN-Liver实体瘤伴肝转移诊疗现状调研报告(2024版)
-

虚拟神经病学投资者活动
-

NVS 202410novartisrenalportfolio oprestation
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






最新报告
- 制冷剂行业点评:英美调整三代制冷剂淘汰节奏,利好中国制冷剂出口量价提升
- 医药生物行业双周报2026年第10期总第159期:创新支持与合规监管并进,关注ASCO大会数据催化
- 医药生物行业跟踪周报:2026ASCO中国创新药成果满满,重点推荐康方生物、科伦博泰生物等
- 化工行业研究:磷酸、BDO等涨幅居前,建议关注进口替代、纯内需、高股息等方向
- 医药生物行业周报:sac-TMT 1L肺癌数据优异,夯实IO+ADC下一代疗法基础
- 医药生物行业周报(5月第3周):国产创新药预热ASCO
- 医药生物行业双周报:冠脉支架国采开标
- iza-bren领衔亮相,5款新药7项数据登陆ASCO
- 化工行业周报:国际油价下跌,六氟磷酸锂价格上涨、丙烯酸价格下跌
- 氟化工行业周报:欧美放宽HFCs制冷剂使用限制,英国制冷剂价格大幅调涨,全球制冷剂补库行情或在酝酿
对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送