-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

康方生物(09926):AK112获批+击败K药,创新药龙头价值当被重估
康方生物(09926):AK112获批+击败K药,创新药龙头价值当被重估
-
下载次数:
1058 次
-
发布机构:
德邦证券
-
发布日期:
2024-07-21
-
页数:
38页
中心思想
创新药龙头价值重估
本报告核心观点认为,康方生物(09926.HK)作为创新药龙头企业,其当前海外价值被市场严重低估,公司正处于价值重估的关键时期。核心产品AK112(依沃西)的超预期获批,以及其在头对头临床试验中击败K药的优异表现,极大地提升了其商业化前景和海外成功的确定性。公司已进入双品种(AK112和AK104)驱动的快速发展阶段,并有望凭借其强大的研发能力和丰富的产品管线,进化为具有国际竞争力的中国一流生物制药企业。
多管线驱动与国际化潜力
康方生物不仅在肿瘤领域拥有AK112和AK104两大重磅产品,其非肿瘤管线(如PCSK9、IL12/23、IL17、IL4R)也已有多款产品进入后期临床或申报上市阶段,展现出均衡且多元化的产品布局。此外,公司在ADC等前沿技术领域的布局也预示着未来的增长潜力。AK112与Summit Therapeutics的海外合作进一步强化了其全球化商业布局,预计现有适应症的海外销售峰值将超过30亿美元,为公司带来显著的国际市场收入。基于DCF估值模型,报告维持“买入”评级,目标价为76.48港元,认为公司未来2-3年将进入业绩高速增长期。
主要内容
AK112:核心产品驱动增长
国内超预期获批,海外临床进展快速
AK112(依沃西,PD-1/VEGF双特异性抗体)于2024年5月获批上市,用于治疗EGFR-TKI进展的局部晚期或转移性非鳞状非小细胞肺癌(nsq-NSCLC),审评用时不到10个月,超出市场预期。首批货值过亿元的药物已成功发货。依沃西联合化疗方案已被纳入《2024 CSCO 非小细胞肺癌(NSCLC)诊疗指南》注释。
EGFR-TKI耐药后NSCLC:巨大蓝海市场
- EGFR突变肺癌市场前景广阔,三代TKI用药已成主流: EGFR突变NSCLC市场巨大,三代EGFR TKI已成为主流治疗方案。全球奥希替尼2023年销售额达58亿美元,中国市场销售额也迅速增长。截至2024年5月,中国已有5款三代EGFR TKI获批。
- 目前治疗手段获益有限,化疗PFS 5个月左右,PD-1方案效果不显著: 针对TKI耐药后NSCLC,现有治疗手段有限。铂类化疗中位PFS仅约4-5个月。此前多项免疫+化疗的III期研究(如CheckMate 722、KEYNOTE 789)均未达到主要终点,PFS无显著改善。信迪利单抗联合贝伐珠单抗+化疗的四药方案在ORIENT-31研究中显示出对一代/二代TKI经治患者的显著疗效(PFS HR 0.72),但在T790M突变和两线治疗亚组中获益不显著,凸显三代耐药治疗的难度。
- 双抗提供新方案,强生c-met双抗做出PFS获益: 强生研发的Amivantamab(EGFR/c-MET双抗)于2021年5月获FDA加速批准,并于2024年3月转为常规批准,用于治疗EGFR外显子20插入突变的NSCLC。MARIPOSA-2研究显示,Amivantamab联合化疗(ACP组)或联合Lazertinib+化疗(LACP组)相比单纯化疗,显著延长了PFS(中位PFS分别为6.3个月、8.3个月 vs 4.2个月),疾病进展或死亡风险降低50%以上。
- AK112 ASCO Oral发布三期数据,OS具有明显获益趋势: 2024年ASCO会议上,康方生物口头报告了AK112-301/HARMONi-A III期临床试验结果。该研究入组322名患者,实验组(依沃西+化疗)显著延长了PFS,HR为0.46(95%CI 0.34-0.62, P < 0.0001),中位PFS达7.06个月(对照组4.80个月)。尤其在脑转移患者中,HR为0.40,疗效优异。对三代EGFR TKI经治患者HR为0.48,T790M突变阳性患者HR为0.22。安全性方面,实验组≥3级TEAE发生率(61.5%)高于对照组(49.1%),主要为化疗相关不良事件,但未观察到严重出血、穿孔等VEGF靶点相关严重不良事件。合作伙伴Summit Therapeutics的二期临床数据显示,AK112治疗二线EGFR-TKI耐药NSCLC的中位OS达到22.5个月。
开展多个头对头PD-1临床,有望确定二代IO核心地位
- 单药头对头K药成功,显示新一代IO潜力: 2023年5月,依沃西单药对比帕博利珠单抗(K药)一线治疗PD-L1阳性NSCLC的HARMONi-2(AK112-303)III期临床获决定性胜出阳性结果,显著延长了患者无进展生存期(PFS),成为全球首个且唯一在III期单药头对头临床中证明疗效显著优于帕博利珠单抗的药物。K药2023年全球销售额达250亿美元。
- HARMONi-3:一线晚期驱动基因阴性鳞状非小细胞肺癌: 康方生物在国内开展AK112+化疗 vs 替雷利珠单抗联合化疗的III期研究(AK112-306),同时Summit Therapeutics开展AK112+化疗对比帕博利珠单抗联合化疗的国际多中心III期HARMONi-3研究。AK112-201 II期临床数据显示,依沃西联合化疗一线治疗晚期NSCLC(EGFR/ALK野生型)在鳞状NSCLC患者中ORR达67%,中位PFS达11.0个月,中位OS未达到,24个月OS比率为64.8%(对比K药+化疗的KEYNOTE-407研究,mPFS约8个月,24个月OS比率仅36%),初步数据令人鼓舞。
全面布局肺癌,有望拓展消化道癌肿
- 脑转移非小细胞肺癌(NSCLC): NSCLC脑转移发生率高(20%-65%),预后差(自然平均生存时间1-2个月)。2024年ELCC会议上,公司发布依沃西治疗脑转移NSCLC的疗效分析结果,颅内缓解率达34%,中位PFS达19.3个月,联合化疗方案颅内缓解率达39%,完全缓解(CR)率达25%,且未观察到颅内出血。
- 新辅助治疗NSCLC: 截至2023年12月31日,依沃西单药新辅助治疗可切除NSCLC的病理完全缓解(pCR)率为30%,主要病理缓解(MPR)率为60%;联合化疗方案pCR率为44%,MPR率为74%。
- 治疗PD-1/化疗后进展的NSCLC: AK112-201 II期临床研究队列3数据显示,治疗既往抗PD-1治疗联合含铂双药化疗进展的晚期NSCLC,ORR为40%,DCR为80%,中位DoR为12.7个月,中位PFS为7.1个月,中位OS达17.1个月,12个月OS率为65%。
- 消化道肿瘤: 2024年ASCO会议上,公司发布依沃西联合化疗作为晚期胆道癌(BTC)一线治疗的II期研究结果,ORR为63.6%(胆囊癌患者77.8%),DCR为100%,中位PFS为8.5个月,中位OS为16.8个月。
AK112海外价值潜力巨大,目前适应症海外峰值预计超30亿美金
2022年12月,康方生物授予Summit Therapeutics依沃西在美国、欧洲、加拿大和日本的独家开发和商业化许可权,获得5亿美元首付款,总交易金额有望高达50亿美元,并享有销售净额低双位数提成。2024年6月,双方签署补充协议,将许可市场拓展至中美、南美、中东和非洲等地区,康方生物获得7000万美元首付款和里程碑款,并继续享有销售提成。目前,依沃西在全球范围内已获批1项适应症,有6项III期临床研究正在开展,其中2项由Summit主导的国际多中心III期临床研究(HARMON1和HARMONi-3)正在推进。经测算,AK112现有进入国际三期的两个适应症(EGFR-TKI耐药NSCLC和一线鳞状NSCLC),全球销售峰值预计将超过30亿美元。
AK104:大适应症市场拓展
宫颈癌:一线已NDA,填补国内空白
AK104(卡度尼利,PD-1/CTLA-4双抗)于2022年6月获批上市,用于复发/转移性宫颈癌的二/三线治疗,2023年度销售额达13.58亿元,同比增长149%。2024年4月,卡度尼利联合含铂化疗联合/不联合贝伐珠单抗用于一线治疗持续、复发或转移性宫颈癌的新药上市申请(sNDA)获CDE受理。AK104-303 III期临床研究已达到无进展生存期(PFS)和总生存期(OS)主要研究终点,有望成为全球首个晚期宫颈癌全人群一线治疗的免疫检查点抑制剂。
一线胃癌:AACR发表数据,NDA已获受理
2024年1月,基于COMPASSION-15/AK104-302期中分析阳性结果,卡度尼利联合XELOX用于一线治疗不可手术切除的局部晚期复发或转移性G/GEJ腺癌的新药上市许可申请(NDA)获国家药品监督管理局受理。2024年4月,该研究的期中分析阳性结果在AACR上以口头报告形式发布。研究数据显示,中位OS为15.0个月(对照组10.8个月),HR 0.62(P<0.001)。即使在PD-L1低表达/阴性人群(CPS<5)中,卡度尼利组的中位OS也达14.8个月(对照组11.1个月),HR 0.70,显著优于历史其他免疫检查点抑制剂联合方案。
肝癌:辅助适应症三期进行中,一线治疗效果优异
肝细胞癌(HCC)在中国发病率高(2020年全球新发病例90.6万,中国占46.7%),5年生存率仅12.1%,存在巨大未满足的临床需求。
- 辅助治疗HCC适应症三期进行中,ESMO发表积极数据: 卡度尼利用于高复发风险肝细胞癌根治术后辅助治疗的注册性III期临床研究(AK104-306)正在高效开展。2023年12月ESMO Asia会议上,公司发布卡度尼利新辅助治疗HCC的IIT临床结果,显示联合FOLFOX-HAIC治疗HCC具有良好的抗肿瘤活性,所有患者疾病控制率(DCR)达100%,所有接受2次卡度尼利治疗的患者均达到主要病理学缓解(MPR)。
- 一线治疗HCC效果优异: 卡度尼利联合仑伐替尼一线治疗HCC的Ib/II期临床研究(AK104-206)更新结果发布于2023年ESMO大会。中位随访时间27.4个月,6mg/kg Q2W剂量组ORR为35.5%,中位PFS为8.61个月,中位OS为27.1个月;15mg/kg Q3W剂量组ORR为35.7%,中位PFS为9.82个月,中位OS尚未达到。研究提示高剂量卡度尼利PFS改善更明显,且高于已获批疗法数据。
丰富管线:肿瘤与非肿瘤并进
CD47:新一代人源化lgG4单抗,已开展海外临床
AK117是一款靶向CD47的IgG4单克隆抗体,能高亲和力结合CD47,阻断CD47与SIRPα的相互作用,增强巨噬细胞吞噬活性。其独特构象使其在保持抗肿瘤活性的同时,不会诱导红细胞凝集,无需低剂量预激给药,具有较大的成药可能性。剂量爬坡阶段安全性数据显示,AK117具有良好的安全性,未观察到严重的血液学毒性或血红蛋白下降。
- MDS: 2023年ASH年会发布AK117联合阿扎胞苷(AZA)治疗较高危骨髓增生异常综合征(HR-MDS)的Ib期临床研究积极成果。在27例疗效可评估患者中,完全缓解(CR)率为48.1%,总体缓解率(ORR)为85.2%。在最初依赖红细胞输注的患者中,61.5%经治后不再依赖输注。中位至缓解时间仅0.97个月。AK117联合AZA治疗初诊较高危MDS的随机、双盲、全球多中心II期临床研究申请已获FDA批准。
- AML: AK117联合AZA治疗初诊急性髓系白血病(AML)患者的Ib期临床研究显示,在20例可评估疗效患者中,复合完全缓解率(CCR)达55%。2024年1月,AK117联合AZA和VEN治疗AML三联疗法II期临床试验申请已获NMPA批准。
- 实体瘤: 2023年ASCO会议报告卡度尼单抗联合AK117和化疗治疗晚期G/GEJ腺癌的初步疗效,在8例有反应患者中,ORR为75%,DCR为100%。
丰富的肿瘤研发管线,多个双抗处于临床阶段
- 安尼可®(派安普利,PD-1): 2023年获批一线治疗鳞状非小细胞肺癌适应症,一线治疗鼻咽癌的新药上市申请也获得受理。
- AK109(普络西单抗,VEGFR2): 布局多个PD-1进展后大适应症。
- 多个双抗进入一期临床: AK129(PD-1/LAG3)、AK130(TIGIT/TGF-β)、AK131(PD-1/CD73)、AK132(Claudin18.2/CD47)均已进入一期临床阶段,展现公司在双抗领域的持续创新能力。
非肿瘤管线加大布局,两款产品申报上市
- AK102(PCSK9): 新药上市申请(NDA)于2023年6月获NMPA受理,用于治疗原发性高胆固醇血症和混合型高脂血症以及杂合子型家族性高胆固醇血症。中国高胆固醇血症患者高达1.1亿人,预计PCSK9单抗2030年中国市场规模可达90亿元。
- 依若奇单抗(AK101、IL-12/IL-23): 新药上市申请(NDA)于2023年8月获NMPA受理,用于治疗中重度斑块状银屑病,是国内首家针对IL-12/IL-23靶点的全新序列I类抗体新药。2023年EADV年会数据显示,135mg剂量组第16周PASI75应答率达79.4%(安慰剂16.5%),sPGA0/1应答率达64%(安慰剂11.7%),安全性良好。
- 古莫奇单抗(AK111、IL-17): 2023年8月完成银屑病三期入组。2023年12月1日,治疗中、重度斑块型银屑病的关键注册性III期临床研究达到包括PASI100和sPGA0/1在内的全部疗效终点,疗效和安全性均具有有力竞争优势。公司计划在取得整个研究期间的安全性数据后,推进新药上市申请(NDA)事宜。
- 曼多奇(AK120、IL-4Rα): 治疗中重度特应性皮炎(AD)已开展三期注册研究。同靶点药物度普利尤单抗2022年全球销售额达82.93亿欧元,市场空间广阔。
估值与盈利:业绩高速增长可期
盈利预测
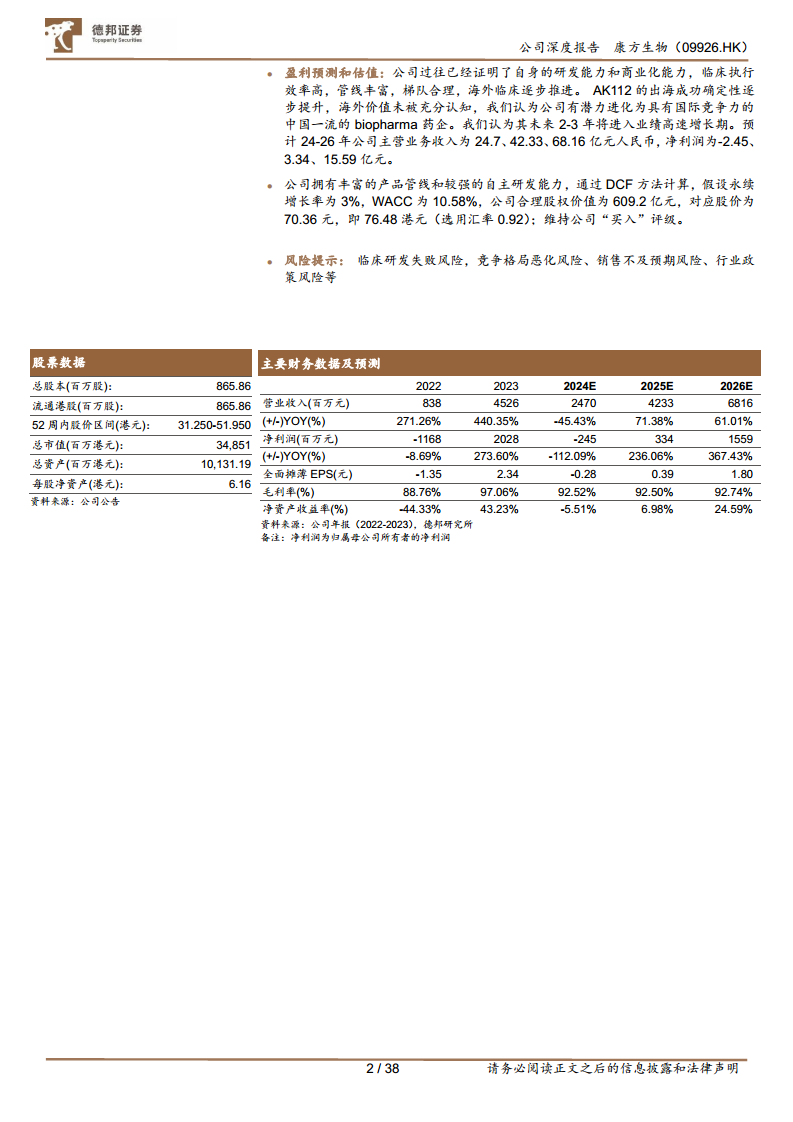
2023年度,康方生物总收入达45.26亿元,同比增长440%。其中,创新药产品销售额16.31亿元(同比增长48%),技术授权和技术合作收入约29.23亿元(主要来自AK112海外授权)。全年研发总投入12.54亿元,实现净利润19.42亿元。截至2023年底,公司现金储备约49亿元人民币。 基于已上市产品和临床后期重磅产品,并假设AK112海外分成比例为低双位数(11%逐步增长至13%),报告预计公司2024-2026年主营业务收入分别为24.7亿元、42.33亿元和68.16亿元人民币。
DCF估值:目标价76.5港元
由于公司尚未实现持续盈利,报告采用DCF估值方法。估值中未包含处于临床II期及更早阶段的早期管线。公司自建工厂生产,预计自营产品毛利率将维持在90%左右,随着海外分成收入提高,毛利率有望进一步提升。销售及管理费用率、研发费用率预计将随着产品收入增长而逐步下降。 通过Wind BETA计算器,公司调整后beta为1.35,无风险收益率假设为十年期国债收益率(2.2%),有效税率假设为15%,计算得出加权平均资本
-

涨价主线!关注活性染料、生物柴油等
-

医药行业周报:美股医疗AI龙头股价反弹,关注AI快速落地的企业
-

博瑞医药:专注代谢药物研发,管线新增口服BGM0504与Amylin类似物
-

医药行业周报:生命科学产业链,需求端逐步回暖,关税战进一步催化国产替代
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送