-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

再生元生物公司(RGNX):Regenxbio公司(RGNX):最新杜氏肌营养不良症(DMD)中期数据积极,但仍需进一步降低风险;维持中性评级
再生元生物公司(RGNX):Regenxbio公司(RGNX):最新杜氏肌营养不良症(DMD)中期数据积极,但仍需进一步降低风险;维持中性评级
-
下载次数:
561 次
-
发布机构:
高华证券
-
发布日期:
2025-06-06
-
页数:
10页
中心思想
RGX-202 临床数据积极但需进一步验证
Regenxbio (RGNX) 针对杜氏肌营养不良症(DMD)的RGX-202基因疗法在1/2期AFFINITY DUCHENNE研究中展现出积极的初步功能性改善和良好的安全性数据,包括北极星步行评估(NSAA)的提升和高水平的微肌营养不良蛋白表达。然而,由于患者样本量较小,投资者对这些发现的广泛适用性和长期疗效仍持谨慎态度。
市场展望与“中性”评级维持
尽管生物标志物数据强劲,但管理层指出将这些发现与功能性结果关联尚为时过早,且部分效应量有所下降。高盛维持对RGNX的“中性”评级,目标价为13美元,并认为在2026年上半年关键性研究顶线数据公布前,需要更多数据来进一步降低投资风险。
主要内容
临床数据与竞争分析
试验设计与患者筛选标准
AFFINITY DUCHENNE研究的入组标准严格,要求患者射血分数大于55%并进行基线心脏检查,以有效控制潜在的心脏相关安全问题,如心肌炎和肌炎。在类固醇使用方面,患者需在研究前使用类固醇12周,并在RGX-202给药后接受短期免疫调节方案,并在3个月内逐渐减量。
功能性疗效数据更新
RGX-202的功能性数据显示出积极信号,但效应量有所减小。
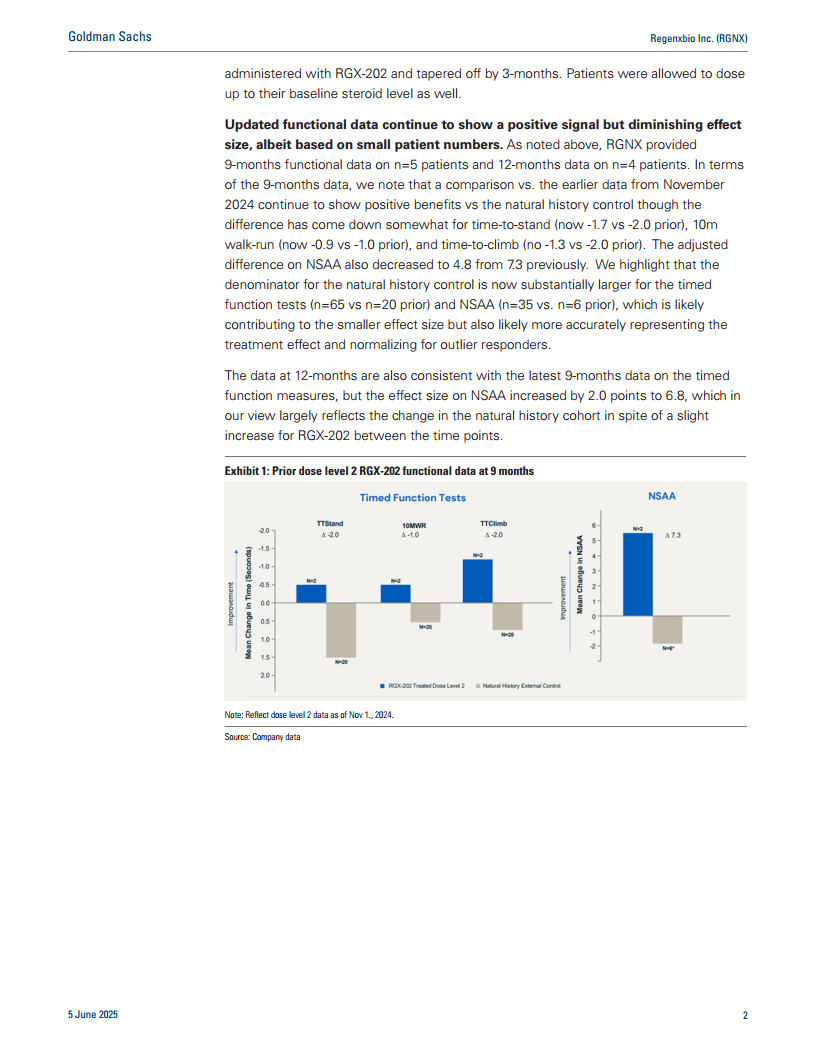
- 9个月数据 (n=5):NSAA平均较基线改善4分,较自然史改善4.8分。与2024年11月的数据相比,NSAA调整后差异从7.3分降至4.8分。定时功能测试(如站立时间、10米步行跑、爬楼时间)的改善幅度也有所下降(例如,站立时间从-2.0秒降至-1.7秒)。
- 12个月数据 (n=4):NSAA平均较基线改善4.5分,较自然史改善6.8分。 效应量减小可能与自然史对照组的样本量显著增加有关(定时功能测试从n=20增至n=65,NSAA从n=6增至n=35),这可能更准确地反映了治疗效果并标准化了异常反应者。
生物标志物表达结果
RGX-202治疗的患者显示出强劲的微肌营养不良蛋白表达水平。一名2岁患者的微肌营养不良蛋白表达量高达对照组的118.6%。值得注意的是,在7岁以上较年长患者中也观察到高相对表达,这表明RGX-202可能在未接受Elevidys治疗的现有患者群体中具有潜在应用价值。
安全性概况与竞争优势
RGX-202的最新中期安全性数据显示出潜在的竞争优势。
- 无严重不良事件:迄今为止,未报告严重不良事件(SAE)或特殊关注不良事件(AEs),也无心肌炎或肌炎病例。这可能部分归因于研究中采用的免疫调节方案。
- 与竞品对比:公司强调RGX-202的安全性优于其他基因疗法,例如Rocket Pharma的RP-A501(不同载体AAV9 vs AAV8,不同疾病背景)和Sarepta的Elevidys(RGX-202无TRAEs报告,而Elevidys有18例TRAEs)。
市场竞争格局分析
RGX-202在安全性方面具有差异化优势,且初步疗效数据在较年长患者群体中表现良好。
- 与Elevidys对比:RGX-202在9个月时NSAA较自然史改善4.8分,12个月时改善6.8分。相比之下,Elevidys在1年时NSAA较自然史改善3.2分,3年时改善7.5分,4年时改善7.0分。RGX-202的安全性数据(无TRAEs报告)也优于Elevidys(18例TRAEs报告)。
- 公司正积极扩大自然史患者数据库,以实现更精确的匹配,从而更准确地评估RGX-202的疗效,并与其他临床阶段资产(如Entrada的ENTR-601-44和Wave Life Sciences的Wave-N531)进行比较。
商业化前景与风险评估
监管策略与商业化展望
Regenxbio有望在2026年上半年公布关键性研究的顶线数据,并计划在今年秋季建立商业库存,为潜在的上市做准备。公司预计,在RGX-202于2027年获批时,约50%的DMD患者群体将可接受治疗。市场趋势显示新生儿筛查的增加将使DMD诊断年龄提前,从而扩大潜在市场规模(TAM)。
估值分析与潜在风险
高盛维持对RGNX的“中性”评级,基于2025-2040财年的折现现金流(DCF)分析,假设折现率为18%,终末增长率为0%,得出12个月目标价为13美元。
- 上行风险:包括湿性AMD和DR基因疗法在眼科医生中推广超预期;竞争资产临床失败;ABBV-RGX-314后期研究安全性结果好于预期。
- 下行风险:包括临床数据(特别是DMD)差于预期;临床试验招募慢于预期;商业销售、上市执行或净定价差于预期;以及不利的监管发展。
总结
本报告对Regenxbio (RGNX) 治疗杜氏肌营养不良症(DMD)的基因疗法RGX-202的最新临床数据进行了专业且分析性的评估。数据显示,RGX-202在功能性改善(NSAA评分提升)和微肌营养不良蛋白表达方面表现积极,且安全性良好,无严重不良事件报告,这在竞争激烈的DMD基因疗法市场中具有潜在优势。然而,由于目前患者样本量较小,且效应量有所下降,投资者仍需谨慎对待。高盛维持对RGNX的“中性”评级,目标价13美元,并强调了未来关键性研究数据(预计2026年上半年公布)以及商业化执行能力对公司估值和市场表现的关键影响。公司在监管计划和商业化准备方面已有所行动,并预计新生儿筛查的增加将扩大其潜在市场。
-

恒瑞医药(600276):恒瑞医药(600276.SS):ADA 2025:GLP-1产品组合的鼓舞性数据集;预计2026年首次推出
-

全球医疗保健:制药业:在即将推出的lenacapavir之前构建HIV暴露前预防(PrEP)市场框架
-

迈瑞医疗(300760):迈瑞(300760.SZ):投资者日要点:强调人工智能和经常性收入,拓展光谱分析 手术机器人领域;买入
-

中国医疗保健:来自我们全球医疗保健会议的解读以及美国市场的投资者反馈
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






最新报告
- 制冷剂行业点评:英美调整三代制冷剂淘汰节奏,利好中国制冷剂出口量价提升
- 医药生物行业双周报2026年第10期总第159期:创新支持与合规监管并进,关注ASCO大会数据催化
- 医药生物行业跟踪周报:2026ASCO中国创新药成果满满,重点推荐康方生物、科伦博泰生物等
- 化工行业研究:磷酸、BDO等涨幅居前,建议关注进口替代、纯内需、高股息等方向
- 医药生物行业周报:sac-TMT 1L肺癌数据优异,夯实IO+ADC下一代疗法基础
- 医药生物行业周报(5月第3周):国产创新药预热ASCO
- 医药生物行业双周报:冠脉支架国采开标
- iza-bren领衔亮相,5款新药7项数据登陆ASCO
- 化工行业周报:国际油价下跌,六氟磷酸锂价格上涨、丙烯酸价格下跌
- 氟化工行业周报:欧美放宽HFCs制冷剂使用限制,英国制冷剂价格大幅调涨,全球制冷剂补库行情或在酝酿
对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送