-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

君实生物(688180):顶刊发表VV116数据,相比P药临床恢复时间更短、安全性更好
君实生物(688180):顶刊发表VV116数据,相比P药临床恢复时间更短、安全性更好
-
下载次数:
2200 次
-
发布机构:
国盛证券
-
发布日期:
2022-12-29
-
页数:
11页
中心思想
VV116临床数据卓越,获国际顶刊认可
君实生物的口服新冠药物VV116与Paxlovid头对头三期临床研究数据在国际顶级医学期刊《新英格兰医学杂志》(NEJM)发表,这是NEJM首次发表的中国自主研发新冠创新药临床试验数据。研究结果显示,VV116在轻中度COVID-19患者中,持续临床恢复时间非劣于Paxlovid,且中位时间更短(4天 vs. 5天),同时安全性顾虑更少,总体不良事件发生率显著低于Paxlovid组(67.4% vs. 77.3%),展现出优异的药效和安全性特征。
公司研发实力获验证,未来增长潜力可期
此次临床研究的成功发布,不仅彰显了君实生物在药物发现、临床研究推进和组织协调方面的卓越能力,也为VV116的商业化前景奠定了坚实基础。考虑到当前国内COVID-19感染发展情势和Omicron变异株的传播力,VV116一旦获批,预计将为公司带来显著的收入弹性。基于VV116的积极进展和市场潜力,国盛证券研究所维持对君实生物的“买入”评级,看好公司未来的发展。
主要内容
VV116三期临床数据发布,药效与安全性获实证
2022年12月29日,君实生物旗下的口服核苷类抗新型冠状病毒(SARS-CoV-2)药物VV116与奈玛特韦片/利托那韦片组合药物(PAXLOVID)头对头治疗轻中度COVID-19的III期临床研究数据,在线发表于国际顶级医学期刊《新英格兰医学杂志》(IF=176.079)。这是NEJM发表的首个中国自主研发新冠创新药临床试验,标志着VV116获得了国际学术界的广泛认可。
该研究是一项多中心、单盲、随机、对照III期临床研究,旨在评价VV116对比PAXLOVID用于轻中度COVID-19高危风险患者早期治疗的有效性和安全性,共入组822例受试者,其中771例(全分析集,FAS)患者接受了VV116(n=384)或PAXLOVID(n=387)的治疗。研究的主要终点为至持续临床恢复时间,次要有效性终点包括COVID-19进展、症状评分、病毒转阴时间等,安全性终点包括不良事件(AE)和严重不良事件(SAE)情况。
有效性方面,研究达到预设主要终点和次要有效性终点。VV116组对比PAXLOVID组中位至持续临床恢复时间更短(4天 vs. 5天),风险比(HR)为1.17(95%置信区间CI,1.01-1.36),显示非劣效性。在每个预定时间节点(第5、7、10、14、28天)上,VV116组症状缓解受试者百分比均高于PAXLOVID组。截至最终分析,研究受试者均无进展为重症/危重症COVID-19或死亡事件。至持续临床症状消失的中位时间两组均为7天,至首次SARS-CoV-2检测呈阴性的中位时间两组也均为7天。
安全性方面,VV116总体安全性良好,总体不良事件发生率低于PAXLOVID。随访28天内,VV116组患者报告不良事件发生率为67.4%,对比PAXLOVID组为77.3%;3级或4级不良事件发生率分别为2.6% vs. 5.7%;严重不良反应事件发生率分别为0.3% vs. 0.5%。此外,VV116不抑制或诱导主要药物代谢酶、不影响主要药物转运蛋白,产生合并用药相互作用的可能性较小,安全性顾虑更少。
VV116既往研究成果积极,全球多项三期临床推进
临床前研究显示,VV116在体内外都表现出显著的抗SARS-CoV-2作用,对SARS-CoV-2原始株和已知重要变异株(Alpha、Beta、Delta和Omicron)均表现出抗病毒活性,同时具有很高的口服生物利用度和良好的化学稳定性、无遗传毒性。在中国健康受试者中进行的3项I期临床研究显示,VV116具有令人满意的安全性、耐受性及药代动力学特征,口服吸收迅速、重复给药可维持有效抗病毒浓度、普通饮食对药物暴露量无影响,相较同类药物既往数据肝毒性风险较低。
VV116已于2021年12月在乌兹别克斯坦获批用于中重度COVID-19患者治疗。2022年5月,VV116在中国Omicron感染者中首个临床研究结果发表于《Emerging Microbes & Infections》,显示VV116组核酸转阴时间为9.92天(对照组11.13天),从开始用药到核酸转阴平均时间为3.52天,且在首次核酸检测阳性5日内使用VV116的受试者中,其核酸从首次检测阳性到转阴的平均时间为8.56天(对照组11.13天),安全性良好。
目前,VV116已在全球范围内开展4项III期临床研究,包括针对中重度COVID-19的VV116对比标准治疗的国际多中心、随机、双盲III期临床研究;针对轻中度COVID-19的国际多中心、双盲、随机、安慰剂对照的III期临床研究;以及已完成并发表数据的轻中度COVID-19对比PAXLOVID的III期临床研究;和针对Omicron毒株特性纳入轻中度COVID-19伴或不伴高危风险因素患者的多中心、双盲、随机、安慰剂对照的III期临床研究。
盈利预测与投资建议
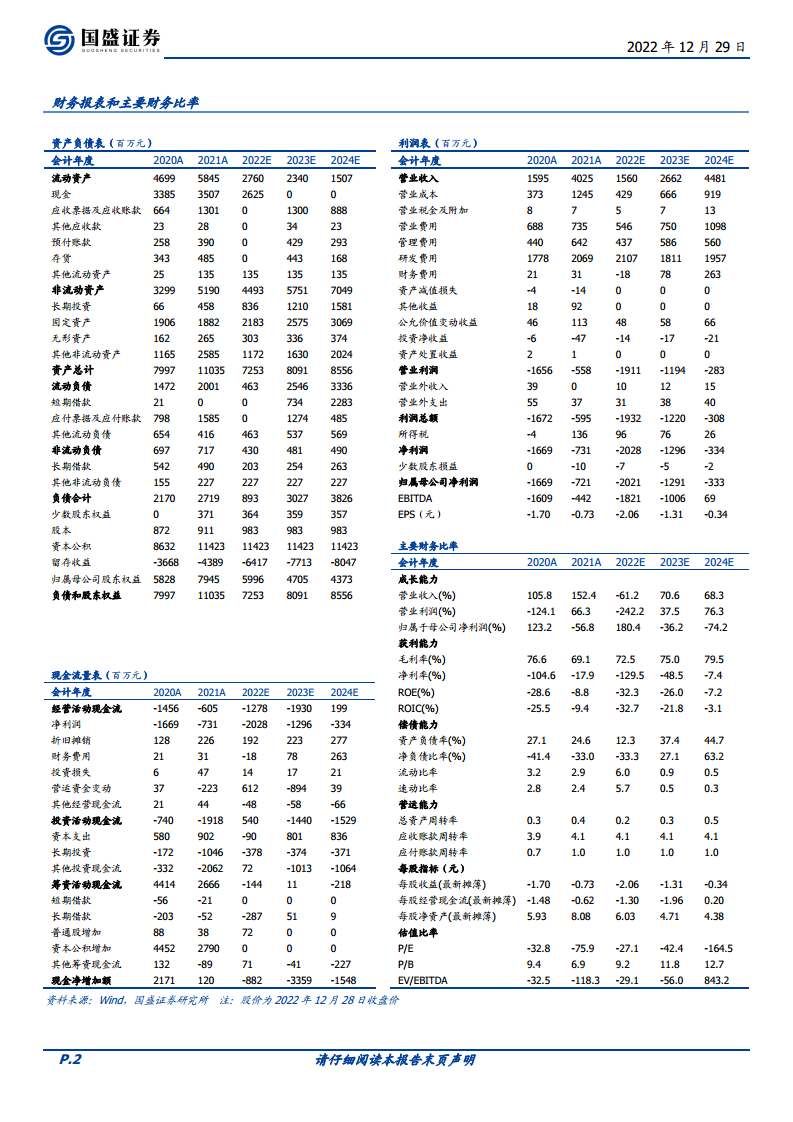
报告暂不考虑VV116的商业化收入,预计君实生物2022-2024年收入分别为15.60亿元、26.62亿元、44.81亿元,同比增长分别为-61.2%、70.6%、68.3%。归母净利润预计分别为-20.21亿元、-12.91亿元、-3.33亿元,对应EPS分别为-2.06、-1.31、-0.34元。考虑到目前国内的COVID-19感染发展情势和Omicron传播力,VV116获批将为公司带来较大的收入弹性,国盛证券研究所看好公司发展,维持“买入”评级。
风险提示
存在研发失败的风险;项目推进不及预期的风险。
总结
本报告详细分析了君实生物口服新冠药物VV116与Paxlovid头对头三期临床研究的积极数据,该数据已在《新英格兰医学杂志》发表,证实了VV116在缩短轻中度COVID-19患者临床恢复时间方面的非劣效性,并展现出更优的安全性。报告强调了VV116扎实的临床前和早期临床基础,以及在全球范围内多项三期临床试验的积极进展。尽管当前财务预测未计入VV116商业化收入,但鉴于其卓越的临床表现和国内疫情形势,VV116的获批预计将为君实生物带来显著的收入增长潜力。基于此,报告维持了对君实生物的“买入”评级,并提示了研发失败和项目推进不及预期的潜在风险。
-

国盛证券医药生物周周题、周观点
-

公牛集团(603195):营收及业绩降幅环比收窄,现金流健康
-

海康威视(002415):基本面企稳回暖,AI赋能企业数字化已进入落地阶段
-

仙乐健康(300791):环比加速,业绩亮眼
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






最新报告
- 医药生物行业周报(26年第23周):ASCO会议顺利闭幕,关注具备高质量创新能力的公司
- 基础化工行业研究:R22、煤焦油等涨幅居前,建议关注进口替代、纯内需、高股息等方向
- 医疗器械行业2026年中期策略:紧扣出海创新,掘金器械复苏
- AI系列深度(十一):高频高速覆铜板有望拉动高性能硅微粉需求持续增长
- 基础化工行业周报:硫磺价格持续上涨,巨化股份超纯PFA量产
- 2025年化学制药行业经济运行报告
- 2025中医药市场研究报告
- EGFR×HER3双抗ADC iza-bren硕果频出,多管线驱动成长
- 服务价格落地,一次性高值耗材推广加速
- 北交所信息更新:NL003塞多明基注射液获批上市,填补我国CLTI临床对因治疗空白
对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送