-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

公司首次覆盖报告:自免赛道龙头企业,新管线赋能中长期发展
公司首次覆盖报告:自免赛道龙头企业,新管线赋能中长期发展
-
下载次数:
403 次
-
发布机构:
开源证券股份有限公司
-
发布日期:
2024-06-18
-
页数:
46页
三生国健(688336)
深耕自免赛道近二十年,核心自免产品已进入后期临床阶段
公司是国内首批专注于抗体药物研发的创新型生物医药企业,目前已有3款单抗产品获批上市,4款核心在研产品进入III期临床。2023年,公司将眼科与肿瘤管线授权沈阳三生,进一步聚焦自免领域。短期看,核心上市产品益赛普销售额企稳回升,赛普汀与健尼哌快速放量,业绩整体稳健增长。中长期维度看,4款自免单品均已进入III期临床,疗效优异进度领先,预计在未来几年将陆续上市。凭借在自免赛道近二十年的深耕,在研自免管线上市后有望快速放量,为公司未来业绩增长贡献新动能。我们看好公司长期发展,预计2024-2026年营业收入为12.08/13.40/16.07亿元,同比增长19.14%/10.89%/19.99%,EPS为0.46/0.39/0.59,当前股价对应PS为11.2/10.1/8.4倍,首次覆盖,给予“买入”评级。
益赛普销售企稳回升,赛普汀/健尼哌快速放量,推动业绩稳健增长
公司目前共拥有益赛普、赛普汀、健尼哌3款上市产品,凭借较强的商业化推广能力,均具有较好的市场表现。益赛普于2005年上市,是中国风湿病领域第一个上市的肿瘤坏死因子抑制剂,市占率在国内占据领先地位;2023年益赛普销量稳中有升,国内销售同比增长约10.5%。赛普汀与健尼哌快速放量,2023年销售额约2.3/0.44亿元,同比增长41.8%/59.4%,推动公司业绩稳健增长。
4款核心自免产品均已进入III期临床,具有较大的放量潜力
公司围绕自免各适应症领域进行布局,4款核心在研管线均已进入III期临床,整体疗效优异、临床进度领先。SSGJ-608(IL-17A)针对斑块状银屑病已于2023年12月达到III期主要临床终点,预计将成为第三款上市的国产IL-17A靶向药物。SSGJ-611(IL-4R)针对成年中重度AD已于2023年12月进入III期临床,针对CRSwNP与COPD已进入II期临床。同时,公司差异化布局了SSGJ-610(IL-5)与SSGJ-613(IL-Iβ)两大管线,针对嗜酸性粒细胞哮喘与急性痛风性关节炎适应症均已进入III期临床,竞争格局较好,未来拥有较大的放量潜力。
风险提示:药物临床研发失败、药物安全性风险、核心成员流失等。
中心思想
聚焦自免赛道,驱动中长期增长
三生国健作为国内首批专注于抗体药物研发的创新型生物医药企业,凭借近二十年在自身免疫(自免)赛道的深耕,已成功上市三款单抗产品,并有四款核心自免在研产品进入III期临床阶段。公司于2023年战略性地将眼科与肿瘤管线授权沈阳三生,进一步聚焦自免领域,此举有望赋能公司中长期发展。
现有产品稳健增长,创新管线潜力巨大
短期来看,核心上市产品益赛普销售额企稳回升,赛普汀与健尼哌实现快速放量,共同推动公司业绩稳健增长。展望中长期,四款进入III期临床的自免单品,包括SSGJ-608(IL-17A)、SSGJ-611(IL-4R)、SSGJ-610(IL-5)及SSGJ-613(IL-1β),均展现出优异的疗效和领先的临床进度,预计未来几年将陆续上市,凭借公司在风湿科等领域的丰富渠道资源,有望快速放量,为公司未来业绩增长贡献新动能。开源证券首次覆盖给予“买入”评级,预计2024-2026年营业收入分别为12.08/13.40/16.07亿元,同比增长19.14%/10.89%/19.99%。
主要内容
三生国健:深耕自免赛道近二十年,新管线赋能未来发展
战略聚焦自免赛道,4款核心自免产品已进入III期临床
- 三生国健成立于2002年,是中国首批专注于抗体药物研发的创新型生物医药企业,拥有研、产、销一体化成熟平台。
- 公司目前拥有3款上市药品和13个处于不同开发阶段的在研创新药物。
- 2023年4月,公司将抗肿瘤项目(602、609、705)和眼科项目(601A)等授权给沈阳三生,交易对价包括首付款4.2亿元及后续15%的权利金,此举旨在战略聚焦自免领域。
- 目前,公司核心在研管线聚焦自免领域,其中SSGJ-608(IL-17A)、SSGJ-611(IL-4R)、SSGJ-610(IL-5)及SSGJ-613(IL-1β)四款产品均已进入III期临床阶段,具有较大放量潜力。
- 公司股权结构稳定,富健药业持有35.92%股份,三生制药为实际控制人。
- 公司核心团队经验丰富,平均拥有超过20年制药行业经验,董事长LOU JING先生和总经理刘彦丽女士在生物制药和公司运营管理方面具有深厚背景。
- 公司已在上海建成规模超40000升的抗体药物商业化生产基地,拥有自主知识产权的填料和培养基,可提供全流程CDMO服务。截至2023年,公司固定资产约8.74亿元,同比增长23.3%;在建工程达6.88亿元。
- 公司在国内自免赛道布局较早,在风湿科等领域积累了丰富的渠道资源,拥有由300余名专业销售人员组成的营销团队,覆盖超4400家医疗机构,其中约2000家为三级医院。
核心产品稳健放量,盈利能力快速提升
- 受疫情及益赛普竞争加剧影响,公司业绩在2020年起波动较大。
- 随着益赛普预充针上市提升竞争力,公司营收自2023年起企稳回升,利润端实现快速增长。2023年营收10.14亿元,同比增长22.84%;扣非归母净利润2.07亿元,同比增长85105.24%。
- 2024年第一季度,公司营收2.67亿元,同比增长28.72%;扣非归母净利润8576万元,同比增长203.60%。
- 益赛普2023年国内销售收入5.70亿元,同比增长10.5%,销售企稳。
- 创新产品赛普汀与健尼哌快速放量,2023年销售额分别达2.30亿元(同比增长41.8%)和0.44亿元(同比增长59.4%)。
- 2023年公司获得授权收入约0.99亿元,其余部分预计在2024-2026年确认。
- 2023年公司毛利率回升至77.90%,期间费用率大幅下滑,净利率从2021年的-0.18%提升至2023年的27.94%,盈利能力显著增强。
上市产品:益赛普销售企稳回升,赛普汀/健尼哌快速放量
- 公司目前拥有益赛普、赛普汀、健尼哌3款上市产品,分别布局自身免疫类疾病、肿瘤、抗排斥3个适应症领域。益赛普和赛普汀已纳入国家医保目录。
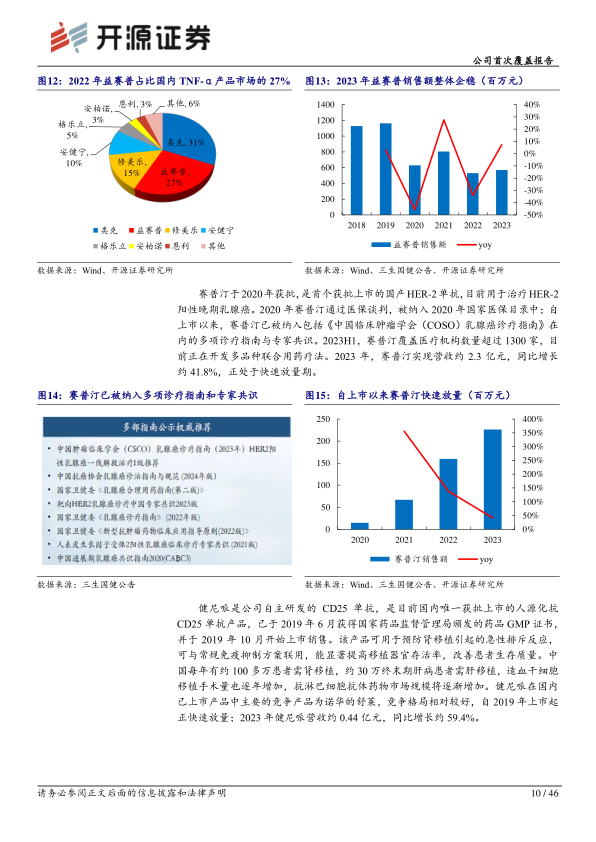
- 益赛普: 2005年上市,是中国风湿病领域首个肿瘤坏死因子(TNF-α)抑制剂,获批类风湿性关节炎、强直性脊柱炎和银屑病3个适应症。2022年国内TNF-α类产品市占率约27%。2023年销售额约5.7亿元,同比增长10.5%,销量稳中有升。
- 赛普汀: 2020年获批,首个获批上市的国产HER-2单抗,用于治疗HER-2阳性晚期乳腺癌。2020年纳入国家医保目录,并被纳入多项诊疗指南。2023年实现营收约2.3亿元,同比增长约41.8%,处于快速放量期。
- 健尼哌: 2019年上市,国内唯一获批上市的人源化抗CD25单抗产品,用于预防肾移植后急性排斥反应。国内肾移植、肝移植及造血干细胞移植手术量逐年增加,市场规模将扩大。2023年营收约0.44亿元,同比增长约59.4%,正快速放量。
在研管线:核心管线均已进入III期临床,整体疗效优异
SSGJ-608(IL-17A):针对斑块状银屑病已达到III期主要临床终点
银屑病(Ps):国内市场患者基数较大,生物药管线布局丰富
- 银屑病是一种慢性、复发性、炎症性、系统性疾病,中国患者数量预计从2018年的约656万人缓慢上升至2030年的约680万人。
- 国内银屑病生物药市场份额快速增加,预计从2018年的约3460万美元增长至2030年的约56.45亿美元,占比预计从5.73%提升至56.77%。
- 斑块状银屑病约占所有银屑病病例的80%-90%。中重度患者主要采用系统性治疗,包括传统小分子药物、生物制剂与小分子靶向药物,其中生物制剂和靶向药物因起效快、疗效突出而日益受到认可。
- 国内已有多款针对银屑病治疗的生物药获批上市,主要为海外大药企产品,靶点覆盖TNF-α、IL12/23、IL-17A、IL-23A等。国产生物制剂中,智翔金泰的赛立奇单抗(IL-17A)、恒瑞医药的夫那奇珠单抗(IL-17A)与康方生物的依若奇单抗(IL-12/23)已进入NDA申报阶段。
IL-17A靶点拥有诞生大单品的潜力,司库奇尤单抗国内快速放量
- IL-17A是促炎细胞因子,通过激活下游通路引发炎症反应,IL-17A单抗能阻断此通路,治疗斑块状银屑病等自身免疫疾病。
- 诺华的司库奇尤单抗(IL-17A单抗)2014年上市,2023年全球销售额达49.80亿美元,同比增长1.48%。
- 司库奇尤单抗在国内已获批银屑病、强直性脊柱炎与银屑病关节炎3个适应症,2023年国内销售额约62.9亿元,同比增长96.0%,市场快速放量。
SSGJ-608有望成为第三款上市的国产IL-17A靶向药物
- 三生国健自主研发的SSGJ-608(IL-17A单抗)针对斑块状银屑病已于2023年12月达到全部疗效终点,针对强直性脊柱炎与放射学阴性中轴型脊柱关节炎适应症已于2024年3月开启II期临床。
- 国内IL-17A靶点管线竞争激烈,已上市产品为诺华司库奇尤单抗和礼来依奇珠单抗。国产进度最快的是智翔金泰赛立奇单抗和恒瑞医药夫那奇珠单抗,已进入NDA阶段。
- SSGJ-608预计将成为第三款上市的国产IL-17A靶向药物。
- 针对银屑病,IL-17A靶点整体疗效优异,PASI 75、PASI 90、PASI 100等指标表现良好。
- SSGJ-608在中重度银屑病II期临床中,给药2-4周即起效,各剂量组在PASI 75、PASI 90、PASI 100等指标上显著优于安慰剂组。非头对头临床结果显示,SSGJ-608疗效和安全性优于同靶点上市产品。
SSGJ-611(IL-4R):对标大单品达必妥,国内进度整体靠前
- 过敏类疾病患者基数庞大,主要由2型免疫通路失衡诱发,生物学机制清晰。全球范围内针对过敏类疾病的靶向药物相对较少,生物制剂渗透率较低,发展潜力巨大。
- IL-4是2型免疫通路核心细胞因子,目前针对IL-4R靶点仅有一款药物获批上市(度普利尤单抗),国内多款药物处于在研阶段。
特应性皮炎(AD):患者基数大,达必妥放量推动生物药渗透率快速提升
- 特应性皮炎患者基数大,2021年全球约6.70亿人,预计2030年约7.56亿人。2022年国内中重度患者约1950万人,预计2030年约2190万人。
- 国内特应性皮炎药品市场规模逐年提升,2022年达9.67亿美元,预计2030年达70.72亿美元,CAGR达28.2%。中重度治疗药品占比高,预计从62.0%提升至77.0%。
- 生物制剂渗透率预计快速增加,从2022年的28.2%提升至2030年的77.5%。
- 特应性皮炎治疗采用阶梯式方案,中重度患者新型治疗手段包括IL-4、IL-5、IL-13等细胞因子及其受体的生物制剂,以及JAK抑制剂和PDE-4抑制剂等小分子药物。
- 国内已上市特应性皮炎药物以化药为主,如PDE-4靶向的克立硼罗和JAK1靶向的乌帕替尼。生物制剂中,靶向IL-4R的度普利尤单抗于2023年获批上市,2023年全球销售额约116亿美元。
- NDA申报阶段有恒瑞的艾玛昔替尼(JAK1)和康诺亚的司普奇拜单抗(IL-4R)。III期临床以JAK抑制剂和IL-4R为主,三生国健的IL-4R单抗SSGJ-611进度较快。
慢性鼻窦炎伴鼻息肉(CRSwNP):国内暂无上市药物,生物药成研发热门
- CRSwNP患者基数大,2021年全球约2.67亿人,预计2030年约3.11亿人。2022年国内患者超2000万人,预计2030年约2200万人。
- 国内CRSwNP药品市场规模逐年提升,2022年达1.42亿美元,预计2030年达6.33亿美元,CAGR达20.6%。
- CRSwNP临床治疗方案包括鼻用糖皮质激素、口服皮质类固醇和内镜鼻窦手术。生物制剂(IL-4R、IL-5和IgE靶点)为治疗提供了新选择,被证实更有效和安全。
- 国内外针对CRSwNP布局的管线中生物药占绝对优势,IL-4R、IL-5与IL-5R是热门靶点。
- 境外已上市生物制剂有度普利尤单抗(IL-4R)、奥玛珠单抗(IgE)和美泊利珠单抗(IL-5)。国内目前尚无治疗CRSwNP的生物制剂获批上市,6款新药处于III期临床,康诺亚的司普奇拜单抗(IL-4R)已于2023年12月达到主要临床终点,保持国内领先地位。
慢性阻塞性肺疾病(COPD):患者基数庞大,国内暂无生物药获批
- COPD患者基数大,2019年全球约4.57亿人,预计2024年约5.28亿人。2019年国内患者约1.04亿人,预计2024年约1.08亿人。
- 国内临床主要药物包括支气管舒张剂与吸入性糖皮质激素,但现有方案以缓解症状为主,患者依从性差。
- IL-4R、IL-5、IL-33靶点药物有望通过抑制2型免疫通路炎症反应,为COPD带来全新治疗方式。
- 海内外针对COPD治疗的上市药物均为化药,目前尚无生物制剂获批上市。
- 在研管线中,赛诺菲的度普利尤单抗(IL-4R)已于2023年11月申请上市。SSGJ-611针对COPD已于2023年10月进入II期临床。
IL-4R是2型免疫通路关键细胞因子受体,拥有诞生大单品的潜力
- IL-4与IL-13是2型免疫通路关键细胞因子,IL-4R靶向单抗能同时阻断IL-4与IL-13两条通路,对Th2细胞及下游嗜酸性粒细胞、肥大细胞、嗜碱性粒细胞增殖具有较好抑制作用。
- IL-4R单抗在特应性皮炎、CRSwNP、哮喘领域均具有较好临床疗效,市场潜力巨大。
- 2023年全球/中国IL-4R靶点药物市场规模预计分别达98/3亿美元,预计2030年将分别达287/41亿美元,国内市场CAGR达44.7%,预计快速放量。
- 度普利尤单抗(IL-4R单抗)是目前唯一获批上市的IL-4R单抗,2023年全球销售额约116亿美元,同比增长32.74%。国内市场2023年销售额约31.0亿元,同比增长136.5%,处于快速放量阶段。
SSGJ-611:国内进度靠前的IL-4R靶点单抗,临床疗效整体优异
- SSGJ-611是三生国健自主研发的IL-4R单抗,国内整体进度领先。
- 针对成人中重度AD已于2023年12月进入III期临床,青少年AD已于2023年12月获批IND并进入II期临床。
- 针对CRSwNP适应症于2024年1月完成II期患者招募;针对慢性阻塞性肺气肿于2023年12月完成II期首例患者入组。
- 国内IL-4R靶点管线竞争格局较好,康诺亚的司普奇拜单抗特应性皮炎适应症已于2023年12月申报NDA。三生国健、智翔金泰与麦济生物的IL-4R单抗均在2023年下半年进入III期临床。
- IL-4R靶点药物在治疗中重度特应性皮炎中疗效好且安全性佳,EASI-75指标扣除安慰剂背景后,IL-4R表现优异。
- 针对CRSwNP,IL-4R靶点药物疗效明显优于其他靶点药物,能显著降低鼻息肉评分(NPS)。
- SSGJ-611 II期临床研究结果显示,16周时各剂量组在IGA0/1和EASI-75等指标上显著优于安慰剂组,且在EASI-75和缓解瘙痒方面应答有高于已上市同靶点药物的趋势,展现出较好的临床疗效。
SSGJ-610(IL-5):国内首个进入III期临床的国产IL-5单抗
嗜酸性粒细胞哮喘(EA):严重哮喘分型,国内仅有一款生物药获批
- 嗜酸性粒细胞哮喘(EA)是一类重度哮喘表型,由嗜酸性粒细胞诱发。
- 2022年全球哮喘患者约7.83亿人,预计2030年约8.60亿人。国内哮喘患者约6700万人,预计2030年约7800万人,CAGR达1.9%。
- 中国EA发病率约6.2%,按2022年数据计算,国内EA患者约415万人。
- 2022年国内哮喘药物市场规模约38亿美元,其中中重度哮喘药品规模约21亿美元(占比55.3%)。
- 哮喘治疗生物制剂渗透率仍处于较低水平(2022年仅3.5%),预计2030年将接近44.1%。
- 哮喘治疗采用阶梯式方案,重度哮喘患者可选用IgE、IL-4R与IL-5为靶点的生物制剂。
- 根据GINA指南,对于重症哮喘患者,推荐使用抗IL-5单克隆抗体和抗IL-5R单抗治疗,可减少急性发作、降低住院率、减少口服激素剂量、改善哮喘控制和肺功能。
- 国内治疗哮喘的药物主要是传统激素类化药,仅有奥玛珠单抗(IgE)、度普利尤单抗(IL-4R)和GSK的美泊利珠单抗(IL-5)3款生物药获批上市,其中美泊利珠单抗主要针对嗜酸性粒细胞哮喘。
- 三生国健的SSGJ-610(IL-5)已于2024年3月进入III期临床,处于国产厂家领先位置。
IL-5诱发嗜酸性粒细胞类疾病,靶向药美泊利珠单抗全球销售额稳健增长
- IL-5在嗜酸性粒细胞的诱导和增殖中起重要作用,可诱发嗜酸粒细胞性哮喘。
- GSK的美泊利珠单抗(IL-5单抗)自2015年获批嗜酸性粒细胞哮喘适应症以来,全球范围内已有5个适应症获批上市。
- 2023年美泊利珠单抗全球销售额约20.63亿美元,同比增长17.6%。
SSGJ-610临床疗效优异,进度处于国产厂家领先位置
- SSGJ-610是三生国健自主研发的IL-5单抗,针对嗜酸性粒细胞哮喘已于2024年1月达到II期主要临床终点,并于2024年3月开启III期临床。
- 国内IL-5靶点管线数量较少,美泊利珠单抗已上市。国产厂家中,SSGJ-610目前处于领先位置。
- SSGJ-610 II期临床结果表明,给药4-8周后开始起效,在改善FEV1和降低ACQ评分方面疗效稳定增长,且有随剂量增加的趋势。
- 非头对头临床试验结果显示,SSGJ-610疗效整体优于同靶点竞品美泊利珠单抗与瑞利珠单抗、IL-5RA产品本瑞利珠单抗。
- 安全性方面,SSGJ-610药物相关不良事件多为1-2级,无>3级药物相关不良事件,整体安全性和耐受性良好。
SSGJ-613(IL-1β):凭借风湿科渠道资源,上市后有望快速放量
痛风性关节炎:国内患者基数较大,暂无生物制品获批上市
- 痛风性关节炎患者人数逐年持续增长,2026年全球/中国痛风性关节炎患者人数预计分别约2.86/0.47亿人,CAGR约5.0%/5.7%。
- 痛风性关节炎自然病程分为无症状高尿酸血症期、急性发作期、发作间歇期和慢性痛风性关节炎期,需根据症状发展程度采用不同治疗方案。
- 急性期治疗一线药物包括秋水仙碱、非甾体抗炎药、糖皮质激素。若治疗不佳,可使用IL-1受体拮抗剂。
- 国内针对痛风性关节炎布局的管线整体较少,已上市药物以激素类化药产品为主,暂无生物制品获批上市。
- 在研管线中,长春金赛的金纳单抗针对急性期痛风性关节炎已于2024年4月申报NDA。三生国健的SSGJ-613针对急性期痛风性关节炎于2023年12月进入III期临床,整体进度领先。
IL-1β是诱发痛风的关键因子,SSGJ-613整体疗效优异进度领先
- IL-1β在痛风发作的发病机制中起重要作用,IL-1β单抗能有效阻断炎症通路,治疗痛风性关节炎。
- SSGJ-613是三生国健自主研发的IL-1β单抗,具有全新的可变区序列,与已上市同靶点产品(如Canakinumab)结合表位不同。
- 国内尚无针对IL-1β的单抗获批上市,长春金赛的金纳单抗率先于2024年4月申报NDA。
- SSGJ-613针对急性期痛风性关节炎于2024年1月完成III期首例患者入组,针对间隙期痛风性关节炎于2024年1月IND获批,整体国内进度领先。
- 凭借益赛普20余年的销售经验,公司在风湿免疫科积累了较多渠道与专家资源,可为SSGJ-613未来商业化放量提供保障。
- SSGJ-613 II期临床研究结果表明,给药6小时后即起效,200mg组72小时VAS疼痛缓解与阳性对照得宝松组类似,且疼痛改善持续下降更显著。
- 在预防痛风复发方面,SSGJ-613显著优于阳性对照组,200mg与300mg组第12周新的痛风急性发作受试比例分别为17.2%、14.4%,显著低于阳性激素对照组51.6%。
- 安全性方面,SSGJ-613整体安全性和耐受性良好,多数不良事件为1-2级,无药物相关SAE,发生率低于激素对照组。
盈利预测与投资建议
关键假设
- 公司核心上市产品益赛普、赛普汀与健尼哌销售额预计稳健增长,2024-2026年收入增速分别为13.85%、20.25%与16.48%;毛利率预计维持在75.00%。
- CDMO业务非核心增长点,规模预计逐渐缩小,2024-2026年收入增速分别为-20.00%、-10.00%、-10.00%;毛利率预计维持在35.00%。
- 公司非自免管线授权收入预计在2024-2025年分别确认2.0亿元和1.3亿元,毛利率为100%。
- 公司在研管线预计在2025-2026年陆续上市,分别贡献0.12亿元和2.25亿元收入;毛利率预计稳定在90.00%。
- 随着收入规模增加,销售、管理、研发及财务费用率有望稳步下降。
盈利预测与估值
- 三生国健作为国内首批专注于抗体药物研发的创新型生物医药企业,战略聚焦自免领域,现有
-

公司信息更新报告:收入提升利润高增,产业投资多层次布局
-

北交所信息更新:从单一磺胺到特色赛道,“原料药+人用药赛道拓展”双轮驱动新成长
-

收入高增验证景气度,并购扩产加速破局
-

公司信息更新报告:2026Q1业绩稳健增长,期待营销改革落地
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送