-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

始于创新、强于执行力,血液瘤及自免领域管线双开花
始于创新、强于执行力,血液瘤及自免领域管线双开花
-
下载次数:
896 次
-
发布机构:
平安证券股份有限公司
-
发布日期:
2024-03-21
-
页数:
38页
诺诚健华(688428)
平安观点:
立足于研发创新,奥布替尼血液瘤及自免领域双开花。公司创始管理团队业内经验丰富,拥有国际创新视野,洞悉行业痛点需求。目前已有两款产品商业化,其中奥布替尼国内已获批3个适应症,2020年12月获批2LMCL和2L CLL/SLL适应症,为国内第三款获批上市的BTK抑制剂;2021年底进入国家医保目录;2023年4月国内新增获批2L MZL。公司持续围绕奥布替尼布局血液肿瘤及自免多项适应症,深入挖掘产品价值:(1)在血液瘤方面,国内1L CLL/SLL临床Ⅲ期已完成入组,预计2024年递交NDA;美国2L MCL同样完成入组,预计2024在美递交NDA;1L MCD亚型DLBCL临床Ⅲ期中。(2)在自免领域,预计2024年完成ITP临床Ⅲ期入组;治疗SLE临床Ⅱb入组中,预计2024年入组完成;海外MS目前临床Ⅱ期完成。
商业化执行团队高效,秉承成本敏感、执行力强的企业精神。奥布替尼2021实现销售收入2.15亿元,2022年进入医保后产品快速放量,实现收入5.66亿元,同比增长164%,预计2023年药品实现销售收入约6.7亿元,同比增长18%以上。从公司销售团队搭建来看,预计2023年营销人员200人以上,人均单产达300万元左右。公司商业化战略布局、人均产出指标等均凸显出高效性及强执行力。
两款口服高选择性TYK2抑制剂,拓宽公司自免领域产品布局。(1)ICP-332口服TYK2/JH1抑制剂,开发探索用于治疗特应性皮炎AD。2023年底ICP-332宣布治疗AD临床Ⅱ期试验达到主要终点,80mg QD给药整体EASI改善78.2%,药物起效快且持续,此外安全性上ICP-332无黑框警告风险。公司计划于2024年启动ICP-332临床Ⅲ期研究,此外预计2024年会针对第二个自免适应症开展临床Ⅱ期,并在美国开展临床试验;(2)ICP-488从结合构象上与ICP-332的区别在于,ICP-488选择性结合JH2假激酶结构域,对JAK1-3无抑制效果,目前正在开展国内银屑病临床Ⅱ期研究中,预计2024年完成Ⅱ期入组。
投资建议:2024年公司将有多款产品国内申报NDA,其中奥布替尼1L CLL/SLL、Tafasitamab2L DLBCL、ICP-723(第二代TRK)预计2024年国内递交NDA,此外2024年多个管线进入关键性Ⅲ期,其中奥布替尼治疗ITP预计2024年完成国内Ⅲ期入组,ICP-332治疗AD国内启动Ⅲ期。预计2023-2025年公司收入主要还是来自奥布替尼的放量,整体年度实现营收分别为7.2/8.78/12.61亿元。针对公司中后期管线DCF估值,对应公司市值205.8亿元。公司创新力强、执行力强、商业团队高效高质,未来陆续多个产品逐步进入销售或研发收获期,首次覆盖给予“推荐”评级。
风险提示:1)药品审批不及预期:公司创新产品可能存在获批时间延迟。2)新药上市放量不及预期:公司创新产品上市后各个节点是否顺利推进对于公司产品销售放量具有显著影响。3)国家政策的影响:医保谈判政策可能调整,从而影响公司创新药销售。
中心思想
创新驱动与高效执行力
诺诚健华(688428.SH)作为一家立足于研发创新的生物医药公司,凭借其经验丰富的创始管理团队和国际化的创新视野,在血液瘤及自身免疫疾病领域展现出强大的研发实力和高效的商业化执行力。公司核心产品奥布替尼(Orelabrutinib)已在国内获批多项适应症并进入国家医保目录,销售额实现快速增长,同时在自身免疫疾病领域也取得了显著的临床进展。
奥布替尼核心地位与多元管线布局
奥布替尼不仅在血液瘤治疗中展现出优异的疗效和安全性,更通过独特的分子结构设计实现了同类最佳的激酶选择性,并积极拓展自身免疫疾病适应症。此外,公司还拥有包括Tafasitamab、ICP-332、ICP-488、ICP-723和ICP-192在内的丰富且多元化的临床管线,覆盖血液瘤、自身免疫和实体瘤等多个治疗领域。预计2024年将迎来多个关键性临床里程碑和NDA申报,为公司未来的持续增长奠定坚实基础。
主要内容
核心产品市场表现与管线深度分析
一、业绩业务概览
诺诚健华于2015年由崔霁松博士和施一公院士联合创立,专注于恶性肿瘤及自身免疫性疾病药物研发,并成功在香港交易所(2020年)和科创板(2022年)上市,科创板募资总额超过29亿元。公司首款商业化产品奥布替尼于2020年12月在国内获批上市,并于2021年底进入国家医保目录,2023年4月新增获批2L MZL适应症。坦昔妥单抗(Tafasitamab)治疗方案于2022年底在香港获批上市。公司战略重心在于开发潜在同类最佳/首创靶向疗法,旨在成为血液瘤领域的领导者以及自身免疫和实体瘤领域的有力竞争者。
截至2023年三季度,公司股权结构相对分散,第一大股东为高瓴资本旗下HHLR及其一致行动人,合计持股11.83%。公司管理团队具备丰富的国际创新视野和行业洞察力,成员拥有辉瑞、GSK、BMS等大型跨国药企的资深工作经验。公司已构建从源头创新、临床开发、生产到商业化的全产业链平台,在北京、南京设有研发基地,并在广州建有5万平方米的生产基地(目标产能每年10亿片,预计2024年完成3万平方米二期扩建)。
公司收入主要来源于奥布替尼的销售放量。2021年奥布替尼销售收入达2.15亿元,同年因奥布替尼MS适应症授权确认Biogen首付款7.76亿元。2022年,奥布替尼产品销售额达5.66亿元,同比增长163.6%。截至2023年前三季度,公司实现收入5.37亿元,同比增长21.7%。预计2023年全年药品销售收入约6.7亿元,同比增长18%以上。公司在手现金充沛,截至2023年三季度末现金及现金等价物达85.8亿元,为研发管线项目进展提供充足保障。
2024年,公司预计将迎来多个重要的管线里程碑:
- 肿瘤领域: 奥布替尼一线治疗CLL/SLL国内递交NDA;奥布替尼二线治疗MCL美国递交NDA;Tafasitamab治疗DLBCL预计2024年上半年国内递交NDA;ICP-723(第二代Pan-TRK抑制剂)治疗NTRK基因融合阳性实体瘤预计2024年底国内递交NDA;ICP-248(BCL2)国内单药治疗NHL临床Ⅰ期数据读出,并在美国开展临床Ⅰ期,同时递交与奥布替尼联用一线治疗CLL/SLL的IND。
- 自免领域: 奥布替尼治疗ITP完成临床Ⅲ期入组;奥布替尼治疗SLE完成临床Ⅱb期入组;奥布替尼海外治疗MS待观察推进入临床Ⅲ期;ICP-332(TYK2 JH1抑制剂)治疗AD国内启动临床Ⅲ期,并开启第二个自免适应症临床Ⅱ期及在美国开展临床试验;ICP-488(TYK2变构抑制剂)治疗银屑病完成临床Ⅱ期入组。
二、奥布替尼:核心产品深度分析
奥布替尼是公司核心产品,其BTK靶点在B细胞淋巴瘤和自身免疫疾病中均取得显著进展。BTK是B细胞受体(BCR)信号通路中的关键激酶,通过靶向BTK可调控BCR信号传导,治疗多种B细胞淋巴瘤。此外,BTK在巨噬细胞Fc受体信号通路中也发挥作用,使其成为治疗自身免疫疾病的新靶点。
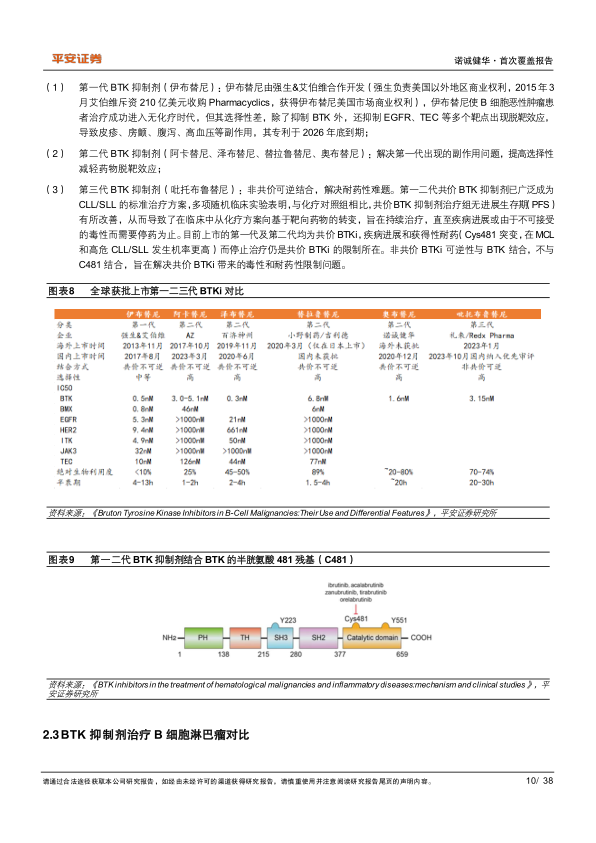
BTK抑制剂的代际演进与市场竞争:
- 第一代(伊布替尼): 开启B细胞恶性肿瘤无化疗时代,但选择性差,存在脱靶效应,导致皮疹、房颤、腹泻、高血压等副作用。
- 第二代(阿卡替尼、泽布替尼、替拉鲁替尼、奥布替尼): 通过结构优化提高选择性,减轻脱靶效应。
- 第三代(吡托布鲁替尼): 非共价可逆结合,旨在解决第一二代共价BTKi的耐药性问题(如Cys481突变)。
在国内市场,伊布替尼、泽布替尼和奥布替尼均已进入医保。奥布替尼在年治疗费用上具有价格优势,相较伊布替尼更低,略低于泽布替尼
-

GLP-1药物未来方向标:减脂增肌、口服剂型、超长效制剂赛道掘金
-

医疗设备招投标数据跟踪:设备更新不断深化,县域医共体持续发力
-

医疗设备招投标数据跟踪:招投标持续恢复,国产替代趋势显著
-

生物医药行业:国产新药闪耀ASCO 2025,关注相关企业投资机遇
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






最新报告
- 医药生物行业周报(26年第23周):ASCO会议顺利闭幕,关注具备高质量创新能力的公司
- 基础化工行业研究:R22、煤焦油等涨幅居前,建议关注进口替代、纯内需、高股息等方向
- 医疗器械行业2026年中期策略:紧扣出海创新,掘金器械复苏
- AI系列深度(十一):高频高速覆铜板有望拉动高性能硅微粉需求持续增长
- 基础化工行业周报:硫磺价格持续上涨,巨化股份超纯PFA量产
- 2025年化学制药行业经济运行报告
- 2025中医药市场研究报告
- EGFR×HER3双抗ADC iza-bren硕果频出,多管线驱动成长
- 服务价格落地,一次性高值耗材推广加速
- 北交所信息更新:NL003塞多明基注射液获批上市,填补我国CLTI临床对因治疗空白
对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送