-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

2023年年报点评:IL-17A单抗获批在即,在研管线快速推进
2023年年报点评:IL-17A单抗获批在即,在研管线快速推进
-
下载次数:
2742 次
-
发布机构:
西南证券股份有限公司
-
发布日期:
2024-05-06
-
页数:
6页
智翔金泰(688443)
投资要点
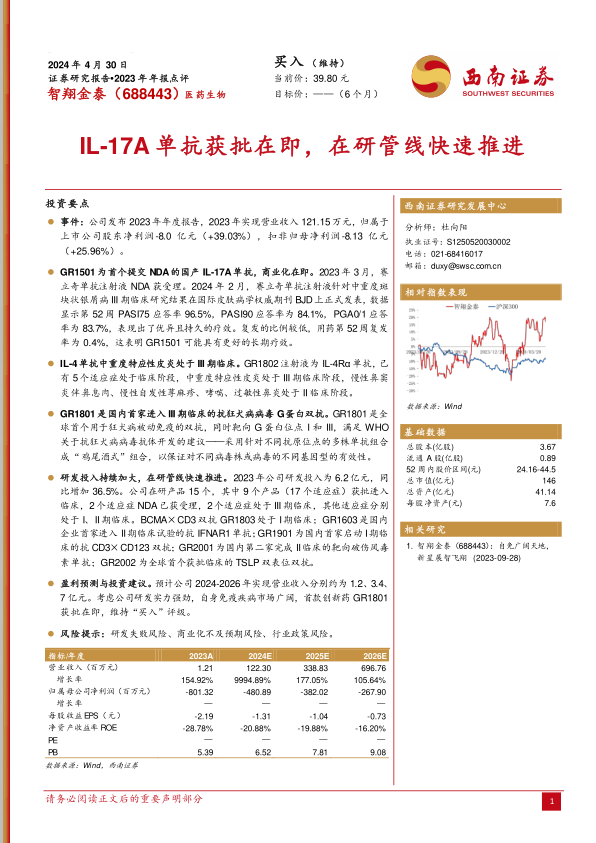
事件:公司发布2023年年度报告,2023年实现营业收入121.15万元,归属于上市公司股东净利润-8.0亿元(+39.03%),扣非归母净利润-8.13亿元(+25.96%)。
GR1501为首个提交NDA的国产IL-17A单抗,商业化在即。2023年3月,赛立奇单抗注射液NDA获受理。2024年2月,赛立奇单抗注射液针对中重度斑块状银屑病III期临床研究结果在国际皮肤病学权威期刊BJD上正式发表,数据显示第52周PASI75应答率96.5%,PASI90应答率为84.1%,PGA0/1应答率为83.7%,表现出了优异且持久的疗效。复发的比例较低,用药第52周复发率为0.4%,这表明GR1501可能具有更好的长期疗效。
IL-4单抗中重度特应性皮炎处于III期临床。GR1802注射液为IL-4Rα单抗,已有5个适应症处于临床阶段,中重度特应性皮炎处于III期临床阶段,慢性鼻窦炎伴鼻息肉、慢性自发性荨麻疹、哮喘、过敏性鼻炎处于II临床阶段。
GR1801是国内首家进入III期临床的抗狂犬病病毒G蛋白双抗。GR1801是全球首个用于狂犬病被动免疫的双抗,同时靶向G蛋白位点I和III,满足WHO关于抗狂犬病病毒抗体开发的建议——采用针对不同抗原位点的多株单抗组合成“鸡尾酒式”组合,以保证对不同病毒株或病毒的不同基因型的有效性。
研发投入持续加大,在研管线快速推进。2023年公司研发投入为6.2亿元,同比增加36.5%。公司在研产品15个,其中9个产品(17个适应症)获批进入临床,2个适应症NDA已获受理,2个适应症处于III期临床,其他适应症分别处于I、II期临床。BCMA×CD3双抗GR1803处于I期临床;GR1603是国内企业首家进入II期临床试验的抗IFNAR1单抗;GR1901为国内首家启动I期临床的抗CD3×CD123双抗;GR2001为国内第二家完成II临床的靶向破伤风毒素单抗;GR2002为全球首个获批临床的TSLP双表位双抗。
盈利预测与投资建议。预计公司2024-2026年实现营业收入分别约为1.2、3.4、7亿元。考虑公司研发实力强劲,自身免疫疾病市场广阔,首款创新药GR1801获批在即,维持“买入”评级。
风险提示:研发失败风险、商业化不及预期风险、行业政策风险。
中心思想
- 国产IL-17A单抗商业化在即: 智翔金泰的GR1501作为首个提交NDA的国产IL-17A单抗,其III期临床数据表现优异且持久,有望迅速占领市场。
- 在研管线快速推进: 公司研发投入持续加大,多个在研产品进入临床阶段,尤其是在狂犬病、特应性皮炎等领域,具有显著的先发优势和市场潜力。
主要内容
公司业绩与财务表现
- 年度业绩概况: 智翔金泰2023年实现营业收入121.15万元,归属于上市公司股东净利润为-8.0亿元,同比增长39.03%,扣非归母净利润-8.13亿元,同比增长25.96%。
- 研发投入增加: 2023年公司研发投入为6.2亿元,同比增长36.5%,显示公司持续加大研发力度,推动管线快速发展。
核心产品与研发管线
-
GR1501(IL-17A单抗):
- NDA已获受理,商业化在即。
- III期临床研究结果在BJD上正式发表,数据显示第52周PASI75应答率96.5%,PASI90应答率为84.1%,PGA0/1应答率为83.7%,疗效优异且持久,复发率低。
-
GR1802(IL-4Rα单抗):
- 针对中重度特应性皮炎的III期临床正在进行中。
- 针对慢性鼻窦炎伴鼻息肉、慢性自发性荨麻疹、哮喘、过敏性鼻炎的II期临床正在进行中。
-
GR1801(抗狂犬病病毒G蛋白双抗):
- 国内首家进入III期临床的抗狂犬病病毒G蛋白双抗。
- 全球首个用于狂犬病被动免疫的双抗,同时靶向G蛋白位点I和III。
-
其他在研管线:
- BCMA×CD3双抗GR1803处于I期临床。
- GR1603是国内企业首家进入II期临床试验的抗IFNAR1单抗。
- GR1901为国内首家启动I期临床的抗CD3×CD123双抗。
- GR2001为国内第二家完成II临床的靶向破伤风毒素单抗。
- GR2002为全球首个获批临床的TSLP双表位双抗。
盈利预测与投资建议
- 盈利预测: 预计公司2024-2026年实现营业收入分别约为1.2亿元、3.4亿元、7亿元。
- 投资建议: 考虑公司研发实力强劲,自身免疫疾病市场广阔,首款创新药GR1801获批在即,维持“买入”评级。
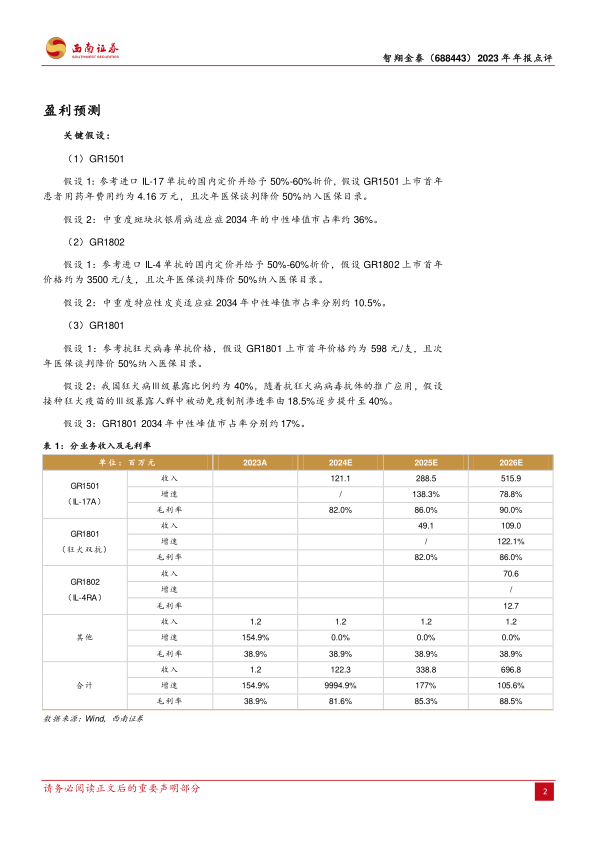
盈利预测关键假设
-
GR1501(IL-17A单抗)
- 假设1:上市首年患者用药年费用约为4.16万元,次年医保谈判降价50%纳入医保目录。
- 假设2:中重度斑块状银屑病适应症2034年的中性峰值市占率约36%。
-
GR1802(IL-4单抗)
- 假设1:上市首年价格约为3500元/支,次年医保谈判降价50%纳入医保目录。
- 假设2:中重度特应性皮炎适应症2034年中性峰值市占率分别约10.5%。
-
GR1801(狂犬双抗)
- 假设1:上市首年价格约为598元/支,次年医保谈判降价50%纳入医保目录。
- 假设2:我国狂犬病Ⅲ级暴露比例约为40%,随着抗狂犬病病毒抗体的推广应用,假设接种狂犬疫苗的Ⅲ级暴露人群中被动免疫制剂渗透率由18.5%逐步提升至40%。
- 假设3:GR1801 2034年中性峰值市占率分别约17%。
风险提示
- 研发失败风险
- 商业化不及预期风险
- 行业政策风险
总结
智翔金泰凭借其在研管线的快速推进和首个国产IL-17A单抗的商业化前景,展现出强大的市场潜力。公司在自身免疫疾病和狂犬病等领域具有显著的竞争优势。维持“买入”评级,但需关注研发、商业化和政策风险。
-

创新药专题:中国之声闪耀2026ASCO
-

医药行业周报:BD合作持续推进,ASCO年会正式开幕
-

医药行业周报:ASCO年会倒计时
-

医药行业周报:百亿BD再现,关注5月末ASCO会议
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送