-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

Ociperlimab在NSCLC具有临床获益,公司多项里程碑事件值得期待
Ociperlimab在NSCLC具有临床获益,公司多项里程碑事件值得期待
-
下载次数:
1743 次
-
发布机构:
天风证券股份有限公司
-
发布日期:
2022-09-05
-
页数:
3页
百济神州(688235)
事件:
公司于近期的2022年WCLC大会上,公布关于TIGIT单抗ociperlimab联用替雷利珠单抗,治疗一线PD-L1阳性转移性NSCLC患者的AdvanTIG-105试验1b期剂量扩展数据。
Ociperlimab用于治疗NSCLC的I期数据公布,具有临床获益
截至2022年4月5日,AdvanTIG-105试验共入组40人。中位随访时间23周时,疗效可评估的39名患者总体ORR(未经确认)达53.8%,PD-L1高表达组(PD-L1TC≥50%)ORR为71.4%,1-49%低表达组ORR为44.0%。横向对比罗氏tiragolumab联用阿特珠单抗II期CITYSCAPE试验结果,总体、PD-L1高表达及低表达组ORR分别为38.8%、69.0%及15.8%;而帕博利珠单抗单药治疗的总体及PD-L1高表达人群ORR分别为27%及39%。我们预计有望经确认后ociperlimab在各个组中ORR均高于罗氏tiragolumab竞品及PD-1单药方案。此外AdvanTIG-105试验总体DCR达89.7%,mPFS5.4月,PD-L1高表达组(PD-L1TC≥50%)mPFS为5.6月,1-49%低表达组mPFS为5.2月,具有临床获益。三级以上TRAE发生率10.0%,非头对头对比tiragolumab22.4%及帕博利珠单抗18%,安全性更佳。
实体瘤领域广泛布局,ociperlimab将开展新的关键临床试验
Ociperlimab预计将于年内公布AdvanTIG-105试验针对多种实体瘤队列数据,并开展新的关键性临床试验。替雷利珠单抗近期一线G/GEJ腺癌及一线ESCC两项适应症上市申请获得NMPA受理;一线HCC适应症III期临床试验头对头对比索拉非尼体现在总生存期上的非劣效性,具体数据将于近期公布;一线GC、一线/局部ESCC及一线HCC适应症上市申请将在2023年向FDA递交。此外公司将与维立志博合作,在今年启动LBL-007(LAG-3)、泽布替尼、surzebiclimab(TIM3)联合疗法临床试验的患者给药。
血液瘤多项里程碑近期达成,泽布替尼CLL适应症即将在美获批
血液瘤基石性品种泽布替尼今年有望在十余个新市场获批上市,III期ALPINE试验PFS最终分析数据预计于年内公布;CLL/SLL适应症全线有望于2023年1月在美获批。2021年美国新发CLL病例超2.1万例,患者基数大,若该适应症顺利获批,有望大幅提升销售额。BGB-11417(BCL-2抑制剂)近期披露多项I期数据体现临床获益,将在今年启动关键临床试验并公布更多I期试验数据。
盈利预测与投资评级
我们预计公司2022至2024年营业收入为96.65亿、127.84亿、170.24亿元,实现归母净利润-78.96亿、-66.73亿、-36.89亿元人民币。维持“买入”评级。
风险提示:研发进度不及预期风险,国际环境恶化风险,授权合作风险
中心思想
本报告主要分析了百济神州在研药物 Ociperlimab 联合替雷利珠单抗治疗一线 PD-L1 阳性转移性 NSCLC 患者的临床数据,并结合公司其他研发管线进展和里程碑事件,维持“买入”评级。
- Ociperlimab 临床数据亮眼: Ociperlimab 联合疗法在 NSCLC 治疗中显示出临床获益,尤其在高 PD-L1 表达患者中 ORR 较高,且安全性良好。
- 多项里程碑事件值得期待: 公司在实体瘤和血液瘤领域均有多项药物处于临床后期或即将获批上市,未来业绩增长可期。
主要内容
Ociperlimab 在 NSCLC 治疗中具有临床获益
- AdvanTIG-105 试验数据分析: 截至 2022 年 4 月 5 日,AdvanTIG-105 试验共入组 40 人,疗效可评估的 39 名患者总体 ORR 达 53.8%,PD-L1 高表达组(PD-L1 TC≥50%)ORR 为 71.4%。
- 竞品对比与安全性优势: Ociperlimab 在各组中的 ORR 均高于罗氏 tiragolumab 竞品及 PD-1 单药方案,且三级以上 TRAE 发生率低于竞品,安全性更佳。
实体瘤领域广泛布局,新试验值得期待
Ociperlimab 预计将于年内公布 AdvanTIG-105 试验针对多种实体瘤队列数据,并开展新的关键性临床试验。替雷利珠单抗近期一线 G/GEJ 腺癌及一线 ESCC 两项适应症上市申请获得 NMPA 受理;一线 HCC 适应症 III 期临床试验头对头对比索拉非尼体现在总生存期上的非劣效性,具体数据将于近期公布;一线 GC、一线/局部 ESCC 及一线 HCC 适应症上市申请将在 2023 年向 FDA 递交。此外公司将与维立志博合作,在今年启动 LBL-007(LAG-3)、泽布替尼、surzebiclimab(TIM3)联合疗法临床试验的患者给药。
血液瘤多项里程碑近期达成,泽布替尼 CLL 适应症即将在美获批
血液瘤基石性品种泽布替尼今年有望在十余个新市场获批上市,III 期 ALPINE 试验 PFS 最终分析数据预计于年内公布;CLL/SLL 适应症全线有望于 2023 年 1 月在美获批。2021 年美国新发 CLL 病例超 2.1 万例,患者基数大,若该适应症顺利获批,有望大幅提升销售额。BGB-11417(BCL-2 抑制剂)近期披露多项 I 期数据体现临床获益,将在今年启动关键临床试验并公布更多 I 期试验数据。
盈利预测与投资评级
我们预计公司 2022 至 2024 年营业收入为 96.65 亿、127.84 亿、170.24 亿元,实现归母净利润-78.96 亿、-66.73 亿、-36.89 亿元人民币。维持“买入”评级。
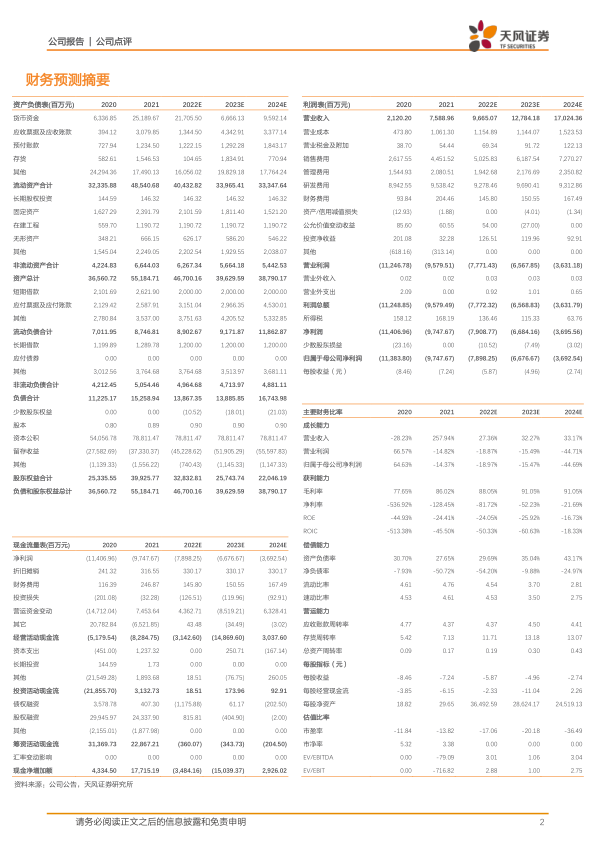
财务数据和估值
- 营业收入: 2022E 为 96.65 亿元,同比增长 27.36%;预计 2023E 和 2024E 分别增长 32.27% 和 33.17%。
- 净利润: 持续亏损,但亏损额逐年收窄,预计 2024 年净利润为 -36.89 亿元。
- 市盈率 (P/E): 持续为负,反映公司盈利能力尚未显现。
风险提示
研发进度不及预期风险,国际环境恶化风险,授权合作风险。
总结
本报告通过对百济神州 Ociperlimab 临床试验数据、其他在研管线进展以及财务数据的分析,认为公司在 NSCLC 治疗领域具有潜力,且在实体瘤和血液瘤领域均有多项里程碑事件值得期待。维持“买入”评级,但同时也提示了研发、国际环境和授权合作等方面的风险。
-

天风医药细分领域分析与展望(2025H1):体外诊断行业及个股2025半年度回顾与展望
-

国内短期承压,海外市场呈现良好增长态势
-

基础化工行业研究周报:国家发改委,支持石化化工行业节能降碳改造,煤化工项目低碳化改造,双氧水、硫酸铵价格上涨
-

化工行业运行指标跟踪:2025年8-9月数据
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






最新报告
- 医药生物行业周报(26年第23周):ASCO会议顺利闭幕,关注具备高质量创新能力的公司
- 基础化工行业研究:R22、煤焦油等涨幅居前,建议关注进口替代、纯内需、高股息等方向
- 医疗器械行业2026年中期策略:紧扣出海创新,掘金器械复苏
- AI系列深度(十一):高频高速覆铜板有望拉动高性能硅微粉需求持续增长
- 基础化工行业周报:硫磺价格持续上涨,巨化股份超纯PFA量产
- 2025年化学制药行业经济运行报告
- 2025中医药市场研究报告
- EGFR×HER3双抗ADC iza-bren硕果频出,多管线驱动成长
- 服务价格落地,一次性高值耗材推广加速
- 北交所信息更新:NL003塞多明基注射液获批上市,填补我国CLTI临床对因治疗空白
对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送