-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

医药生物行业:2023ASCO:国产CLDN18.2创新药再露锋芒
医药生物行业:2023ASCO:国产CLDN18.2创新药再露锋芒
-
下载次数:
1197 次
-
发布机构:
国联证券股份有限公司
-
发布日期:
2023-06-09
-
页数:
7页
行业事件:
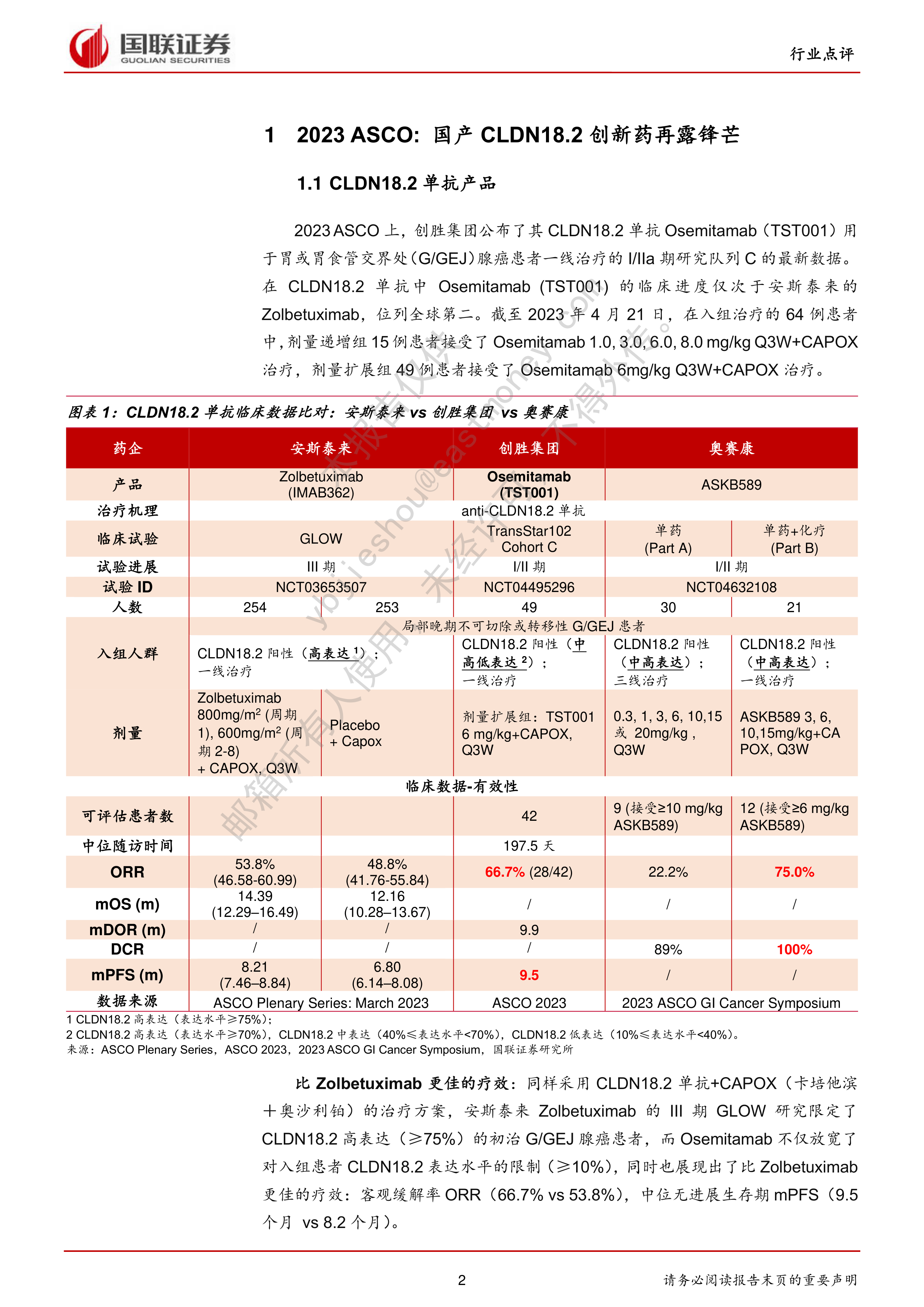
ASCO2023会议上,创胜集团公布了其CLDN18.2单抗Osemitamab(TST001)用于胃或胃食管交界处(G/GEJ)腺癌患者一线治疗的I/IIa期研究的最新数据。石药集团也首次公布了其CLDN18.2ADC产品SYSA1801治疗CLDN18.2表达晚期恶性实体瘤患者的Ⅰ期临床研究成果。两款产品在胃或胃食管交界处(G/GEJ)腺癌患者的早线/后线治疗上均展现了显著的疗效和可控的安全性,具备成为同类药物最佳的潜力。
Osemitamab在疗效和潜在获益患者群体上优势明显
不同于安斯泰来Zolbetuximab的III期GLOW研究限定了CLDN18.2高表达(≥75%)的初治G/GEJ腺癌患者,创胜集团的Osemitamab不仅放宽了对入组患者CLDN18.2表达水平的限制(≥10%),在与Zolbetuximab临床数据的非头对头比较中也展现了更佳的疗效:客观缓解率ORR(66.7%vs53.8%),中位无进展生存期mPFS(9.5个月vs8.2个月),未来有望凭借这两点优势在G/GEJ腺癌患者的早线市场竞争中实现后来居上。
SYSA1801临床进度位列全球第一梯队,潜力十足
石药集团的SYSA1801是继康诺亚的CMG901之后全球第二款公布临床数据的CLDN18.2ADC产品。SYSA1801在治疗CLDN18.2表达晚期胃癌患者的I期临床研究中展现了良好的抗肿瘤活性,ORR和DCR分别达到47.1%和62.7%,其中有1例胃癌受试者是在既往接受靶向CLDN18.2单抗治疗失败后接受SYSA1801治疗后获得PR,另有1例受试者获得了持续的缓解。同时SYSA1801也展示了较好的安全耐受性,潜力十足。
风险提示:临床试验结果不及预期;商业化合作进度不及预期;市场竞争加剧。
中心思想
本报告的核心观点是:2023年ASCO会议上,国产CLDN18.2创新药展现出显著疗效和安全性,尤其创胜集团的Osemitamab和石药集团的SYSA1801在胃或胃食管交界处(G/GEJ)腺癌治疗领域表现突出,有望在市场竞争中占据优势地位。然而,临床试验结果的不确定性、商业化合作的进展以及市场竞争的加剧仍然是潜在风险。
国产CLDN18.2创新药市场竞争格局分析
国产CLDN18.2创新药在疗效和安全性方面均展现出巨大潜力,但同时也面临激烈的市场竞争。
主要内容
本报告主要围绕2023年ASCO会议上公布的国产CLDN18.2创新药临床数据展开分析,涵盖CLDN18.2单抗产品和CLDN18.2 ADC产品两大方面。
CLDN18.2单抗产品临床数据分析
报告详细分析了创胜集团Osemitamab(TST001)和安斯泰来Zolbetuximab的临床数据,并与奥赛康ASKB589进行了比较。Osemitamab在客观缓解率(ORR)和中位无进展生存期(mPFS)方面均优于Zolbetuximab,且对CLDN18.2表达水平的限制更低,潜在获益患者群体更广。安全性方面,Osemitamab也表现良好,不良事件多为1-2级,3级不良事件发生率低于Zolbetuximab。奥赛康ASKB589的临床进度虽然落后,但其有效性和安全性数据也值得关注。
Osemitamab疗效及安全性数据解读
报告通过图表详细展示了Osemitamab在不同CLDN18.2表达水平患者中的疗效数据,并对安全性数据进行了深入分析,包括常见不良事件和严重不良事件的发生率。数据显示,Osemitamab在不同表达水平的患者中均展现出优异的治疗效果,且安全性良好。
CLDN18.2单抗产品市场竞争分析
报告对安斯泰来Zolbetuximab、创胜集团Osemitamab和奥赛康ASKB589三款CLDN18.2单抗产品的临床数据、进展阶段以及潜在市场份额进行了比较分析,指出Osemitamab凭借其疗效和安全性优势,有望在市场竞争中后来居上。
CLDN18.2 ADC产品临床数据分析
报告分析了石药集团SYSA1801的临床数据,并与科济药业CT041和康诺亚CMG901进行了比较。SYSA1801在I期临床研究中展现了良好的抗肿瘤活性,ORR和DCR分别达到47.1%和62.7%。值得关注的是,部分患者在既往靶向CLDN18.2单抗治疗失败后,使用SYSA1801仍获得疗效。安全性方面,SYSA1801也表现出较好的耐受性。报告还对科济药业的新一代CLDN18.2 CAR-T产品CT048进行了简要介绍。
SYSA1801疗效及安全性数据解读
报告对SYSA1801的临床数据进行了详细解读,包括ORR、DCR等关键指标,并分析了其在不同患者群体中的疗效差异。同时,报告也对SYSA1801的安全性数据进行了分析,指出其耐受性良好。
CLDN18.2 ADC产品市场竞争分析
报告对科济药业CT041、康诺亚CMG901和石药集团SYSA1801三款CLDN18.2 ADC产品的临床数据、进展阶段以及潜在市场份额进行了比较分析,并指出了ADC药物在肿瘤末线治疗中可能存在的复发耐药问题,建议关注更长随访时间的临床数据。
总结
2023年ASCO会议上公布的国产CLDN18.2创新药临床数据显示,国产创新药在疗效和安全性方面均具有显著优势,尤其在胃或胃食管交界处(G/GEJ)腺癌治疗领域展现出巨大的市场潜力。创胜集团的Osemitamab和石药集团的SYSA1801分别在单抗和ADC领域表现突出,有望在未来的市场竞争中占据领先地位。然而,投资者仍需关注临床试验结果的不确定性、商业化合作的进展以及市场竞争的加剧等潜在风险。 持续关注后续临床试验数据以及市场动态,将有助于更准确地评估这些创新药的长期发展前景和市场价值。
-

医药生物行业深度研究:PD-(L)1双靶点药物再掀免疫治疗热潮(一)
-

农药:行业风口或指向杀虫剂-关注氨基甲酸酯类杀虫剂产业机遇
-

医药2024年三季报总结:业绩触底,行业有望稳健回升
-

基础化工行业专题研究:双碳若加速,化工看点足
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送