-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

核心产品持续放量,期待海外进展
核心产品持续放量,期待海外进展
-
下载次数:
1035 次
-
发布机构:
西南证券股份有限公司
-
发布日期:
2024-03-29
-
页数:
6页
荣昌生物(688331)
投资要点
事件:公司发布2023年度报告,2023年实现营业收入达10.8亿元(+40.3%),公司加大研发投入,2023年研发费用为13.1亿元(+33%)。
核心产品持续放量,自免和肿瘤均准入超过600家医院。泰它西普和维迪西妥单抗2023年持续放量,纳入医保后以量换价明显。截至2023年12月31日,自身免疫商业化团队超过750人,已准入超过800家医院。肿瘤科商业化团队近600人,已准入超过650家医院。
泰它西普多项适应症持续推进,渐入收获期。泰它西普中国治疗重症肌无力完成患者入组,美国于2023年1月获FDA批准IND申请。干燥综合征的中国Ⅲ期临床研究于2023年4月完成首例患者入组。免疫球蛋白A肾病(IgAN)的国内Ⅲ期临床试验方案于2022年9月获得CDE同意,并于2023年第二季度完成首例患者入组。公司正在美国开展泰它西普用于治疗SLE的Ⅲ期国际多中心临床研究,于2022年6月获得首例患者入组。
维迪西妥单抗持续探索UC、GC、BC及妇科肿瘤等适应症。维迪西妥单抗在美国作为治疗一线化疗失败后HER2表达UC患者的的II期关键性临床试验患者招募工作正在进行中。联合特瑞普利单抗及化疗或联合特瑞普利单抗及赫赛汀治疗一线HER2表达局部晚期或转移性GC患者的II/III期临床试验IND获得CDE批准。该试验已于2023年第三季度完成首例患者入组。与帕妥珠单抗联合或不联合特瑞普利单抗新辅助治疗HER2阳性BC的II期临床实验获批。联合特瑞普利单抗或来曲唑新辅助治疗HR阳性和HER2低表达BC的II期临床试验于2023年3月获批。联合赛帕利单抗治疗至少一线含铂标准治疗失败的PD-1/PD-L1经治的HER2表达的复发或转移性宫颈癌II期临床研究正式获得CDE批准。
盈利预测:随着泰它西普和维迪西妥单抗的持续放量,我们预计公司2024-2026年营业收入分别为16.7、23.4和41.6亿元。
风险提示:研发进展或不及预期、核心品种商业化进展或不及预期、政策风险。
中心思想
本报告对荣昌生物(688331)2023年年报进行了点评,核心观点如下:
- 核心产品放量驱动增长:泰它西普和维迪西妥单抗作为核心产品,在纳入医保后销量显著增长,成为公司营收的主要驱动力。
- 研发投入与适应症拓展:公司持续加大研发投入,积极推进泰它西普和维迪西妥单抗的多项适应症临床试验,有望进入收获期。
- 盈利预测与风险提示:基于核心产品销售放量和适应症拓展的假设,报告对公司未来收入进行了预测,并提示了研发进展、商业化以及政策风险。
主要内容
公司业绩与研发投入
荣昌生物2023年实现营业收入10.8亿元,同比增长40.3%。公司持续加大研发投入,2023年研发费用达13.1亿元,同比增长33%。
核心产品市场准入与商业化
泰它西普和维迪西妥单抗持续放量,自免和肿瘤均准入超过600家医院。截至2023年12月31日,自身免疫商业化团队超过750人,已准入超过800家医院;肿瘤科商业化团队近600人,已准入超过650家医院。
泰它西普适应症进展
泰它西普多项适应症持续推进,渐入收获期。
- 国内临床进展:重症肌无力完成患者入组,干燥综合征Ⅲ期临床研究完成首例患者入组,IgAN的Ⅲ期临床试验方案获得CDE同意并完成首例患者入组。
- 海外临床进展:美国获FDA批准IND申请,SLE的Ⅲ期国际多中心临床研究正在美国开展。
维迪西妥单抗适应症探索
维迪西妥单抗持续探索UC、GC、BC及妇科肿瘤等适应症。
- 美国临床进展:在美国作为治疗一线化疗失败后HER2表达UC患者的II期关键性临床试验患者招募工作正在进行中。
- 国内临床进展:联合特瑞普利单抗及化疗或联合特瑞普利单抗及赫赛汀治疗一线HER2表达局部晚期或转移性GC患者的II/III期临床试验IND获CDE批准并完成首例患者入组;与帕妥珠单抗联合或不联合特瑞普利单抗新辅助治疗HER2阳性BC的II期临床实验获批;联合特瑞普利单抗或来曲唑新辅助治疗HR阳性和HER2低表达BC的II期临床试验获批;联合赛帕利单抗治疗至少一线含铂标准治疗失败的PD-1/PD-L1经治的HER2表达的复发或转移性宫颈癌II期临床研究正式获得CDE批准。
盈利预测
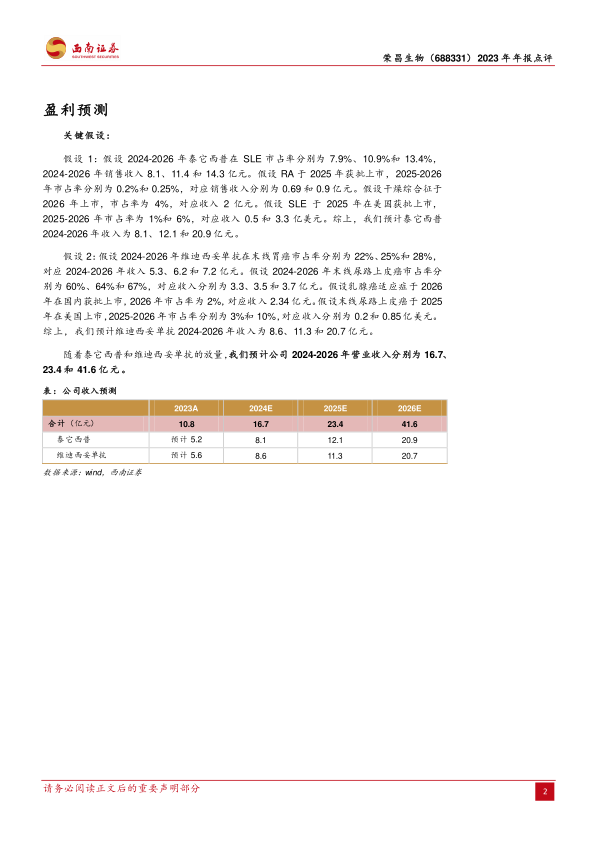
基于泰它西普和维迪西妥单抗的销售放量,预计公司2024-2026年营业收入分别为16.7亿元、23.4亿元和41.6亿元。
- 泰它西普收入预测:预计2024-2026年收入为8.1亿元、12.1亿元和20.9亿元。
- 维迪西妥单抗收入预测:预计2024-2026年收入为8.6亿元、11.3亿元和20.7亿元。
风险提示
报告提示了研发进展或不及预期、核心品种商业化进展或不及预期、政策风险。
总结
荣昌生物2023年报显示,公司核心产品泰它西普和维迪西妥单抗持续放量,驱动营收增长。公司加大研发投入,积极拓展适应症,有望迎来收获期。报告基于核心产品销售和适应症拓展的假设,对公司未来收入进行了预测,并提示了相关风险。总体而言,荣昌生物在自免和肿瘤领域具有较强的竞争力,未来发展值得期待。
-

创新药专题:中国之声闪耀2026ASCO
-

医药行业周报:BD合作持续推进,ASCO年会正式开幕
-

医药行业周报:ASCO年会倒计时
-

医药行业周报:百亿BD再现,关注5月末ASCO会议
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送