-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

专注于first-in-class的创新药先锋
专注于first-in-class的创新药先锋
-
下载次数:
1817 次
-
发布机构:
平安证券股份有限公司
-
发布日期:
2020-09-08
-
页数:
40页
中心思想
微芯生物:原创创新药的先行者与价值低估的投资机遇
微芯生物作为国内专注于first-in-class(全球首创)创新药研发的先行者,凭借其独特的化学基因组学集成式药物创新平台,在小分子原创药领域展现出卓越的研发实力和高效的创新能力。报告核心观点认为,公司目前拥有西达本胺、西格列他钠和西奥罗尼三大核心产品,这些产品均具备广阔的市场前景和显著的临床优势,但其现有价值被市场显著低估。
核心产品驱动增长,技术平台赋能未来
西达本胺作为全球首个亚型选择性组蛋白去乙酰化酶(HDAC)抑制剂,在获批外周T细胞淋巴瘤和乳腺癌适应症后,未来有望通过新适应症的不断落地和联合用药的巨大潜力,成长为销售峰值超20亿元的重磅炸弹。西格列他钠作为全球首个PPAR全激动剂,其2型糖尿病适应症即将上市,非酒精性脂肪性肝炎(NASH)适应症也具备成为首批上市药物的潜力,市场空间巨大。西奥罗尼作为机制新颖的多靶点激酶抑制剂,在多个肿瘤适应症中展现出良好前景。公司特有的化学基因组学技术平台是其保持高效创新的核心竞争力,能够源源不断地发现创新药物活性分子,并显著降低新药开发风险,为公司未来持续发展提供强大动力。基于对三大主力品种的估值,报告首次覆盖给予“推荐”评级,并认为公司200亿市值仅是起点,未来发展空间广阔。
主要内容
前言:市场对微芯生物价值的低估与报告解读
本报告旨在深入分析微芯生物的内在价值,纠正市场对其价值解读的不足之处。市场普遍认为西达本胺放量低于预期,且低估了公司特有的化学基因组学研发平台及其在研管线的价值。报告将通过详细分析,揭示西达本胺在广谱抗癌和联合用药方面的巨大潜力,以及公司研发平台在降低first-in-class创新药研发风险、提高研发效率方面的核心作用。
一、 公司概况:国内 first-in-class 级别原创药引领者
专注于原创新分子实体药物研发,创始团队资历深厚
微芯生物由鲁先平博士等资深留美归国团队于2001年在深圳创立,专注于first-in-class级别的新分子实体原创药研发,与国内多数以仿制药或me-too类新药开发为主的医药企业形成鲜明对比。公司依托其特有的“化学基因组学的集成式药物发现及早期评价平台”,能够持续发现创新药物活性分子并预判其生物学功能和潜在副作用,从而降低新药开发风险。核心创始人鲁先平博士拥有深厚的学术背景和丰富的药物研发经验,在新分子创新药治疗领域已获得100余项发明专利。公司股权结构稳定,鲁先平博士为实际控制人,主要股东承诺科创板上市后3年内不转让股份。公司已形成深圳总部(研发和管理)、深圳微芯药业(西达本胺产业化)、成都微芯药业(西格列他钠和西奥罗尼产业化及区域研发)、北京临床研究中心和上海商业中心“四位一体”的产业布局。
创新药是公司主要业绩来源
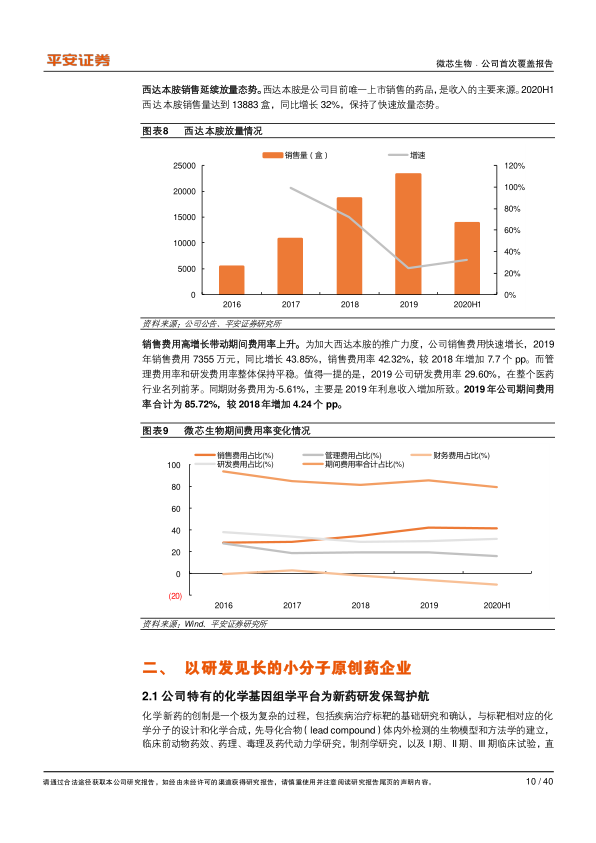
微芯生物的业绩保持快速增长态势。2015-2019年,公司营业收入和归母净利润的复合年均增长率(CAGR)分别达到39.83%和37.84%。2020年上半年,公司实现收入1.11亿元,同比增长35.00%,归母净利润2871万元,同比增长63.97%,在疫情影响下逆势大幅回升。西达本胺作为公司目前唯一上市销售的药品,是收入的主要来源,2020年上半年销售量达到13883盒,同比增长32%,保持了快速放量态势。公司在研发方面投入巨大,2019年研发费用率高达29.60%,在医药行业中名列前茅,显示出其以研发为核心的经营策略。同期销售费用也快速增长,2019年销售费用7355万元,同比增长43.85%,销售费用率达到42.32%,主要用于加大西达本胺的推广力度。
二、 以研发见长的小分子原创药企业
公司特有的化学基因组学平台为新药研发保驾护航
新药创制是一个高投入、高风险的复杂过程,根据《美国医学会杂志》2020年3月的分析,2009-2018年美国制药公司将每个新药推向市场的成本约10亿美元,其中肿瘤和免疫领域更高,且临床研究阶段风险尤为突出。微芯生物在国际上率先构建了基于化学基因组学的集成式药物创新和早期评价平台,该平台通过对化合物与基因表达、生物表型或疾病表型之间关系的并行研究,能够前瞻性地评价和预测新化合物的分子药理和毒理,从而优化候选化合物结构,显著降低新药开发风险。该平台涵盖分子医学、计算机辅助药物设计、药物化学及组合化学、高通量高内涵药物筛选、基因表达芯片谱、生物信息学和化学信息学分析等六部分。得益于此,公司推进到临床阶段的产品上市成功率达到100%,展现出与市场上已有治疗药物显著的差异化和临床独特价值。
西达本胺开启中国创新药对欧美专利授权先河
微芯生物实施全球化的知识产权战略,围绕产品链在化合物通式、制备方法、晶型、剂型和用途等方面进行全链条、全生命周期的专利布局,已在全球范围内申请发明专利200余项,获授权70余项。其中,西达本胺化合物中国发明专利于2017年获得“中国专利金奖”。2006年10月,公司通过“许可费+里程碑收入+收益分成”的方式,将西达本胺在美国、日本、欧盟等国家或地区的权利授权给沪亚生物国际有限责任公司(美国企业),开创了中国原创新药对欧美进行专利授权的先河。2016年2月,沪亚生物又将西达本胺在日本、韩国等8个亚洲国家的开发和销售权再许可给日本卫材,再许可的里程碑付款高达2.8亿美元,充分体现了西达本胺的创新价值和国际认可度。
在研管线丰富,均为自主研发的新分子实体药物
公司主要产品均为自主研发的新分子实体原创新药,作用机制新颖。已上市的1类新药西达本胺是全球首个亚型选择性组蛋白去乙酰化酶抑制剂;已提交2型糖尿病适应症上市申请的西格列他钠是全球首个完成III期临床的PPAR全激动剂;已开展多个II期临床的西奥罗尼是机制新颖的多靶点、多通路选择性激酶抑制剂。此外,公司还拥有一系列新分子实体候选药物,如CS12192(JAK3/JAK1/TBK1选择性激酶抑制剂,类风关等适应症处于临床I期)、CS27109(靶向肝脏TRβ选择性抑制剂,NASH、脂代谢紊乱适应症即将进入临床)等,正在进行临床前与早期探索性研究。公司在研管线全面布局代谢性疾病、自身免疫性疾病、肿瘤、中枢神经和抗病毒五个治疗领域,展现出强大的持续创新能力。
三、 西达本胺:全球首个亚型选择性 HDAC 抑制剂
表观遗传学是当前药物研发的重要热点
在抗肿瘤治疗领域,表观遗传学已成为药物研发的重要热点。表观遗传调控在克服肿瘤免疫逃逸、诱导肿瘤干细胞分化、逆转上皮间充质细胞表型转化以及清除耐药性细胞等方面发挥关键作用。西达本胺作为全球首个亚型选择性组蛋白去乙酰化酶(HDAC)抑制剂,属于表观遗传调控剂类药物,其作用机理独特,包括直接抑制肿瘤细胞周期并诱导细胞凋亡、诱导和激活自然杀伤细胞(NK)和抗原特异性细胞毒T细胞(CLT)介导的肿瘤杀伤作用,以及抑制肿瘤细胞的表型转化及微环境的促耐药/促转移活性。西达本胺与其他机制药品联用潜力巨大,可通过表观遗传调控恢复耐药肿瘤细胞对药物的敏感性,并抑制肿瘤转移和复发。目前,ClinicalTrials.gov显示西达本胺共有71项临床试验记录,其中多项为联合用药试验,如与PD-1、CAR-T、利妥昔单抗等的联合治疗。
外周 T 细胞淋巴瘤是西达本胺获批的首个适应症
西达本胺于2014年12月在中国获批上市,是国内首个以二期临床试验结果获批的国家1类原创新药,也是目前中国唯一治疗复发或难治性外周T细胞淋巴瘤(PTCL)的药物。PTCL是淋巴瘤的一种亚型,在我国发病率约占非霍奇金淋巴瘤(NHL)的25%~30%,显著高于欧美国家。2019年我国大陆地区新发PTCL约2.32万人,且发病率呈上升趋势。西达本胺与现有治疗方式相比优势明显,其总生存期中位数达21.4个月,远高于传统化疗(5.8个月)和国际上其他HDAC抑制剂(如贝利司他7.9个月、罗米地辛11.3个月),且为口服给药,依从性高,月治疗费用(1.85万元)相对较低。西达本胺在《中国临床肿瘤学会(CSCO)淋巴瘤诊疗指南》中连续三年获得最高推荐等级I级专家推荐。2017年纳入国家医保后,2019年成功续约,支付标准调整为343元/片(5mg),进一步助力其持续放量。根据测算,西达本胺PTCL适应症的销售峰值有望达到6.27亿元。
乳腺癌适应症获批,西达本胺为 I 级专家推荐治疗方案
2019年11月,西达本胺新适应症获批,即联合芳香化酶抑制剂用于激素受体阳性(HR+)、人表皮生长因子-2阴性(HER2-)、绝经后、经内分泌治疗复发或进展的局部晚期或转移性乳腺癌患者。乳腺癌是我国女性第一大肿瘤,年新发病例达30.4万例。HR+/HER2-乳腺癌约占所有乳腺癌的70%,其中约一半为绝经后患者,晚期患者占比约20%。据测算,西达本胺乳腺癌适应症年新增潜在患者约5.1万人,远超PTCL。内分泌治疗是HR+晚期乳腺癌的一线疗法,而HDAC抑制剂药物凭借全新作用机制和突出临床效果,与芳香化酶抑制剂(AI)联用已成为内分泌治疗中I级专家推荐治疗方案,证据等级1A。在关键性III期临床试验ACE研究中,西达本胺联合依西美坦可显著延长患者无进展生存期(PFS)(7.4个月VS 3.8个月),尤其在内脏转移患者中差异更明显。西达本胺与其他二线药物机制不同,存在巨大的联合用药潜力。根据测算,西达本胺乳腺癌适应症的销售峰值可达11.63亿元。
弥漫性大 B 细胞淋巴瘤、NSCLC 等适应症逐步落地
除已获批的PTCL和乳腺癌适应症外,西达本胺“弥漫性大B细胞淋巴瘤(DLBCL)联合一线”和“非小细胞肺癌(NSCLC)”适应症均处于III期临床试验过程中。
- 弥漫性大B细胞淋巴瘤: DLBCL是非霍奇金淋巴瘤的常见类型,约占NHL的36%。标准一线治疗方案为利妥昔单抗联合CHOP化疗方案(R-CHOP方案)。西达本胺联合R-CHOP方案具有多重协同药效机制,包括针对DLBCL存在的表观遗传异常、与柔红霉素的协同作用以及促进CD20表达。2018年ASH年会公布的II期研究结果显示,西达本胺联合R-CHOP21治疗老年新诊断DLBCL患者的完全缓解率(CR)达85.1%,客观缓解率(ORR)达89.4%,且安全性良好。根据测算,西达本胺DLBCL适应症的销售峰值可达3.55亿元。
- 非小细胞肺癌: 肺癌是我国发病率和死亡率第一大癌症,NSCLC约占全部肺癌的85%。西达本胺主要针对晚期NSCLC无驱动基因的患者,此类患者过去首选化疗,但耐药问题突出。西达本胺联合PD-1单抗治疗晚期NSCLC的效果已得到证实,Ib/II期临床试验显示客观缓解率达38%,疾病控制率达75%。根据测算,西达本胺NSCLC适应症的销售峰值约6.39亿元。
四、 西格列他钠:2 型糖尿病大适应症即将上市
2 型糖尿病适应症空间广阔
西格列他钠是公司自主研发的PPAR全激动剂1类新药,作用机制新颖,可适度且平衡地激活PPAR三个受体亚型,除胰岛素增敏作用外,还能调节脂代谢,减少PPARγ相关的副作用。其2型糖尿病适应症已于2019年9月提交上市申请,获批在即。糖尿病患者人群庞大,2019年全球成人糖尿病患者约4.62亿人,我国达1.16亿人,其中90%左右为2型糖尿病,且我国仍有56%的患者未诊断,市场空间广阔。西格列他钠已完成2项III期临床试验,结果显示其可显著降低2型糖尿病患者的HbA1c,且非劣效于西格列汀,整体安全性良好。西格列汀2019年全球销售额仍高达34.8亿美元。随着GLP-1受体激动剂、DPP-4抑制剂和SGLT-2抑制剂等新机制降糖药在国内医保覆盖下渗透率快速提升,西格列他钠作为机制新颖的药物,有望尽快进入医保。根据测算,西格列他钠2型糖尿病适应症的销售峰值有望达到15.78亿元。
NASH 是下一个蓝海市场
非酒精性脂肪性肝炎(NASH)是非酒精性脂肪性肝病(NAFLD)的进展阶段,会显著提高肝硬化、肝衰竭和肝细胞癌的风险。NAFLD是全球最常见的慢性肝病,普通成人患病率在6.3%~45%,其中10%~30%为NASH。目前针对NASH的治疗药物稀缺,全球仅一款药品上市(印度Zydus Cadia公司的Saroglitazar)。EvaluatePharma预测,全球NASH药物市场规模在2025年将达到400亿美元,是一个即将爆发的蓝海市场。西格列他钠作为PPAR全激动剂,具有突出的糖脂代谢调节作用和一定的抗炎效果,其NASH适应症已进入II期临床阶段,有望成为首批上市的NASH治疗药物。微芯生物在NASH治疗领域还布局了CS27109(TRβ选择性激动剂)和CS17919(ASK1抑制剂),均处于临床前期。根据测算,西格列他钠NASH适应症的销售峰值可达10.61亿元。
五、 西奥罗尼:机制新颖的多靶点多通路激酶抑制剂
西奥罗尼是公司自主研发的小分子原创新药,属于多靶点多通路选择性激酶抑制剂,对VEGFR1/2/3、PDGFR α/β、CSF-1R和Aurora B等多种肿瘤相关标靶蛋白激酶均有显著的体外抑制活性。其抗肿瘤效果主要通过抑制肿瘤血管生成(VEGFR和PDGFR)、抑制肿瘤细胞有丝分裂(Aurora B)和调节肿瘤免疫微环境(CSF-1R)三种活性机制发挥。目前,VEGFR、PDGFR和CSF-1R靶点已有相关药品上市,而Aurora B靶点尚无品种获批,但Aurora A/B在多种肿瘤组织中均有显著高表达,是潜在的肿瘤治疗靶点。从竞品的临床进展来看,除武田的Alisertib完成3期临床外,其他Aurora靶点药物基本处在1期和2期。西奥罗尼目前有小细胞肺癌、卵巢癌、肝癌和淋巴瘤等4个适应症已开展2期临床,有望成为首批上市的Aurora抑制剂产品。报告预计西奥罗尼销售峰值为15亿元,并根据经验给予3倍PS估值,估值结果为45亿元。
六、 盈利预测与投资评级
报告对微芯生物三大核心产品进行了估值。西达本胺采用DCF绝对估值方法,估值结果为86.92亿元。西格列他钠同样采用DCF估值方法,估值结果为72.66亿元。对于西奥罗尼,考虑到其主要适应症尚处于II期临床,采用PS估值方式,预计销售峰值为15亿元,给予3倍PS,估值结果为45亿元。综合来看,公司三大主力品种合计估值达204.58亿元。报告认为,考虑到西达本胺的海外权益和公司丰富的在研管线价值,公司现有价值被显著低估。公司特有的化学基因组学技术平台是其核心竞争力,能够提供源源不断的创新活水。参考海外平台型公司和CRO企业估值,报告认为200亿市值仅是起点,未来公司发展空间广阔。报告预计公司2020-2022年归母净利润分别为0.32亿、0.61亿和1.20亿元。首次覆盖,给予“推荐”评级。
七、 风险提示
技术平台迭代风险
生物医药行业技术发展迅速,若未来出现突破性技术发现而公司未能保持先进性,将对公司未来经营产生不利影响。
研发失败风险
创新药研发具有高投入、高风险的特征,公司在研品种存在研发失败或未能获批上市的可能。
行业竞争风险
在PTCL、2型糖尿病等适应症中,有多个
-

GLP-1药物未来方向标:减脂增肌、口服剂型、超长效制剂赛道掘金
-

医疗设备招投标数据跟踪:设备更新不断深化,县域医共体持续发力
-

医疗设备招投标数据跟踪:招投标持续恢复,国产替代趋势显著
-

生物医药行业:国产新药闪耀ASCO 2025,关注相关企业投资机遇
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送