-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

医疗器械:重磅政策加码创新医疗器械,行业迎来发展新契机
医疗器械:重磅政策加码创新医疗器械,行业迎来发展新契机
-
下载次数:
2477 次
-
发布机构:
天风证券股份有限公司
-
发布日期:
2017-11-07
-
页数:
7页
中心思想
本报告的核心观点是:中国政府近年来出台了一系列政策,大力推动创新医疗器械的发展,为行业带来了新的发展契机。这些政策主要围绕加快审评审批、重点发展高临床价值产品和突破自主创新加速国产化三个方向展开,通过“特别审批”和“优先审批”等绿色通道,加速创新医疗器械的上市进程,最终目标是提升医疗器械的创新能力和产业化水平,降低医疗成本,惠及民生。报告同时推荐了五家有望受益于政策红利的医疗器械公司。
政策驱动下的医疗器械行业发展新机遇
中国政府对创新医疗器械产业的支持力度不断加大,一系列政策的出台为行业发展提供了强劲动力。 《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》以及CFDA发布的《医疗器械监督管理条例修正案(草案征求意见稿)》等政策,从加快审评审批、重点发展高临床价值产品和突破自主创新加速国产化三个方面入手,为创新医疗器械的发展创造了良好的政策环境。
“绿色通道”加速创新产品上市
“特别审批”和“优先审批”程序的实施,为符合条件的创新医疗器械提供了快速上市的通道。与传统审批流程相比,这些绿色通道显著缩短了审批时间,例如,明峰医疗公司的产品仅用5个月就完成了上市审批。虽然加速审批并不意味着降低标准,但其有效地促进了创新医疗器械的研发和产业化进程。 数据显示,虽然申请数量逐年增加,但最终获批上市的产品占比相对较低,这表明政策旨在优中选优,确保产品质量和安全性。
主要内容
政策分析:三驾马车驱动行业变革
报告详细分析了近年来中国政府在创新医疗器械领域出台的政策,并将其核心逻辑归纳为三个方面:
- 加快创新医疗器械审评审批: 通过“特别审批”和“优先审批”等机制,简化审批流程,缩短审批时间,为创新医疗器械打开绿色通道。
- 重点发展具备重大临床价值产品: 加大对影像设备、医用机器人、植介入医疗器械、基因检测等高临床价值产品的投入,提升医疗服务水平,降低疾病死亡率,改善患者生活质量。
- 突破自主创新,加速国产化: 鼓励自主研发,突破进口垄断技术,提高国产医疗器械的市场占有率,降低医疗成本。
报告还列举了自2014年以来一系列重要的政策文件,并对“特别审批”和“优先审批”两种程序进行了对比分析,突出了其在审批时间和申请范围上的差异。
市场分析:创新医疗器械发展现状及未来展望
报告分析了2015年和2016年CFDA的数据,指出虽然创新医疗器械的注册申请量逐年增长,但最终获批上市的产品比例相对较低。这并非政策标准降低,而是体现了对创新医疗器械的严格审查,以确保其安全性和有效性。报告预测未来2-3年内,创新医疗器械概念将持续火热,政策环境将持续利好具有强大创新基因的医疗器械公司。
投资建议:重点关注具备技术护城河的标的
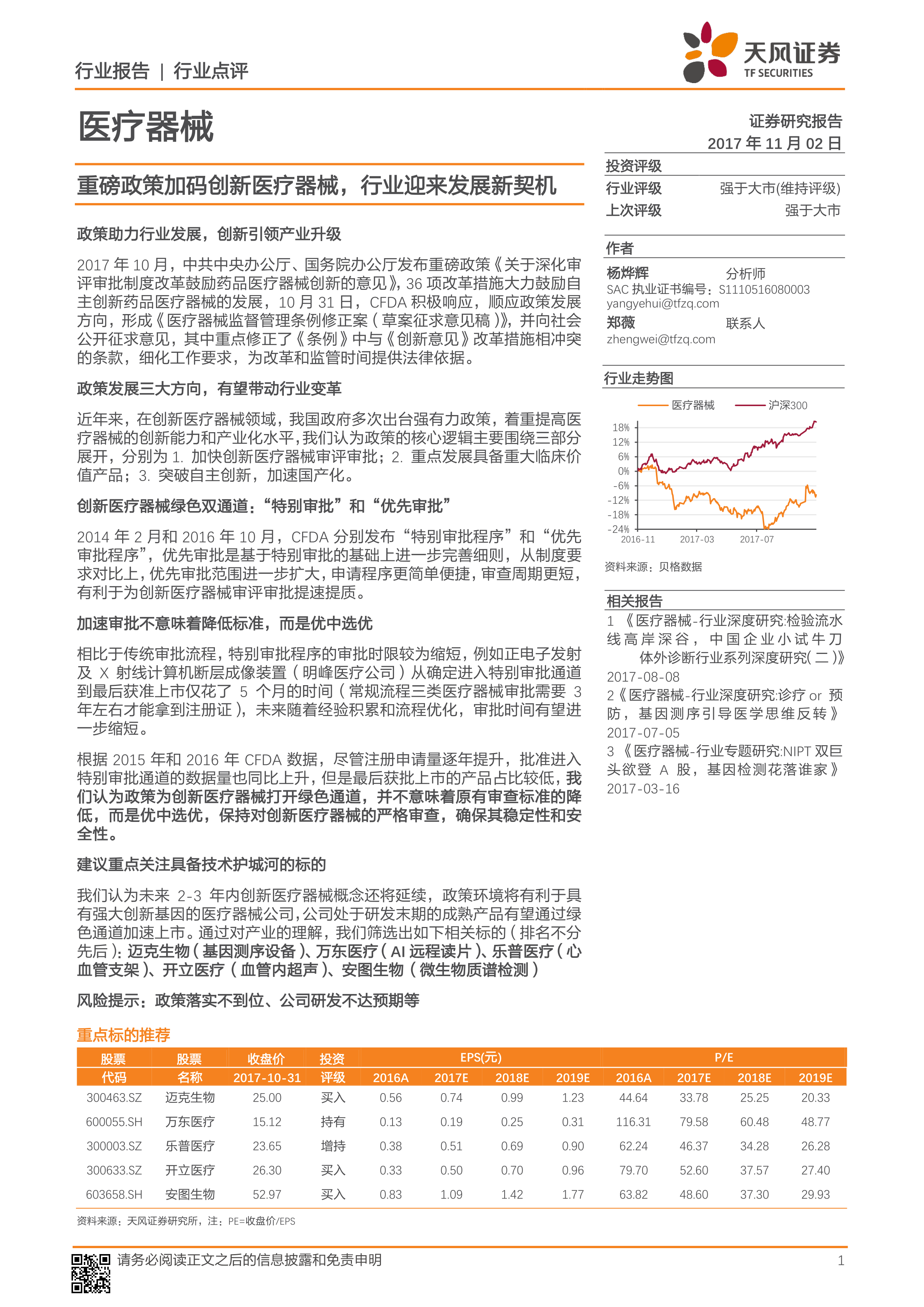
基于对政策环境、市场现状和公司数据的综合分析,报告推荐了五家重点关注的医疗器械公司:迈克生物(基因测序设备)、万东医疗(AI远程读片)、乐普医疗(心血管支架)、开立医疗(血管内超声)、安图生物(微生物质谱检测)。报告还提供了这些公司的股票代码、收盘价、投资评级以及未来几年的EPS预测数据,为投资者提供参考。
总结
本报告深入分析了中国创新医疗器械行业的发展现状和未来趋势。 一系列利好政策的出台,特别是“特别审批”和“优先审批”绿色通道的建立,为创新医疗器械的快速发展提供了强劲动力。 虽然审批过程依然严格,但政策的导向明确,旨在优中选优,确保产品质量和安全性。 报告推荐的五家公司,凭借其在技术创新和临床应用方面的优势,有望在未来几年获得快速发展,成为行业发展的受益者。 然而,投资者仍需关注政策落实情况和公司研发进展等风险因素。
-

天风医药细分领域分析与展望(2025H1):体外诊断行业及个股2025半年度回顾与展望
-

国内短期承压,海外市场呈现良好增长态势
-

基础化工行业研究周报:国家发改委,支持石化化工行业节能降碳改造,煤化工项目低碳化改造,双氧水、硫酸铵价格上涨
-

化工行业运行指标跟踪:2025年8-9月数据
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送