-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

深度报告:深耕恶性肿瘤,源头创新构建全球竞争力
深度报告:深耕恶性肿瘤,源头创新构建全球竞争力
-
下载次数:
927 次
-
发布机构:
中航证券有限公司
-
发布日期:
2024-12-25
-
页数:
57页
迪哲医药(688192)
核心观点:
深耕恶性肿瘤,坚持源头创新的药企。迪哲医药于2017年10月由AZAB、先进制造、无锡灵创共同出资成立;2021年12月于上交所科创板上市,是一家新型生物医药企业,致力于恶性肿瘤新疗法的研究、开发和商业化。2024年前三季度,公司实现营业收入3.38亿元,同比增长743.97%;2024Q3单季实现营业收入1.35亿元,同比增长236.39%。2024年前三季度,公司实现归母净利润-5.58亿元,同比增长32.63%;2024Q3单季实现归母净利润-2.14亿元,同比增长32.09%。公司目前推出两款创新产品上市,舒沃哲(舒沃替尼)于2023年8月获NMPA批准上市;高瑞哲(戈利昔替尼)于2024年6月获NMPA批准上市,舒沃替尼和戈利昔替尼两款产品为公司盈利的主要来源,带动公司整体业绩高速增长。除此以外,公司研发管线拥有多个处于临床阶段应用于多个适应症的小分子创新药,临床试验在全球多国开展,所有产品全球同步开发模式,享有全球权益。
差异化产品实现商业化,提供自我造血能力。
商业化产品1:舒沃替尼是我国自主研发的、获得中美双突破性疗法认定的的创新小分子药物,是目前全球唯一获批靶向治疗EGFRExon20ins突变NSCLC的口服小分子药物,适用于既往经含铂化疗失败且存在表皮生长因子受体EGFR20号外显子插入突变的局部晚期或脑转移性非小细胞肺癌成人患者。EGFRExon20ins是NSCLC罕见突变,恶化程度高,预后差,患者预期生命仅有16.2个月。临床试验表明,舒沃替尼二线治疗EGFRExon20insNSCLC的客观缓解率(ORR)达61%,中位无进展生存期(mPFS)达到6.5个月。舒沃哲由于分子量小,可突破血脑屏障,基线伴脑转移患者同样获得临床收益,mPFS达5.5个月。舒沃替尼获中美“突破性疗法认定”,并被《CSCO指南》I级推荐。
商业化产品2:戈利昔替尼作为全球首个且唯一靶向JAK-STAT通路的治疗PTCL的药物,针对复发性PTCL停药率仅7.3%,具有良好的安全性,且适应症覆盖PTCL多个亚型。临床试验II期单臂试验表明,相比于西达本胺,戈利昔替尼的客观缓解率(ORR)提升58%,达到44.3%,中位无进展生存期(mPFS)提升167%,达到5.6月。2024年4月获得《CSCO淋巴瘤诊疗指南(2024)》II级推荐;并获FDA“快速通道认定”和“孤儿药资格认定”。
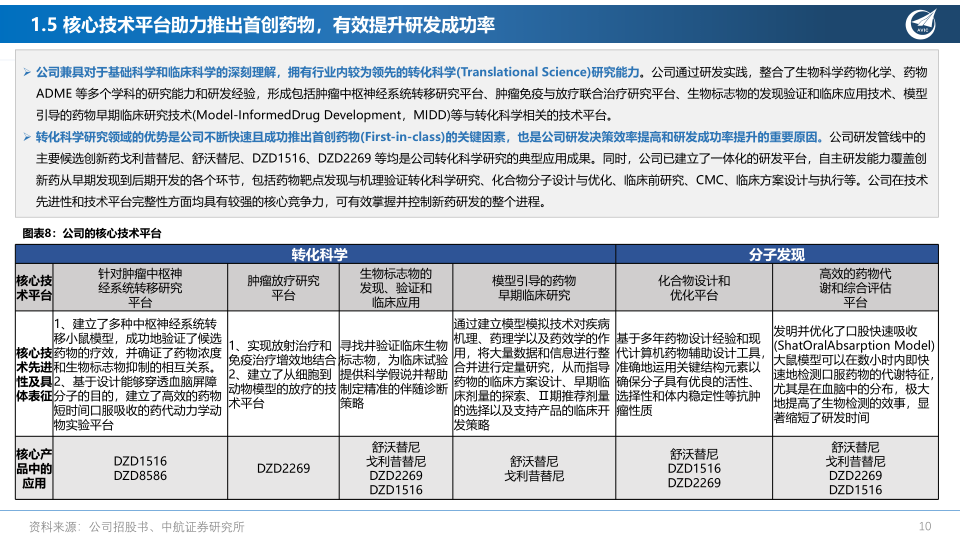
在研管线高度创新,提供持续增长动力。公司为源头创新企业。自公司2021上市以来,研发费用始终是营业成本中占比最大的部分,由2022年的6.65亿元增长到2023年的8.06亿元,截至2024前三季度,公司研发费用为5.68亿元,同比降低1.94%。公司兼具对于基础科学和临床科学的深刻理解,拥有行业内较为领先的转化科学(TranslationalScience)研究能力,拥有包括肿瘤中枢神经系统转移研究平台、肿瘤免疫与放疗联合治疗研究平台、生物标志物的发现验证和临床应用技术、模型引导的药物早期临床研究技术(Model-InformedDrugDevelopment,MIDD)等与转化科学相关的技术平台。转化科学研究领域的优势是公司不断快速且成功推出首创药物(First-in-class)的关键因素,也是公司研发决策效率提高和研发成功率提升的重要原因。基于行业领先的转化科学和新药分子设计与筛选技术平台,公司已建立了六款具备全球竞争力的产品管线,其中两大处于全球注册临床试验阶段的领先产品均已在中国获批上市。公司已建立了极具创新性和市场潜力的小分子产品管线组合,所有产品均享有完整的全球权益,并采用全球同步开发的模式。公司当前战略性专注于恶性肿瘤等存在巨大未被满足和刚性治疗需求的疾病领域。
投资建议。公司作为国内专注于恶性肿瘤治疗的小分子药物龙头,其目前两款商业化产品在疗效和安全性方面较已国内上市竞品具有明显优势。随着公司商业化产品在国内市场的快速放量,有望驱动公司业绩实现快速增长。其中,舒沃哲作为首个且唯一全线治疗EGFRExon20insNSCLC获四项中、美“突破性疗法认定”的创新药物,其二线治疗EGFRExon20insNSCLC在美国上市申请已经提交,一线治疗的三期临床研究正在全球顺利开展,随着产品的各个适应症顺利研发并成功上市,公司产品销售业绩有望进一步增厚。早期管线方面,公司的多个产品均基于自身研发平台研发,具有高度的源头创新特性,且布局的赛道高度差异化,竞争格局比较缓和,未来后续产品的顺利研发或将给公司带来持续的增长动力。我们预计公司2024-2026年的EPS分别为-1.88元、-1.40元和-0.01元,给予买入评级。
风险提示:公司在研产品研发不及预期风险;公司产品审评审批进度及结果不及预期风险;销售不及预期风险;技术升级及产品迭代风险。
中心思想
源头创新驱动业绩增长
迪哲医药作为一家深耕恶性肿瘤领域的生物医药企业,始终坚持源头创新,致力于新型疗法的研究、开发和商业化。公司已成功推出舒沃哲(舒沃替尼)和高瑞哲(戈利昔替尼)两款创新产品,并凭借其卓越的临床疗效和安全性,迅速实现商业化放量,成为公司业绩高速增长的主要驱动力。
差异化产品构建全球竞争力
迪哲医药通过其领先的转化科学平台和新药分子设计与筛选技术,构建了具有全球竞争力的产品管线。舒沃哲是全球唯一获批靶向EGFR Exon20ins突变NSCLC的口服小分子药物,填补了该领域的治疗空白;高瑞哲是全球首个且唯一靶向JAK-STAT通路治疗PTCL的创新小分子药物。这些差异化产品不仅满足了巨大的未被满足的临床需求,也为公司提供了持续的自我造血能力和全球市场拓展潜力。
主要内容
深耕恶性肿瘤,坚持源头创新的药企
公司概况与业绩表现
- 公司历史沿革: 迪哲医药于2017年10月成立,2021年12月在上交所科创板上市,专注于恶性肿瘤新疗法的研究、开发和商业化。公司拥有先进的转化科学平台和完善的研发管线,以推出首创药物(First-in-class)为目标。
- 产品快速放量,长期业绩有望扭亏: 2024年前三季度,公司实现营业收入3.38亿元,同比增长743.97%;其中2024Q3单季营收1.35亿元,同比增长236.39%。尽管归母净利润仍为负(-5.58亿元),但同比增幅达32.63%,显示亏损收窄。舒沃替尼和戈利昔替尼两款商业化产品是公司业绩高速增长的主要来源。
- 维持高研发费用投入,加快创新项目落地: 迪哲医药作为源头创新企业,研发费用始终是营业成本中占比最大的部分,2023年达到8.06亿元。公司拥有肿瘤中枢神经系统转移研究平台、肿瘤免疫与放疗联合治疗研究平台等转化科学技术平台,这些优势是公司快速成功推出首创药物的关键。
- 公司核心商业化产品:
- 舒沃哲(舒沃替尼): 于2023年8月获NMPA批准上市,是全球唯一获批靶向EGFR Exon20ins突变NSCLC的口服小分子药物,获得中美双突破性疗法认定。
- 高瑞哲(戈利昔替尼): 于2024年6月获NMPA批准上市,是全球首个且唯一靶向JAK-STAT通路的治疗PTCL的药物。
- 全球权益与同步开发: 公司所有产品均享有完整的全球权益,并采用全球同步开发的模式,已建立了六款具备全球竞争力的产品管线。
差异化产品实现商业化,提供自我造血能力
商业化产品1:舒沃替尼——填补EGFR Exon20ins突变晚期NSCLC治疗领域空白
- 肺癌市场概况:
- 全球与中国肺癌发病率: 肺癌是全球和中国新发和死亡病例最高的恶性肿瘤。2022年,肺癌在全球新发癌症中占比20%,死亡率占比27%。在中国,肺癌新发病例占比28%,死亡率占比35%,是我国恶性肿瘤和死亡的首位原因。
- 肺癌新发病例数量: 全球肺癌新发病例从2016年的198.08万人增长到2020年的220.68万人,年复合增长率2.7%。中国新发肺癌病例从2016年的81.34万人增长到2020年的92.41万人,年复合增长率3.2%,高于全球水平。
- 肺癌治疗方案与靶向治疗:
- 靶向治疗适用性: 靶向治疗是适用于驱动基因阳性的肺癌治疗方案,可减少对健康细胞的侵害,提高生存期。
- EGFR-TKIs市场规模: 全球EGFR-TKI药物市场规模从2015年的33亿美元增长到2019年的53亿美元,预计2024年将达到123亿美元。中国市场规模从2015年的24亿元增长到2019年的77亿元,年复合增长率33.7%,预计2024年将达到312亿元。
- EGFR Exon20ins突变与临床需求:
- 突变特点: EGFR Exon20ins是第三常见的EGFR基因突变,占所有NSCLC人群的0.1%~4%,占EGFR突变患者的1%~12%。该突变恶化程度高,预后差,患者预期生命仅16.2个月,且临床上缺乏标准治疗方案。
- 传统治疗局限性: EGFR Exon20ins突变具有高度异质性和特殊分子结构,导致传统化疗及第一、二、三代TKI药物疗效不佳,中位无进展生存期(PFS)仅2-6个月。
- 舒沃替尼的创新性与优势:
- 分子设计创新: 舒沃替尼具有柔性苯氨基结构,可弯折嵌入EGFR与ATP结合的“楔形口袋”,对EGFR Exon20ins突变型具有高度选择性(对野生型选择性是3-10倍),降低脱靶毒性。分子量小,可突破血脑屏障。
- 二线治疗临床疗效与安全性: 在WU-KONG6临床试验中,舒沃替尼二线治疗EGFR Exon20ins NSCLC的客观缓解率(ORR)达61%,中位无进展生存期(mPFS)达6.5个月。基线伴脑转移患者mPFS达5.5个月。3级及以上严重不良事件发生率仅18%,安全性优于竞品莫博赛替尼(69%)和埃万妥单抗(输液相关反应)。
- 一线治疗临床疗效与安全性: 在WU-KONG28临床试验中,舒沃替尼一线治疗ORR达53.3%,9个月DoR达57%,mPFS为7.3个月。WUKONG1和WUKONG15汇总分析显示ORR达78.6%,mPFS达12.4个月。安全性良好,未出现剂量限制性毒性(DLT)。
- 指南推荐: 舒沃替尼被《CSCO指南》I级推荐为IV期EGFR 20外显子插入突变后线治疗方案。
- 竞争格局与市场潜力:
- 竞争格局: 二线治疗领域,舒沃替尼是全球前二、国内唯一获批药物。一线治疗领域,舒沃替尼进展居前,已进入三期临床。
- 市场销售峰值测算: 全球EGFR Exon20ins NSCLC新发病例预计2024年达7.35万人,中国达3.54万人。考虑到舒沃哲年化费用约22万元/人,预计中国市场销售峰值有望突破30.76亿元;全球市场销售峰值有望达到129.54亿元。
商业化产品2:戈利昔替尼——全球首个且唯一靶向JAK-STAT通路治疗PCTL的创新小分子药物
- 淋巴瘤市场概况:
- 淋巴瘤分类: 非霍奇金淋巴瘤(NHL)约占所有淋巴瘤的90%,其中外周T细胞淋巴瘤(PTCL)和皮肤T细胞淋巴瘤(CTCL)合计约占NHL的17%-25%。
- 淋巴瘤新发病例: 2020年中国新发NHL病例92834例,男性高于女性。全球淋巴瘤新发病例从2016年的56.4万增至2020年的62.7万,预计2030年达76.5万。中国淋巴瘤新发病例从2015年的8.70万人增长到2019年的9.66万人,增速略高于全球。
- 外周T细胞淋巴瘤发病人数: 全球PTCL发病人数从2015年的3.33万人增长到2019年的3.65万人,预计2030年达4.68万人。中国PTCL发病人数从2015年的2.04万人增长到2019年的2.26万人,增速略高于全球。
- 皮肤T细胞淋巴瘤发病人数: 全球CTCL发病人数预计2030年达2.81万人。中国CTCL发病人数预计2030年达4500人。
- 临床需求与现有治疗局限性:
- PTCL侵袭性强,缺乏标准治疗: PTCL侵袭性强、预后较差,国际上尚缺乏标准治疗方案。复发或难治性PTCL患者3年总体生存率仅21%-28%。
- 国内药物选择有限: 国内获批的复发难治性PTCL单药治疗药物较少,主要为HDAC抑制剂西达本胺及叶酸拮抗剂普拉曲沙,但HDAC抑制剂临床疗效有限,客观缓解率约为25%-28%。
- 戈利昔替尼的创新性与优势:
- 源头创新: 戈利昔替尼是基于公司转化科学技术平台的新靶点药物,通过研究发现JAK1和STAT3/5在T细胞淋巴瘤发生发展中的主导作用。
- 高选择性与药代动力学: 戈利昔替尼以独特的“两氢键-盐桥”结构实现对JAK1的高度选择性(对JAK家族其他成员选择性大于200倍),避免了JAK2抑制可能导致的严重贫血。半衰期长达50小时,适合每日一次给药,提高患者依从性。
- 显著且持久的抗肿瘤疗效: 在全球关键性注册临床试验(JACKPOT8的B部分)中,戈利昔替尼单药治疗r/r PTCL的ORR达44.3%,完全缓解(CR)率达23.9%,中位DoR长达20.7个月,中位PFS为5.6个月。相较于西达本胺,ORR提升58%,mPFS提升167%。
- 良好安全性与耐受性: 最常见的≥3级治疗相关不良事件(TRAEs)为血液学毒性,但可逆或临床可管理,停药率低(6.3%)。
- 指南推荐: 2024年4月获得《CSCO淋巴瘤诊疗指南(2024)》II级推荐。
- 竞争格局与市场潜力:
- 竞争格局缓和: 戈利昔替尼所在的r/r PTCL赛道竞争格局相对缓和,大部分管线处于早期临床阶段。
- 市场销售峰值测算: 考虑到高瑞哲年化费用约20.4万元/人,预计中国CTCL市场销售峰值有望达到9.18亿元;全球市场销售峰值有望达到82.82亿元。
在研管线高度创新,提供持续增长动力
DZD8586:全新非共价LYN/BTK双靶点抑制剂
- 靶点与适应症: DZD8586是一款能完全穿透血脑屏障的全新非共价LYN/BTK双靶点抑制剂,针对B细胞非霍奇金淋巴瘤(B-NHL)。中国NHL新发病例预计2024年达10.2万人。
- 解决BTK耐药问题: 旨在克服BTK抑制剂的两种主要耐药机制(BTKC481S突变和非BTK依赖性BCR信号通路激活)。
- 临床前与临床试验结果: 临床前研究显示DZD8586可强效抑制LYN和BTK激酶介导的信号通路,有效抑制多种B-NHL亚型细胞生长,并具备完全的血脑屏障穿透能力,对中枢神经系统淋巴瘤(CNSL)具有治疗潜力。I/II期临床研究显示,在多线治疗失败的B-NHL患者中,ORR达64.7%,在DLBCL患者中ORR高达83.3%,在前线接受过BTK抑制剂的患者中ORR达50%,有望克服BTK抑制剂耐药。
DZD1516:高选择性HER2小分子酪氨酸激酶抑制剂
- 靶点与适应症: DZD1516是一种具有穿透血脑屏障能力的高选择性HER2小分子酪氨酸激酶抑制剂,目标适应症为HER2阳性晚期乳腺癌,尤其是有中枢神经系统(CNS)转移的患者。中国HER2阳性乳腺癌发病人数预计2024年达8.8万人。
- 临床痛点: HER2阳性乳腺癌患者CNS转移发生率高(可达40%),且现有大分子靶向药物难以有效通过血脑屏障,导致CNS转移治疗和预防成为瓶颈。
- 优势与竞争格局: DZD1516对HER2具有高选择性(比EGFR高300倍以上),与竞品妥卡替尼相当,远高于其他已上市抑制剂。在小鼠、大鼠和猴子大脑和脑脊液中均显示出良好的血脑屏障穿透性,临床上在带有CNS转移的乳腺癌患者中Kp,uu为1.8。竞争格局方面,全球已上市HER2小分子药物包括吡咯替尼、奈拉替尼、妥卡替尼等,DZD1516处于I期临床。
DZD2269:A2aR拮抗剂
- 靶点与适应症: DZD2269是一种A2aR拮抗剂,目标适应症为转移性去势抵抗性前列腺癌(mCRPC)。中国mCRPC患病人数预计2024年达42.6万人。
- 临床痛点: 肿瘤微环境中高浓度腺苷水平通过腺苷2a受体(A2aR)介导免疫抑制,限制了免疫疗法的效果。现有A2aR拮抗剂在高浓度腺苷下活性显著降低。
- 优势与竞争格局: DZD2269能有效抑制高浓度腺苷引起的免疫抑制作用,体外活性明显高于现有临床中的A2aR拮抗剂。动物实验表明,DZD2269在多种肿瘤模型中显示出肿瘤抑制作用,与放疗、化疗或免疫抑制剂联用时可显著增强。竞争格局缓和,全球范围内以A2aR为靶点、前列腺癌为适应症的研发管线共7个,DZD2269处于I期临床。
投资建议与盈利预测
投资建议
- 核心优势: 迪哲医药作为国内专注于恶性肿瘤治疗的小分子药物龙头,两款商业化产品在疗效和安全性方面具有明显优势。
- 业绩增长驱动: 商业化产品在国内市场的快速放量有望驱动公司业绩快速增长。舒沃哲在美国的上市申请已提交,一线治疗三期临床研究全球顺利开展,未来产品销售业绩有望进一步增厚。
- 持续增长动力: 早期管线产品基于自身研发平台,具有高度源头创新特性,布局赛道高度差异化,竞争格局缓和,有望带来持续增长动力。
- 评级与预测: 预计公司2024-2026年的EPS分别为-1.88元、-1.40元和-0.01元,给予“买入”评级。
盈利预测
- 营业收入: 预计2024-2026年营业收入分别为4.03亿元、8.13亿元和15.25亿元,增长率分别为341.68%、101.53%和87.62%。
- 归母净利润: 预计2024-2026年归母净利润分别为-7.80亿元、-5.84亿元和-0.05亿元,亏损持续收窄。
- 产品贡献: 舒沃哲和高瑞哲的销售收入预计将快速增长,毛利率保持高位。
风险提示
- 在研产品研发不及预期风险。
- 产品审评审批进度及结果不及预期风险。
- 销售不及预期风险。
- 技术升级及产品迭代风险。
总结
迪哲医药凭借其深耕恶性肿瘤领域的源头创新战略,已成功将舒沃哲和高瑞哲两款差异化创新药物推向市场,并展现出强劲的商业化增长势头。舒沃哲作为全球唯一靶向EGFR Exon20ins突变NSCLC的口服小分子药物,以及高瑞哲作为全球首个且唯一靶向JAK-STAT通路治疗PTCL的药物,均填补了各自领域的临床空白,并在临床疗效和安全性方面表现出显著优势。
公司持续高强度的研发投入和领先的转化科学平台,为其构建了包括DZD8586、DZD1516和DZD2269在内的多个高度创新、具备全球竞争力的在研管线,这些管线布局于未被满足的巨大临床需求领域,且竞争格局相对缓和,预示着公司未来持续增长的强大潜力。尽管目前公司仍处于亏损状态,但随着商业化产品的快速放量和全球市场拓展,以及后续管线的顺利推进,公司业绩有望逐步扭亏为盈。分析师给予“买入”评级,反映了对公司长期发展前景的信心,但投资者仍需关注新药研发、审批、销售及技术迭代等潜在风险。
-

脑机接口深度报告:未来产业制高点竞速,多场景需求打开成长空间
-

AI医疗2月月报:AI药物发现提速,国产医疗大模型彰显国际竞争力
-

KC1086获批FDA临床批准,源头创新能力显现
-

2025年三季报点评:业绩维持增长,研发项目稳步推进
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






最新报告
- 医药生物行业周报:分级诊疗体系迎重要部署,关注基层医疗资源配置优化、服务能力提升
- 医疗投资与成果:在中央和东欧
- 2025年年报点评:营养品板块韧性十足,香精香料及新材料业务稳步推进
- 2026年中国生物创新药市场跟踪报告:司美格鲁肽2025年第二季度市场回顾
- 化工行业2026年度春季投资策略:政策发力地缘博弈 重塑化工新格局
- 醋酸行业点评:成本推动叠加出口拉动,醋酸价格快速上行
- 公司事件点评报告:产品结构持续升级,克服集采降价影响
- 基础化工行业研究:硫酸、丁基橡胶等涨幅居前,建议关注进口替代、纯内需、高股息等方向
- 创新药行业研究:抗体偶联药物(ADC)行业:靶点多元化+IO联用创新,开启肿瘤精准治疗新周期
- 25年达成“增长、增效、增值”目标,短中长期部署多个研发项目
对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送