-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

阿立哌唑片美国获批,有望转报国内
阿立哌唑片美国获批,有望转报国内
-
下载次数:
417 次
-
发布机构:
国金证券股份有限公司
-
发布日期:
2017-12-11
-
页数:
9页
中心思想
阿立哌唑美国获批:市场拓展新里程碑
本报告核心观点指出,华海药业(600521.SH)的阿立哌唑片获得美国FDA新药简略申请(ANDA)批准,标志着公司在国际制剂市场取得重要进展。此举不仅巩固了华海药业在制剂出口领域的领先地位,更预示着该品种有望通过海外上市品种转报国内渠道,享受国内一致性评价等政策优势,从而打开国内市场增长空间。
华海药业:制剂出口与国内市场双轮驱动
报告强调,华海药业已成功构建“华海模式”,通过成熟的高技术固体制剂仿制药研发和申报注册平台,以及Solco销售渠道,在美国市场形成竞争优势。同时,公司在国内市场积极响应“优先审评审批”等政策,致力于实现海外获批品种的国内批量上市。结合原料药业务的稳定支撑和生物药领域的长期布局,华海药业正形成制剂出口与国内市场双轮驱动的增长格局。
主要内容
阿立哌唑产品概览与市场格局
阿立哌唑片作为第三代非典型抗精神病药物,是目前治疗精神分裂症的一线用药。该药由Otsuka研发,于2002年在美国上市,其专利行政保护期已于2015年4月到期。目前,美国市场的主要生产厂商包括Teva和Apotex等,而国内主要生产厂商有成都康弘药业集团股份有限公司和江苏恩华药业股份有限公司等。
美国市场分析:仿制药竞争与华海机遇
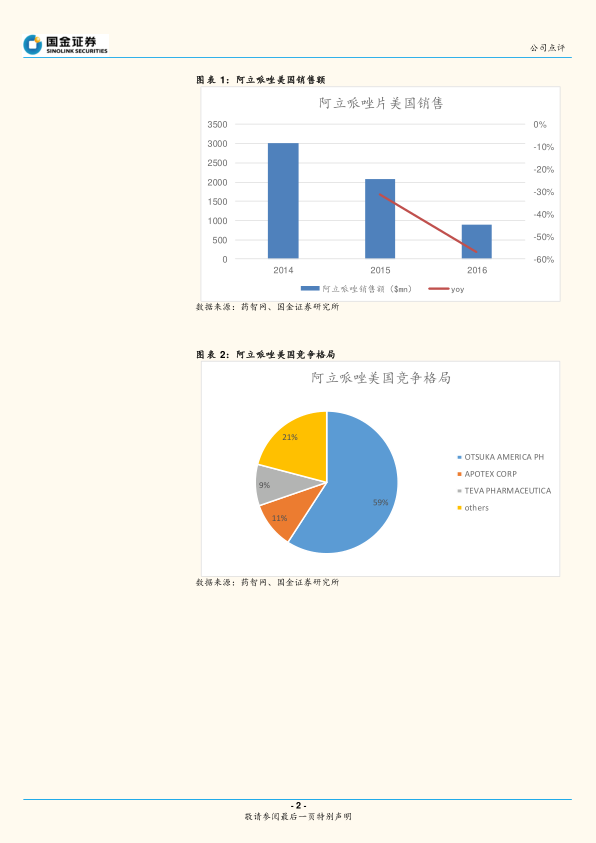
截至2017年12月,美国市场共有14家企业获得阿立哌唑片的ANDA批准。随着仿制药的上市,原研药的市场销售额有所下滑。2016年度,阿立哌唑片在美国市场的销售额约为8.96亿美元;2017年1月至9月,销售额约为2.17亿美元(数据来源于IMS数据库)。在竞争格局方面,原研药厂OTSUKA仍占据约59%的市场份额,APOTEX CORP和Teva分别占据约11%和9%的市场份额,仿制药正在逐步蚕食市场。华海药业凭借其于2011年获得的阿立哌唑DMF以及Solco的现有销售渠道和原料药优势,有望在美国市场获得一定的市场份额。
国内市场展望:高速增长与政策红利
国内阿立哌唑市场呈现高速增长态势。根据终端数据,其销售额从2010年的2亿人民币增长至2016年的8.74亿人民币,复合年均增长率(CAGR)高达26.89%。截至2017年第三季度,国内市场竞争格局中,大冢制药的市场份额超过50%并持续提升,康弘药业市场份额约为34%并缓慢下降,中西制药市场份额相对稳定,约为14%。随着阿立哌唑片进入国家医保甲类目录以及国内精神分裂症诊疗率的提高,预计国内市场空间将维持高速增长。华海药业有望通过海外上市品种转报国内的渠道优势,享受上市后的一致性评价政策红利。
华海药业核心投资逻辑
- 制剂出口: 华海药业通过十年投入成功打造“华海模式”,拥有成熟的高技术固体制剂仿制药研发、申报注册平台。其产品集群已形成,并通过Solco销售平台进入美国主流销售渠道,在多奈哌齐、缬沙坦等品种上具备竞争优势。公司后续申报产品多以缓控释等高毛利产品为主,并通过专利挑战实现业务质变。此外,公司还通过“制剂出口平台”与国内企业合作,实现“中国制造叠加美国渠道”的双赢模式。
- 国内制剂: 公司在国内市场已打通“优先审评审批”+“等同于通过一致性评价”+“招标优势”的逻辑,正等待产品批量上市。通过合作销售和自建销售团队,公司加速推广优势产品。长期来看,随着医保支付价、两票制等政策的执行,医药行业正从“市场销售”导向型转向以“研发、产品”为主的阶段,华海药业完全符合这一发展趋势。
- 原料药: 原料药业务是公司的基石,新品种和产能释放保证了稳定增长,提供了持续现金流,并确保了公司产品的质量、成本优势和供应链的稳定。
- 生物药: 公司在高仿生物药(biosimilar)领域进行布局,目前有产品处于临床阶段,旨在通过生物类似药的优势节省注册时间和临床费用,其中针对TNFα的生物类似药进展较快,同时也有生物创新药在研。
财务预测与投资评级
报告预计华海药业2017年至2019年的净利润将分别达到6.40亿、7.54亿和9.86亿人民币。考虑到公司在制剂出口领域的龙头地位、国内制剂业务的巨大潜力以及单抗业务的长期布局,国金证券维持对华海药业的“买入”评级。
潜在风险因素
报告提示了多项潜在风险,包括ANDA获批速度可能不达预期(因FDA积压和审批速度可能低于预期)、国内审批慢于预期(CFDA人力不足,尤其在海外飞行检查审评员方面)、销售慢于预期(新药品定价和准入体系尚未形成,医院“一品双规”等政策限制可能影响产品上市后销售),以及环保风险(国内环保标准提高和检查从严可能带来环保压力)。
总结
华海药业凭借阿立哌唑片在美国市场的成功获批,进一步巩固了其在国际制剂出口领域的领先地位,并为该品种在国内市场的上市和增长奠定了基础。公司通过“华海模式”在制剂出口方面形成核心竞争力,同时积极布局国内制剂市场,受益于政策红利。原料药业务提供稳定支撑,生物药领域则展现长期增长潜力。尽管面临ANDA审批、国内销售及环保等风险,但基于其强大的研发实力、国际化布局和国内市场策略,华海药业的未来业绩增长可期,因此维持“买入”评级。
-

基础化工行业研究:双碳考核细则落地,碳中和政策延续有效,供给端影响逐步落地
-

医药工业增长稳健,创新成果逐步兑现
-

业绩持续高增长,盈利能力稳健
-

业绩平稳增长,营销改革有望贡献新增量
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送