-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用
立即咨询
产品矩阵


摩熵数科产品矩阵
查看详情
{{ item.category }}
{{ product.info.desc }}

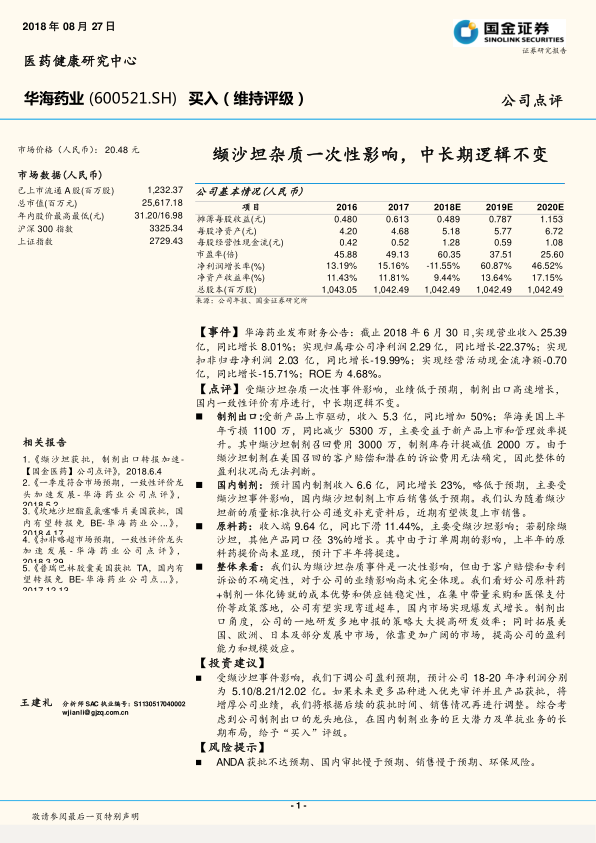
缬沙坦杂质一次性影响,中长期逻辑不变
研报
缬沙坦杂质一次性影响,中长期逻辑不变
# 中心思想
## 缬沙坦事件影响分析:短期冲击与长期价值
本报告核心观点如下:
* **短期业绩受挫:** 华海药业因缬沙坦杂质事件导致短期业绩低于预期,但剔除该因素影响,公司整体运营仍保持增长态势。
* **长期逻辑不变:** 公司制剂出口业务高速增长,国内一致性评价有序推进,原料药+制剂一体化优势显著,长期发展逻辑未变。
* **投资评级维持:** 尽管下调了公司盈利预期,但考虑到公司在制剂出口、国内制剂业务以及单抗业务的长期布局,维持“买入”评级。
# 主要内容
## 财务数据与业绩表现
* **营收与净利润:** 2018年上半年营收25.39亿元,同比增长8.01%;归母净利润2.29亿元,同比下降22.37%。
* **现金流:** 经营活动现金流净额-0.70亿元,同比下降-15.71%。
* **盈利能力:** ROE为4.68%。
## 制剂出口业务
* **收入增长:** 制剂出口收入5.3亿元,同比增长50%,主要受益于新产品上市驱动。
* **盈利改善:** 华海美国上半年亏损1100万,同比减少5300万,得益于新产品上市和管理效率提升。
* **缬沙坦影响:** 缬沙坦制剂召回费用3000万,制剂库存计提减值2000万,客户赔偿和潜在诉讼费用尚无法确定。
* **市场拓展:** 公司已有55个产品自主拥有美国ANDA文号,其中15个自主销售的制剂产品市场份额领先;12 个产品在欧盟 24 个国家获批上市。
* **全球化战略:** 通过自有市场的拓展、日本产品引进及合作等方式积极拓展日本市场,德国公司已成立并准备下阶段运营工作,全球化战略稳步推进。
## 国内制剂业务
* **收入增长:** 预计国内制剂收入6.6亿元,同比增长23%,略低于预期,主要受缬沙坦事件影响。
* **恢复预期:** 随着缬沙坦新的质量标准执行公司递交补充资料后,近期有望恢复上市销售。
* **一致性评价:** 截至目前,公司共有 10 个品种(15 个品规)通过一致性评价。
* **新产品上市:** 今年以来,公司完成 4 个新产品申报生产, 5 个产品完成注册申请,缬沙坦片、伏立康唑片及罗库溴铵注射剂获得国家药品生产注册批件,新产品的上市加速国内制剂的腾飞发展。
* **发展前景:** 随着国内一致性评价政策和药品带量集中采购、医保支付价的影响,华海药业有望实现国内产品的后来居上,实现爆发式发展。
* **产业链延伸:** 参股湖北共同药业,保证公司甾体激素类原料药的供应,延续原料药+制剂一体化的产业竞争策略。
## 原料药业务
* **收入下滑:** 收入端9.64亿,同比下滑11.44%,主要受缬沙坦影响;若剔除缬沙坦,其他产品同口径3%的增长。
* **价格调整:** 由于订单周期的影响,上半年的原料药提价尚未显现,预计下半年将提速。
* **研发进展:** 报告期内,公司原料药获得注册批件 4 个,新申报注册项目 6个,启动技改项目5个。
## 缬沙坦召回事件影响
* **财务影响:** 整体影响收入1.7亿,利润约1亿。其中原料药退回约5000万,美国缬沙坦制剂召回的渠道费用 3000 万,缬沙坦制剂计提减值约2000 万。
* **召回进展:** 公司已完成国内缬沙坦原料药的召回工作,正积极推进国外缬沙坦原料药召回工作。美国上市的在有效期内的缬沙坦制剂产品已部分召回。
* **工艺改进:** 公司缬沙坦新工艺验证已经完成,新工艺相关材料正在整理,以期尽快上报各药监部门等待审批。
## 研发投入与项目进展
* **研发费用:** 研发费用 1.81 亿,同比保持稳健。
* **创新药研发:** I 类生物新药重组人血管内皮生长因子受体-抗体融合蛋白眼用注射液(HB002.1M)I 期临床试验进展顺利。
* **生物类似药:** 生物类似药重组全人源抗肿瘤坏死因子-α单克隆抗体注射液获得药物临床试验批件。
* **新药研发:** 注射用双羟萘酸多奈哌齐已取得临床试验批件,盐酸羟哌吡酮完成临床IIA期研究,正在启动临床IIB研究。
## 财务分析
* **借款增加:** 短期借款增加 9 亿,长期借款增加 8 亿,导致公司 2018 年上半年财务费用增加 2500 万。
* **排污费增加:** 排污费 1.1 亿,同比增加接近 5000 万,主要公司针对废弃新增加设备约 5000万,预计下半年将与收入同步增长。
* **政府补助减少:** 政府补助 3460万,与上年同期减少1200万。
* **毛利率提高:** 整体毛利率58.11%,同比提高4个百分点。
* **应收账款增加:** 应收账款 17.55 亿,同比增长9.42%,占营业收入69%,同比提高6 个百分点。
## 一致性评价政策分析
* **政策支持:** 各地陆续出台鼓励政策,其中“量”方面多数可以直接挂网采购,新的市场准入途径形成;“价”方面以议价为核心,参照其他省份及历史价格。
* **转报优势:** 华海药业的缬沙坦应用全套的美国申请资料进行国内的转报,目前制剂出口转报从实操层面完全落地,公司在海外获批的产品有望通过该渠道加速上市。
* **产品储备:** 目前国内有13个品种申报待审批中,其中盐酸多奈哌齐片、盐酸度洛西汀肠溶胶囊、缬沙坦氢氯噻嗪片、伏立康唑片优先审评审批。
## 投资逻辑
* **制剂出口:** 十年投入成功创造“华海模式”,拥有成熟的高技术固体制剂仿制药研发、申报注册平台,现有产品集群已经形成。
* **国内制剂:** “优先审评审批”+“等同于通过一致性评价”+“招标优势”国内逻辑完全打通,静待产品批量上市。
* **原料药:** 公司的业务的基石,新品种和产能释放保证稳定增长,带来持续现金流,保证公司的产品质量、成本优势和供应链的稳定。
* **生物药:** 高仿产品,目前临床中,以 biosimilar 优势节省注册时间和临床费用,其中针对TNFα的 biosimilar进展较快,并有生物创新药在研。
# 总结
## 核心业务稳健,长期发展可期
华海药业短期业绩受到缬沙坦事件的影响,但公司制剂出口业务保持高速增长,国内一致性评价有序进行,原料药业务稳健发展。公司原料药+制剂一体化的产业链优势、全球化布局以及创新药研发投入,将支撑其长期发展。维持“买入”评级,但需关注ANDA获批、国内审批、销售以及环保等风险。
报告专题:
-
下载次数:
2285 次
-
发布机构:
国金证券股份有限公司
-
发布日期:
2018-08-30
-
页数:
10页
下载全文
定制咨询
AI精读报告
中心思想
缬沙坦事件影响分析:短期冲击与长期价值
本报告核心观点如下:
- 短期业绩受挫: 华海药业因缬沙坦杂质事件导致短期业绩低于预期,但剔除该因素影响,公司整体运营仍保持增长态势。
- 长期逻辑不变: 公司制剂出口业务高速增长,国内一致性评价有序推进,原料药+制剂一体化优势显著,长期发展逻辑未变。
- 投资评级维持: 尽管下调了公司盈利预期,但考虑到公司在制剂出口、国内制剂业务以及单抗业务的长期布局,维持“买入”评级。
主要内容
财务数据与业绩表现
- 营收与净利润: 2018年上半年营收25.39亿元,同比增长8.01%;归母净利润2.29亿元,同比下降22.37%。
- 现金流: 经营活动现金流净额-0.70亿元,同比下降-15.71%。
- 盈利能力: ROE为4.68%。
制剂出口业务
- 收入增长: 制剂出口收入5.3亿元,同比增长50%,主要受益于新产品上市驱动。
- 盈利改善: 华海美国上半年亏损1100万,同比减少5300万,得益于新产品上市和管理效率提升。
- 缬沙坦影响: 缬沙坦制剂召回费用3000万,制剂库存计提减值2000万,客户赔偿和潜在诉讼费用尚无法确定。
- 市场拓展: 公司已有55个产品自主拥有美国ANDA文号,其中15个自主销售的制剂产品市场份额领先;12 个产品在欧盟 24 个国家获批上市。
- 全球化战略: 通过自有市场的拓展、日本产品引进及合作等方式积极拓展日本市场,德国公司已成立并准备下阶段运营工作,全球化战略稳步推进。
国内制剂业务
- 收入增长: 预计国内制剂收入6.6亿元,同比增长23%,略低于预期,主要受缬沙坦事件影响。
- 恢复预期: 随着缬沙坦新的质量标准执行公司递交补充资料后,近期有望恢复上市销售。
- 一致性评价: 截至目前,公司共有 10 个品种(15 个品规)通过一致性评价。
- 新产品上市: 今年以来,公司完成 4 个新产品申报生产, 5 个产品完成注册申请,缬沙坦片、伏立康唑片及罗库溴铵注射剂获得国家药品生产注册批件,新产品的上市加速国内制剂的腾飞发展。
- 发展前景: 随着国内一致性评价政策和药品带量集中采购、医保支付价的影响,华海药业有望实现国内产品的后来居上,实现爆发式发展。
- 产业链延伸: 参股湖北共同药业,保证公司甾体激素类原料药的供应,延续原料药+制剂一体化的产业竞争策略。
原料药业务
- 收入下滑: 收入端9.64亿,同比下滑11.44%,主要受缬沙坦影响;若剔除缬沙坦,其他产品同口径3%的增长。
- 价格调整: 由于订单周期的影响,上半年的原料药提价尚未显现,预计下半年将提速。
- 研发进展: 报告期内,公司原料药获得注册批件 4 个,新申报注册项目 6个,启动技改项目5个。
缬沙坦召回事件影响
- 财务影响: 整体影响收入1.7亿,利润约1亿。其中原料药退回约5000万,美国缬沙坦制剂召回的渠道费用 3000 万,缬沙坦制剂计提减值约2000 万。
- 召回进展: 公司已完成国内缬沙坦原料药的召回工作,正积极推进国外缬沙坦原料药召回工作。美国上市的在有效期内的缬沙坦制剂产品已部分召回。
- 工艺改进: 公司缬沙坦新工艺验证已经完成,新工艺相关材料正在整理,以期尽快上报各药监部门等待审批。
研发投入与项目进展
- 研发费用: 研发费用 1.81 亿,同比保持稳健。
- 创新药研发: I 类生物新药重组人血管内皮生长因子受体-抗体融合蛋白眼用注射液(HB002.1M)I 期临床试验进展顺利。
- 生物类似药: 生物类似药重组全人源抗肿瘤坏死因子-α单克隆抗体注射液获得药物临床试验批件。
- 新药研发: 注射用双羟萘酸多奈哌齐已取得临床试验批件,盐酸羟哌吡酮完成临床IIA期研究,正在启动临床IIB研究。
财务分析
- 借款增加: 短期借款增加 9 亿,长期借款增加 8 亿,导致公司 2018 年上半年财务费用增加 2500 万。
- 排污费增加: 排污费 1.1 亿,同比增加接近 5000 万,主要公司针对废弃新增加设备约 5000万,预计下半年将与收入同步增长。
- 政府补助减少: 政府补助 3460万,与上年同期减少1200万。
- 毛利率提高: 整体毛利率58.11%,同比提高4个百分点。
- 应收账款增加: 应收账款 17.55 亿,同比增长9.42%,占营业收入69%,同比提高6 个百分点。
一致性评价政策分析
- 政策支持: 各地陆续出台鼓励政策,其中“量”方面多数可以直接挂网采购,新的市场准入途径形成;“价”方面以议价为核心,参照其他省份及历史价格。
- 转报优势: 华海药业的缬沙坦应用全套的美国申请资料进行国内的转报,目前制剂出口转报从实操层面完全落地,公司在海外获批的产品有望通过该渠道加速上市。
- 产品储备: 目前国内有13个品种申报待审批中,其中盐酸多奈哌齐片、盐酸度洛西汀肠溶胶囊、缬沙坦氢氯噻嗪片、伏立康唑片优先审评审批。
投资逻辑
- 制剂出口: 十年投入成功创造“华海模式”,拥有成熟的高技术固体制剂仿制药研发、申报注册平台,现有产品集群已经形成。
- 国内制剂: “优先审评审批”+“等同于通过一致性评价”+“招标优势”国内逻辑完全打通,静待产品批量上市。
- 原料药: 公司的业务的基石,新品种和产能释放保证稳定增长,带来持续现金流,保证公司的产品质量、成本优势和供应链的稳定。
- 生物药: 高仿产品,目前临床中,以 biosimilar 优势节省注册时间和临床费用,其中针对TNFα的 biosimilar进展较快,并有生物创新药在研。
总结
核心业务稳健,长期发展可期
华海药业短期业绩受到缬沙坦事件的影响,但公司制剂出口业务保持高速增长,国内一致性评价有序进行,原料药业务稳健发展。公司原料药+制剂一体化的产业链优势、全球化布局以及创新药研发投入,将支撑其长期发展。维持“买入”评级,但需关注ANDA获批、国内审批、销售以及环保等风险。
如果您有其他需求,请点击
定制服务咨询
国金证券股份有限公司最新报告
-

基础化工行业研究:双碳考核细则落地,碳中和政策延续有效,供给端影响逐步落地
-

医药工业增长稳健,创新成果逐步兑现
-

业绩持续高增长,盈利能力稳健
-

业绩平稳增长,营销改革有望贡献新增量
关于摩熵咨询
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案
1W+
医药行业研究报告
200+
真实项目案例
1300+
业内高端专家资源

市场洞察与营销赋能
分析市场现状,洞察行业趋势,依托数据分析和深度研究,辅助商业决策。

立项评估及管线规划
提供疾病领域品种调研、专家访谈、品种立项、项目交易整套服务。

产业规划及研究服务
以数据为基础,为组织、园区、企业提供科学的决策依据和趋势线索。

多渠道数据分析及定制服务
帮助客户深入了解目标领域和市场情况,发现潜在机会,优化企业决策。

投资决策与交易估值
依托全球医药全产业链数据库与顶级投行级分析模型,为并购、融资、IPO提供全周期决策支持。

立即定制
对不起!您还未登录!请登陆后查看!
立即登录
您今日剩余【10】次下载额度,确定继续吗?
取消
确定
确定
获取定制报告
请填写你的需求,我们将尽快与您取得联系
姓名
{{nameTip}}
单位
{{companyTip}}
电话
{{telTip}}
验证码
{{sms_codeTip}}
{{ setTime ? `${second}s` : '获取验证码' }}
邮箱
{{emailTip}}
需求描述
{{descriptionTip}}
提交
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送