-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

能力全面的创新药公司,Nectin-4 ADC进度领先
能力全面的创新药公司,Nectin-4 ADC进度领先
-
下载次数:
1850 次
-
发布机构:
国信证券股份有限公司
-
发布日期:
2024-02-01
-
页数:
45页
迈威生物(688062)
报告摘要
迈威生物:能力全面的创新药公司,Nectin-4ADC进度领先。迈威生物成立于2017年,公司通过收购、整合、自建等方式,快速具备了研发、生产与商业化的能力。目前公司已有两款生物类似药处于商业化阶段,并与国内外的多家公司达成了广泛的商业化合作。公司的研发管线覆盖肿瘤、自免、代谢等领域,核心产品9MW2821是全球第二款进入3期临床的Nectin-4ADC,研发进度较为领先。
9MW2821:进度最快的国产Nectin-4ADC。Seagen与安斯泰来联合开发的Enfortumab vedotin(PADCEV)是全球唯一获批上市的Nectin-4ADC,PADCEV与K药联用临床数据惊艳,预计将成为一线尿路上皮癌(UC)患者的标准治疗。同时,Nectin-4ADC具备向早期膀胱癌以及宫颈癌等其他瘤种拓展的潜力,有望成为全球范围内的重磅品种。9MW2821已经开启了后线UC的3期临床,临床进度大幅领先后续的国产分子,预计将成为全球第二款获批上市的Nectin-4ADC。9MW2821展现出了优秀的早期有效性和安全性数据,具备一定的差异化竞争优势。
生物类似药迎来收获,创新管线厚积薄发。君迈康(阿达木单抗)和迈利舒(地舒单抗骨松适应症)是公司已经实现商业化的两款生物类似药;除此之外,9MW0321(地舒单抗骨转适应症)和8MW0511(长效G-CSF)也已申报上市。公司的生物类似药正处于销售爬坡期,预计未来将为公司带来可观的现金流。除了9MW2821外,公司的9MW1911(ST2单抗)、9MW3011(TMPRSS6单抗)和9MW3811(IL-11单抗)临床进度在全球范围内均处于较为靠前的位置,将成为公司后续成长的重要驱动力。
投资建议:Nectin-4ADC有望成为重磅品种,首次覆盖,给予“增持”评级。迈威生物的核心产品9MW2821有望凭借优秀的临床数据和领先的研发进度,在国内的UC市场占据主要地位,并且具备出海的潜力。公司的生物类似药销售预计将进入快速增长阶段。我们暂不考虑9MW2821在海外市场的预期。我们预计2023~2025年公司的营收分别为1.40/4.17/8.87亿元,同比增长405%/198%/113%,归母净利润-9.86/-6.82/-4.35亿元。采用绝对估值方法,我们得到公司的合理估值区间为121~139亿元,对应股价30.2~34.8元/股,相对当前股价有16%~33%的上涨空间;首次覆盖,给予“增持”评级。
中心思想
迈威生物:创新驱动与全产业链布局的生物制药企业
迈威生物(688062.SH)作为一家成立于2017年的创新药公司,凭借前瞻性的战略布局,通过收购、整合与自建,迅速构建了涵盖研发、生产与商业化的全产业链能力。公司目前已有两款生物类似药成功实现商业化,并与国内外多家企业建立了广泛的商业合作网络。其研发管线深度覆盖肿瘤、自身免疫和代谢等多个高潜力治疗领域,其中核心产品9MW2821(Nectin-4 ADC)在全球同类产品中研发进度领先,已进入三期临床阶段,有望成为全球第二款获批上市的Nectin-4 ADC。
核心产品与生物类似药:双轮驱动未来增长
报告强调,迈威生物的核心竞争力在于其领先的创新药管线和日益成熟的生物类似药业务。9MW2821作为国产Nectin-4 ADC的领跑者,在尿路上皮癌(UC)治疗领域展现出优异的早期临床有效性和安全性数据,具备显著的差异化竞争优势,预计将占据国内UC市场的重要份额并具备国际化潜力。同时,君迈康(阿达木单抗)和迈利舒(地舒单抗骨松适应症)等生物类似药正处于销售爬坡期,预计将为公司带来可观的现金流,为创新药的持续研发提供有力支撑。公司在研的9MW0321(地舒单抗骨转适应症)和8MW0511(长效G-CSF)也已申报上市,进一步丰富了产品组合。基于此,报告首次覆盖迈威生物并给予“增持”评级,预测公司营收将实现高速增长,并采用绝对估值法得出其合理估值区间为121~139亿元人民币。
主要内容
迈威生物:能力全面的创新药公司
全产业链布局与稳固股权结构
迈威生物自2017年成立以来,便致力于构建全面的生物制药能力。公司通过一系列战略性举措,包括收购、整合现有资源以及自建研发和生产设施,迅速形成了从药物发现、临床前研究、临床开发到商业化生产和销售的全产业链布局。这一前瞻性策略使得公司在短时间内具备了强大的运营能力。2022年,公司首个产品——阿达木单抗生物类似药(君迈康)成功获批上市,标志着其商业化能力的初步实现。截至目前,迈威生物已有两款生物类似药进入商业化阶段,并与国内外多家公司建立了广泛的商业合作关系,为其产品的市场渗透和全球拓展奠定了基础。
在股权结构方面,迈威生物的实际控制人为唐春山、陈姗娜夫妇,他们合计控制公司42.39%的股权,确保了公司战略的稳定性和执行力。此外,公司还设立了中骏建隆、真珠投资等员工持股平台,覆盖了包括联合创始人刘大涛在内的近百名管理层及其他员工,有效激励了核心人才,增强了团队凝聚力。公司旗下设有多家子公司,各司其职,共同支撑其创新药研发体系:普铭生物、诺艾新、科诺信诚、迈威康和迈威(美国)专注于创新药发现及技术开发;迈威康负责临床前研究;泰康生物从事抗体与重组蛋白的研发及生产;迈威丽水则专注于ADC药物的研发。这种精细化的分工与协同,为公司多元化管线的推进提供了坚实的基础。
经验丰富的管理团队与多元化管线
迈威生物拥有一支在制药行业经验丰富的管理团队,这为公司的战略规划和执行提供了专业保障。例如,董事长刘大涛拥有药物化学博士学位和肿瘤药理博士后经历,曾任上海医药中央研究院副院长,在药物研发和管理方面具有深厚背景。董事唐春山作为资深医药投资人,曾成功打造青峰医药集团,为公司带来了丰富的产业经验和资源。这些核心管理人员的专业背景和行业影响力,是迈威生物快速发展的重要驱动力。
公司的在研管线布局广泛,主要集中在肿瘤、自身免疫和代谢等高发病率和未满足临床需求领域。目前,公司已有两款生物类似药成功上市销售:君迈康(阿达木单抗)和迈利舒(地舒单抗骨松适应症),这两款产品为公司带来了稳定的收入来源。此外,9MW0321(地舒单抗骨转适应症)和8MW0511(长效G-CSF)也已提交上市申请,预计将进一步丰富公司的商业化产品组合。
在创新药方面,迈威生物的核心产品9MW2821(Nectin-4 ADC)的研发进度在全球范围内处于领先地位,是全球第二款进入临床开发阶段的Nectin-4 ADC新药,目前已在中国进入尿路上皮癌的三期临床试验。除了9MW2821,公司还有多款创新药处于临床早期阶段,包括9MW1911(ST2单抗)、9MW3011(TMPRSS6单抗)和9MW3811(IL-11单抗),这些产品在全球同靶点研发中均处于较为靠前的位置,预示着公司未来持续增长的强大潜力。这种“生物类似药提供现金流,创新药驱动未来增长”的双轮驱动策略,使得迈威生物在激烈的市场竞争中具备了独特的优势。
9MW2821:进度最快的国产Nectin-4 ADC
Nectin-4靶点潜力与膀胱癌市场分析
Nectin-4作为黏连蛋白家族的一员,在多种实体瘤中表现出高表达,包括乳腺癌、卵巢癌、胰腺癌、宫颈癌和膀胱癌等,并与癌症的复发和不良预后密切相关。该蛋白通过调控WNT/β-catenin、PI3K-AKT等重要信号通路,参与肿瘤的增殖、转移、淋巴生成和血管生成等关键过程,因此被认为是癌症治疗中极具潜力的靶点。
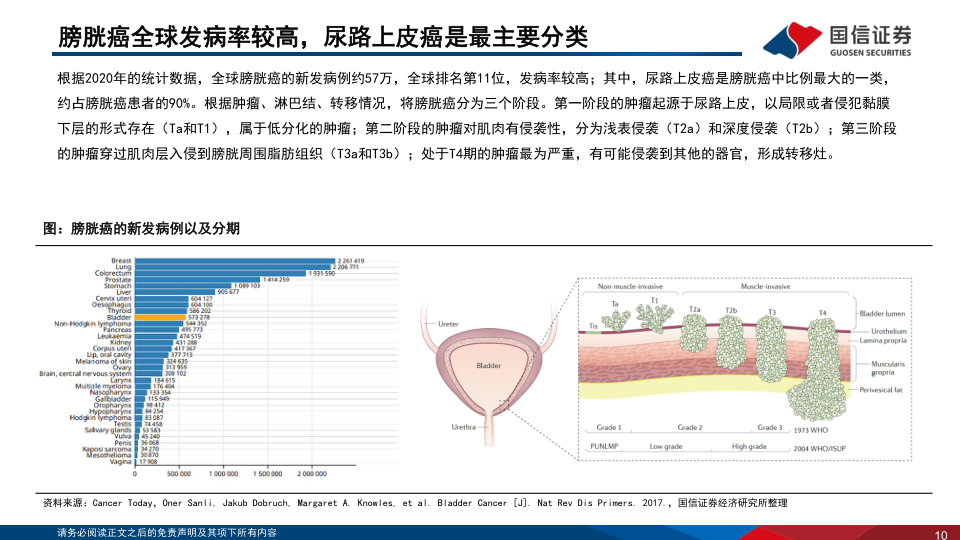
膀胱癌在全球范围内发病率较高。根据2020年的统计数据,全球膀胱癌新发病例约57万,位居全球第11位。其中,尿路上皮癌(UC)是膀胱癌中最主要的类型,约占膀胱癌患者的90%。膀胱癌的治疗范式根据肿瘤是否浸润膀胱肌层分为非肌层浸润性膀胱癌(NMIBC)和肌层浸润性膀胱癌(MIBC)。NMIBC的标准治疗手段是经尿道膀胱肿瘤切除术(TURBT)辅以膀胱灌注药物治疗。对于进展到肌层浸润性的MIBC,指南推荐采用根治性膀胱切除术。而对于疾病进一步进展、不可手术的患者,则采用放化疗、免疫治疗等系统用药。
Nectin-4 ADC(Enfortumab Vedotin/EV)已获得CSCO和NCCN临床指南的推荐,覆盖了转移性尿路上皮癌(mUC)的一线至三线治疗。特别是EV联合帕博利珠单抗(K药)的临床数据表现出色,已获得一线治疗的推荐,有望成为一线尿路上皮癌患者的标准治疗方案。Nectin-4 ADC还具备向早期膀胱癌以及宫颈癌等其他瘤种拓展的潜力,预示着其在全球范围内成为重磅品种的巨大市场前景。
EV市场表现与9MW2821的竞争优势
Enfortumab vedotin(EV,商品名:PADCEV®)是全球首款以Nectin-4为靶点的ADC创新药,由Seagen和安斯泰来联合开发。EV通过靶向表达Nectin-4的肿瘤细胞,内吞后释放MMAE(payload),促使肿瘤细胞凋亡并引起旁观者杀伤效应。自2019年底获美国FDA加速批准上市以来,PADCEV的销售额呈现快速增长态势。Seagen在2020-2022年录得PADCEV销售额分别为2.22亿美元、3.40亿美元和4.51亿美元。Astellas同期销售额分别为128亿日元(约0.9亿美元)、217亿日元(约1.5亿美元)和444亿日元(约3.1亿美元)。进入2023年,Seagen的PADCEV销售额继续强劲增长,Q1-Q3单季度销售额分别为1.19亿美元、1.61亿美元和2.00亿美元,同比增速分别达到19%、30%和90%。随着PADCEV联合K药的一线适应症获批,其销售额有望进一步爆发,并具备向早期膀胱癌(MIBC)拓展的潜力,有望成为全球重磅炸弹级产品。
EV的临床数据也十分亮眼:
- EV-201(II期单臂试验):在接受过免疫治疗且含铂化疗不耐受的mUC患者(n=89)中,EV单药治疗的客观缓解率(ORR)达到51%,其中完全缓解(CR)22%,部分缓解(PR)28%,中位缓解持续时间(mDOR)达到13.8个月。
- EV-301(III期确证性临床):EV单药治疗接受过免疫治疗及含铂化疗的mUC患者,与化疗组相比,中位总生存期(mOS)为12.9个月 vs 9.0个月(HR=0.70,p=0.0014),中位无进展生存期(mPFS)为5.6个月 vs 3.7个月(HR=0.62,p<0.0001),ORR为40.6% vs 17.9%。
- EV-103(I/II期多队列临床):在121名一线mUC患者(含铂化疗不耐受)中,EV联合K药的整体ORR达到68%,其中CR=12%,PR=55%,mDOR=22.1个月。
- EV-302(III期临床):一线治疗mUC患者,EV+K药组与含铂化疗组相比,mPFS为12.5个月 vs 6.3个月(HR=0.45),mOS为31.5个月 vs 16.1个月(HR=0.47),ORR为67.7% vs 44.4%,其中CR=29.1% vs 12.5%。EV+K药联用组的安全性良好,多数不良反应为1级/2级。
迈威生物开发的9MW2821是全球第二款进入临床开发阶段的Nectin-4 ADC新药,于2021年11月获得NMPA临床许可,2022年8月获得FDA临床许可。该产品采用公司自主知识产权的IDconnectTM桥连定点偶联技术,确保了偶联药物抗体部分与MMAE连接的DAR值均一(DAR=4比例≥95%),且碎片峰更少(≤3%),相较于已上市的Nectin-4 ADC药物具有一定的差异化竞争优势。
9MW2821的临床数据也表现出色:
- 在2023年ESMO会议上公布的ph1/2临床试验中,97名实体瘤患者接受0.33-1.5mg/kg的9MW2821治疗。在接受1.25mg/kg或以上剂量的39例实体瘤可评估患者中,ORR=38.5%,临床客观缓解率(cORR)=33.3%,疾病控制率(DCR)=84.6%。
- 在接受1.25mg/kg剂量9MW2821治疗的UC患者(既往接受过铂类化疗和免疫检查点抑制剂治疗)中,ORR=55.6%,cORR=50.0%,DCR=94.4%。
- 近期公司公告披露,在II期临床1.25mg/kg剂量组下,单药治疗晚期尿路上皮癌患者的ORR和DCR分别为62.2%(95%CI:44.8%-77.5%)和91.9%(95%CI:78.1%-98.3%),中位PFS为6.7个月,中位OS尚未达到。
根据销售测算模型,9MW2821在UC 2L+(单药)适应症下,预计2027年销售额可达8.88亿元人民币;在UC 1L(+PD1单抗)适应症下,预计2027年销售额可达9.50亿元人民币。综合来看,9MW2821在晚期尿路上皮癌市场具有成为大单品的巨大潜力,预计2027年合计销售额将达到16.53亿元人民币。
生物类似药迎来收获,创新管线厚积薄发
生物类似药市场进展与现金流贡献
迈威生物的生物类似药业务正逐步进入收获期,为公司提供稳健的现金流,支持其创新药的研发投入。
迈利舒(地舒单抗生物类似药):地舒单抗是靶向RANKL的单克隆抗体,通过抑制破骨细胞活性来减少骨吸收,增加骨量。原研安进的地舒单抗(安加维/普罗力)在2022年全球销售额高达56.42亿美元,是全球范围内的重磅药物。迈威生物开发的迈利舒已于2023年3月底获得中国上市许可批准,用于骨折高风险的绝经后妇女骨质疏松症治疗。截至2023年三季度末,迈利舒已实现销售额2343万元。尽管骨质疏松适应症适用人群广泛,但患者用药频次较低(一年两次),产品正处于销售爬坡期。此外,公司地舒单抗的骨转移适应症(商品名:迈卫健)也已提交上市申请,有望进一步拓展市场。目前中国市场已有安加维、普罗力(安进)、LY06006(绿叶制药)、迈利舒(迈威生物)和鲁可欣(齐鲁制药)等多款地舒单抗产品上市,竞争逐渐加剧。
君迈康(阿达木单抗生物类似药):君迈康(9MW0113)是迈威生物与君实生物合作开发的阿达木单抗生物类似药,靶向TNF-α。原研药物艾伯维的修美乐(Humira)在2022年全球销售额高达212.37亿美元,是全球销售额最高的药品。阿达木单抗的适应症广泛,包括类风湿性关节炎、强直性脊柱炎和银屑病等,覆盖了庞大的患者群体。修美乐于2010年进入中国,并于2019年底首次进入医保。随着价格下降和纳入医保,阿达木单抗的渗透率有望迅速提升。目前,国内阿达木单抗市场已形成“7+1”的竞争格局,君迈康是第六款上市的生物类似药。2023年上半年,君迈康发货83,573支,已在25个省份招标挂网,新准入医院67家,累计准入医院172家,覆盖药店955家,君实生物确认收入6,800万元。
8MW0511(白蛋白融合长效G-CSF):8MW0511是一款注射用重组人血清白蛋白-人粒细胞集落刺激因子融合蛋白,适用于成年非髓性恶性肿瘤患者在接受骨髓抑制性抗癌药物治疗时,降低发热性中性粒细胞减少症的感染发生率。作为新一代长效G-CSF,8MW0511采用人血清白蛋白融合技术延长G-CSF在体内的半衰期,且制备过程避免了复杂的PEG化学修饰反应,生产工艺简单、成本较低。公司已就8MW0511与扬子江药业签署许可协议,后者获得其在中国的独家生产及商业化权益。目前国内已有7款长效G-CSF获批上市,其中6款采用PEG化技术,亿一生物/正大天晴的亿立舒采用Fc融合蛋白。国内长效G-CSF市场空间预计在百亿以上,8MW0511有望凭借其技术优势和合作渠道占据一席之地。
早期创新管线布局与全球领先地位
除了已上市和即将上市的生物类似药,迈威生物还拥有多项处于早期研发阶段的创新药管线,这些分子在全球同靶点研发中均处于较为领先的位置,展现了公司强大的创新能力和未来增长潜力。
- 9MW1911(ST2单抗):该产品正在进行慢性阻塞性肺疾病(COPD)适应症的ph1b/2a临床试验。ST2靶点在炎症和免疫疾病中扮演重要角色,9MW1911的进展有望为COPD患者带来新的治疗选择。
- 9MW3011(TMPRSS6单抗):该产品正在β-地中海贫血、真性红细胞增多症等适应症中进行ph1临床试验。TMPRSS6是铁代谢的关键调节因子,其单抗有望通过调节铁稳态来治疗相关血液疾病。公司已就9MW3011与美国DISC MEDICINE, INC.达成独家许可协议,授权除大中华和东南亚以外区域的开发、生产和商业化权益,并与Legrand合作授权哥伦比亚及厄瓜多尔的注册和商业化,体现了其国际化布局。
- 9MW3811(IL-11单抗):该产品正在进行肺纤维化适应症的1期临床试验。IL-11在纤维化疾病中发挥作用,9MW3811有望成为治疗肺纤维化的创新疗法。
这些早期创新管线的全球领先进度,不仅彰显了迈威生物在生物制药前沿领域的研发实力,也为公司未来的可持续发展和市场竞争力提供了坚实保障。公司通过与国内外多家企业达成合作协议,累计协议金额最高可达35.6亿元人民币,并可获得上市后的销售收益分成,进一步验证了其创新管线的市场价值和国际吸引力。
财务分析及投资建议
营收增长与费用控制
迈威生物的财务表现显示出其业务正处于快速发展阶段。2023年Q1-3,公司实现营收1.00亿元,同比增长387%,主要得益于子公司迈威(美国)就9MW3011项目与美国DISC MEDICINE, INC.达成独家许可协议确认的较高收入,以及迈利舒于2023年3月底获批上市后的销售贡献(截至三季度末销售2343万元)。尽管当前产品销售体量相对较小,但随着生物类似药的销售放量和创新药的陆续获批上市,预计公司未来营收将实现快速增长。
在费用控制方面,2023年Q1-3,公司的研发费用为4.94亿元,同比下降7.7%,显示出公司在研发投入保持高位的同时,对费用进行了合理控制。销售费用为1.61亿元,同比增长139.9%,这主要是由于地舒单抗获批上市后,公司加大了市场推广和销售团队建设的投入。管理费用为1.44亿元,同比增长4.5%,基本保持稳定。截至2023年9月30日,公司在手现金及现金等价物约18亿元人民币,充裕的现金储备足以支持公司未来两年以上的业务发展和研发投入。
产业化能力与商业化策略
迈威生物已具备强大的产业化能力,并为大规模商业化做好了充分准备。公司的泰州生产基地(泰康生物)已按照中国GMP、美国FDA cGMP和欧盟EMA GMP标准完成建设并投入使用。该基地拥有三条原液生产线和两条制剂生产线,抗体药物产能达到8,000L,重组蛋白药物产能达到4,000L,制剂生产线可满足一次性预充针和多个规格西林瓶的灌装需求。截至2023年年中,该基地已完成9个在研品种的临床试验样品制备,并成功进行了1个品种的商业化生产,所有批次样品均检定合格,充分验证了其生产能力和质量控制水平。
为应对未来产品放量需求,迈威生物还在积极扩建产能。上海金山基地总占地面积6.97万平方米,正参照国际高标准建设1000kg抗体产业化项目,其中2条原液生产线和1条西林瓶制剂生产线已完成设备安装调试,即将试产。泰州基地的“中试产业化建设项目”也已完成相关公用工程及工艺设备安装调试,ADC车间已具备试生产能力。这些产能的扩建将为公司未来产品的商业化提供坚实的生产保障。
在商业化策略上,迈威生物采取了多元化的合作模式,积极拓展海外市场。公司主要布局南美、“一带一路”等新兴市场,这些地区拥有巨大的医药市场潜力和未满足的临床需求。例如,首款上市的9MW0113(君迈康)已签署覆盖10个国家的商业化推广协议。9MW0321(地舒单抗)也通过商业化合作方式签署了战略合作协议。此外,公司多个在研管线与国内外多家企业达成共同开发协议,累计协议金额最高可达35.6亿元人民币,并可获得上市后的销售收益分成,这不仅分散了研发风险,也加速了产品的市场化进程。
盈利预测与投资评级
基于对迈威生物产品管线、市场潜力及财务状况的深入分析,报告对公司进行了盈利预测和估值。
- 盈利预测:报告预计,公司已上市或即将上市的生物类似药将带来稳健增长的现金流,支撑公司未来2-3年的营收增长。核心产品9MW2821预计将在2027年获批上市,凭借其优秀的临床数据和后续适应症的拓展潜力,有望成为
-

基础化工行业专题:英伟达Rubin架构发布 CCL上游材料体系升级
-

医药生物2026ASCO年会摘要总结:关注国产双抗、ADC等创新分子
-

制冷剂行业点评:英美调整三代制冷剂淘汰节奏,利好中国制冷剂出口量价提升
-

高纯四氯化硅行业点评:光纤、半导体需求高速增长,高纯四氯化硅迎来量价齐升
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送