-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

抗疫品种添新元,复必泰二价苗获中国香港EUA
抗疫品种添新元,复必泰二价苗获中国香港EUA
-
下载次数:
873 次
-
发布机构:
国金证券股份有限公司
-
发布日期:
2022-11-21
-
页数:
4页
复星医药(600196)
事件
2022年11月19日,公司公告其许可项目进展:项目,是复星医药产业于2020年3月获得德国BioNTech授权,在约定许可区域内独家开发、商业化基于其专有的mRNA技术平台研发的、针对新冠病毒的疫苗产品;进展,是复必泰二价疫苗获中国香港紧急使用认可。
点评
复必泰二价新冠疫苗在中国香港和中国澳门获批EUA。(1)复必泰原始株/Omicron变异株BA.4-5二价疫苗(每剂30微克)已分别获前述监管特别许可,可用于当地12岁及以上人群加强接种。(2)这是已上市复必泰BNT162b2的迭代和补充。复必泰二价疫苗每剂含有15微克编码原始毒株刺突蛋白的mRNA和15微克编码奥密克戎BA.4/BA.5变异毒株刺突蛋白的mRNA。除了添加奥密克戎BA.4/BA.5刺突蛋白的mRNA序列外,疫苗的所有其他成分保持不变。(3)此前,2020年3月16日,公司已获BioNTech授权,在中国内地及港澳台地区独家开发及商业化基于其专有的mRNA技术平台研发的新冠疫苗。mRNA新冠疫苗复必泰已于2021年3月在港澳地区纳入政府接种计划,并于2021年9月在中国台湾地区开始接种。
防疫优化与第四针推进在即,mRNA疫苗进展为公司业绩与发展再添弹性。(1)公司此前早在2021年5月已与BioNTech签约,于上海设立合资公司,复星医药产业拟以现金/厂房/生产设施等、BioNTech以相关生产技术和专利技术许可等,各出资不超过1亿美元,各占50%注册资本。合资公司设立于中国上海,期限15年。规划年产能10亿剂mRNA新冠疫苗。合资公司的产品销售,将由复星医药产业之关联公司为CSO(不含港澳台),并支付后者相应费用。合资公司实现本地化生产和商业化之前,仍按原协议,即复星医药获得60-65%的毛利提成。(2)我们认为,公司在mRNA领域的抢先布局,是公司国际化专业决策力的佐证,为公司在此类前沿技术中抢得先机。(3)不过,mRNA疫苗的生产中,材料与过程都相对复杂,且复必泰二价苗在中国内地获批与否也存在较大的不确定性。
盈利预测、估值与评级
我们维持盈利预测,预计公司2022/23/24年营收449/517/597亿元,归母净利润39.84/53.73/66.55亿元。公司目前股价对应2022/23/24年PE为26/19/15倍。维持“买入”评级。
风险提示
新药研发及上市进程不达预期、集采等政策影响盈利能力等风险。
中心思想
mRNA疫苗进展驱动业绩增长
复星医药在mRNA疫苗领域的最新进展,特别是复必泰二价疫苗在中国香港和中国澳门获得紧急使用认可,是公司业绩增长和市场拓展的重要驱动力。这不仅巩固了公司在新冠疫苗市场的地位,也为其未来的国际化发展奠定了基础。
战略布局与财务展望
公司通过与BioNTech的深度合作及合资公司设立,展现了其在mRNA前沿技术领域的战略远见和抢先布局能力。尽管面临生产复杂性和中国内地审批的不确定性,但公司整体财务预测显示营收和归母净利润将持续增长,国金证券维持“买入”评级,凸显其长期投资价值。
主要内容
复必泰二价疫苗获批与市场影响
- 紧急使用认可: 2022年11月19日,复星医药公告其与德国BioNTech合作开发的复必泰二价新冠疫苗(原始株/Omicron变异株BA.4-5)获得中国香港紧急使用认可(EUA),随后在中国澳门也获批EUA,可用于当地12岁及以上人群的加强接种。
- 疫苗特性: 该二价疫苗是已上市复必泰BNT162b2的迭代和补充,每剂含有15微克编码原始毒株刺突蛋白的mRNA和15微克编码奥密克戎BA.4/BA.5变异毒株刺突蛋白的mRNA,疫苗的其他成分保持不变。
- 区域授权历史: 复星医药自2020年3月起获得BioNTech授权,在中国内地及港澳台地区独家开发及商业化其mRNA新冠疫苗。复必泰已于2021年3月在港澳地区纳入政府接种计划,并于2021年9月在中国台湾地区开始接种。
mRNA疫苗战略布局与挑战
- 合资公司设立: 为实现mRNA疫苗的本地化生产和商业化,复星医药于2021年5月与BioNTech签约,在上海设立合资公司,双方各出资不超过1亿美元,各占50%注册资本,规划年产能10亿剂。在本地化生产和商业化之前,复星医药可按原协议获得60-65%的毛利提成。
- 战略优势: 公司在mRNA领域的抢先布局,体现了其国际化专业决策力,使其在此类前沿技术中占据先机,为公司业绩与发展增添弹性。
- 潜在风险: mRNA疫苗的生产工艺相对复杂,材料与过程要求高。同时,复必泰二价疫苗在中国内地获批仍存在较大的不确定性。
盈利预测与投资评级
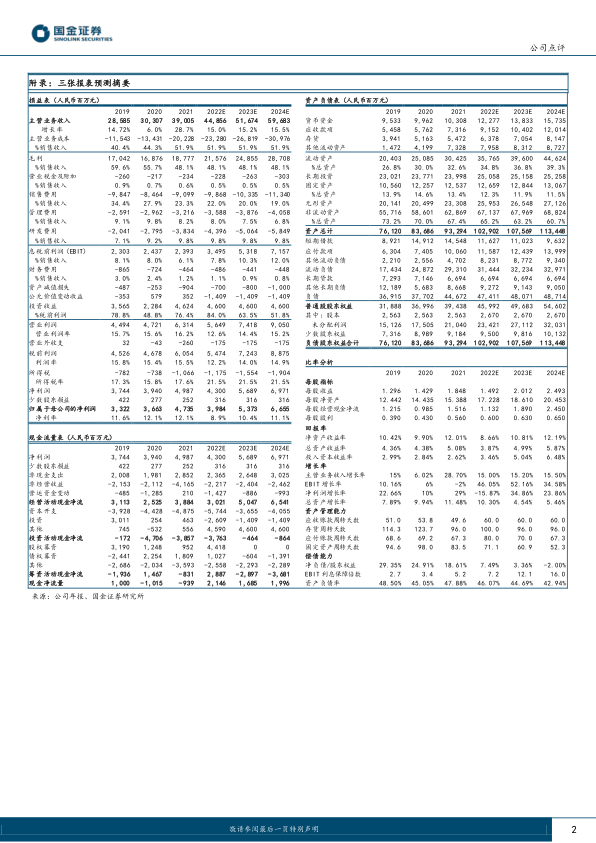
- 营收与净利润预测: 国金证券维持对复星医药的盈利预测,预计公司2022/2023/2024年营业收入分别为449亿元、517亿元和597亿元,归属于母公司净利润分别为39.84亿元、53.73亿元和66.55亿元。
- 估值分析: 基于当前股价,公司2022/2023/2024年市盈率(PE)分别为26倍、19倍和15倍。
- 投资建议: 维持“买入”评级。
- 风险提示: 主要风险包括新药研发及上市进程不达预期,以及集采等政策对盈利能力的影响。
财务数据概览与比率分析
- 营收增长: 预计2022-2024年营业收入将保持15%以上的增长率,显示公司业务持续扩张。
- 净利润波动: 归母净利润在2022年预计出现短期下滑(-15.87%),但随后在2023年和2024年将恢复高速增长(34.86%和23.86%),反映出业绩的韧性和未来增长潜力。
- 盈利能力: 净资产收益率(ROE)在2022年预计降至8.66%,但随后将回升至10.81%(2023E)和12.19%(2024E),表明公司盈利能力将逐步改善。
- 偿债能力: 净负债/股东权益比率预计将持续下降,从2022年的7.49%降至2024年的-2.00%,显示公司财务结构持续优化,偿债能力增强。
- 市场评级: 市场中相关报告普遍给予“买入”评级,历史推荐也均为“买入”,反映了市场对公司未来发展的普遍看好。
总结
复星医药凭借其与BioNTech合作的mRNA新冠疫苗项目,特别是复必泰二价疫苗在港澳地区的紧急使用认可,进一步巩固了其在疫苗市场的战略地位。公司在mRNA技术领域的抢先布局和合资公司的设立,为其未来的业绩增长和国际化发展提供了坚实基础。尽管面临生产复杂性和中国内地审批的不确定性,但国金证券维持对公司营收和净利润的积极增长预测,并重申“买入”评级,认为公司具备长期投资价值。同时,投资者需关注新药研发进展及政策变化带来的潜在风险。
-

基础化工行业研究:双碳考核细则落地,碳中和政策延续有效,供给端影响逐步落地
-

医药工业增长稳健,创新成果逐步兑现
-

业绩持续高增长,盈利能力稳健
-

业绩平稳增长,营销改革有望贡献新增量
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送