-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

2023年中国创新药研发报告
2023年中国创新药研发报告
-
下载次数:
979 次
-
发布机构:
重庆药智企业管理咨询
-
发布日期:
2024-12-26
-
页数:
26页
国内创新药申报和临床登情况
说明:本部分创新药包含按照现行《药品注册管理办法》(国家市场监督管理总局令第27号)注册分类中药、化药、生物制品1类和原《药品注册管理办法》(国家食品药品监督管理总局令第28号)注册分类中药1-6类、化药1.1类、生物制品1类受理的药品,其中包含国产创新药和进口创新药。统计时间截至2023年12月31日。
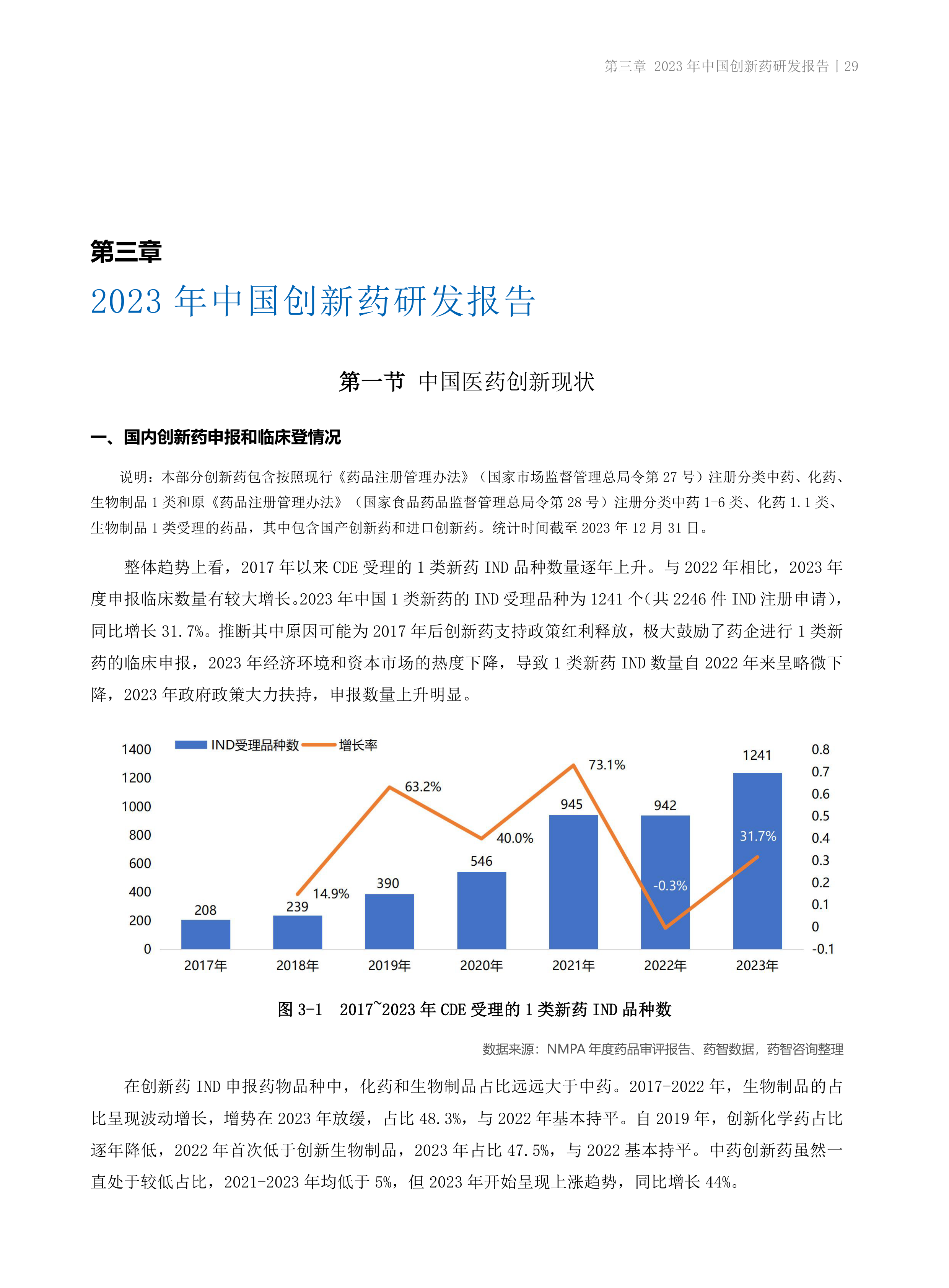
整体趋势上看,2017年以来CDE受理的1类新药IND品种数量逐年上升。与2022年相比,2023年度申报临床数量有较大增长。2023年中国1类新药的IND受理品种为1241个(共2246件IND注册申请),同比增长31.7%。推断其中原因可能为2017年后创新药支持政策红利释放,极大鼓励了药企进行1类新药的临床申报,2023年经济环境和资本市场的热度下降,导致1类新药IND数量自2022年来呈略微下降,2023年政府政策大力扶持,申报数量上升明显。
中心思想
中国创新药研发的蓬勃发展与国际化趋势
- 2023年中国创新药研发呈现强劲增长态势,IND申报数量和上市品种数量均显著增加,这主要得益于2017年后创新药支持政策的红利释放以及2023年政府政策的大力扶持。
- 创新药研发重心集中在肿瘤、血液等热点领域,新兴疗法如CGT(细胞疗法、基因疗法和寡核酸药物)和ADC(抗体偶联药物)持续增长,PD-L1、CD3、PD-1是目前主要的在研靶点。
- 中国创新药企业“出海”步伐加快,2023年License-out交易数量首次超过License-in,表明中国自主研发能力获得国际认可,多款国产新药成功获得FDA批准,开启了国产创新药的国际化征途。
改良型新药的机遇与挑战:临床价值、技术创新与资源整合
- 改良型新药市场发展迅速,但与美国相比,中国改良型新药的批准数量和治疗领域分布仍有差距,主要集中在抗肿瘤领域以及新剂型、新适应症的开发。
- 改良型新药的研发成功率高于创新药,但注册成功率略低,其研发需重点关注临床价值的考量、技术创新的硬实力以及人才和资金等资源的有效整合。
- 政策支持在推动改良型新药发展中发挥了关键作用,但企业仍需在确保产品具有“明显临床优势”的前提下,不断突破技术壁垒,以实现可持续发展。
主要内容
中国医药创新现状
国内创新药申报和临床登情况
- 2017年以来,CDE受理的1类新药IND品种数量逐年上升,2023年达到1241个(共2246件IND注册申请),同比增长31.7%。
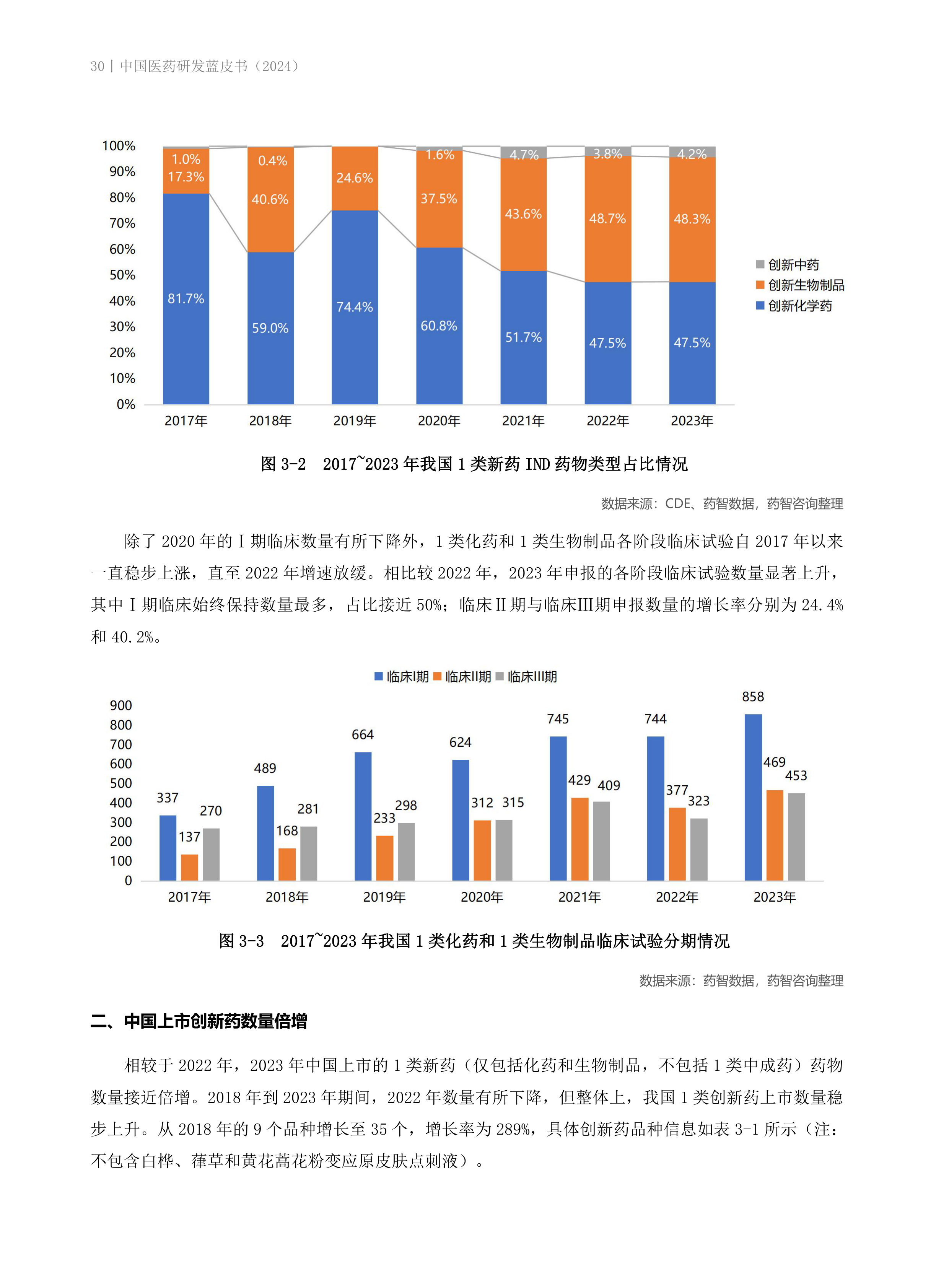
- 创新药IND申报中,化药和生物制品占比远大于中药。2023年生物制品占比48.3%,化药占比47.5%,两者基本持平;中药创新药占比虽低于5%,但2023年呈现44%的上涨趋势。
- 1类化药和1类生物制品各阶段临床试验数量自2017年稳步上涨,2023年显著上升,其中Ⅰ期临床数量最多,占比接近50%;临床Ⅱ期和Ⅲ期申报数量增长率分别为24.4%和40.2%。
中国上市创新药数量倍增
- 2023年中国上市的1类新药(仅包括化药和生物制品)数量接近倍增,从2018年的9个品种增长至2023年的35个,增长率为289%。
- 2018年至2023年累计上市创新药中,抗肿瘤药和免疫机能调节药占比最大(47%),其次是系统用抗感染药(22%)。
- 从药物类型看,化学药品占比达到72%,生物药品占比28%。
国内生物医药创新热点领域
创新药首次IND数量呈上升趋势
- 2023年我国首次IND创新药新品种数量为821个,同比增长16.4%,近四年总体复合增长率(CAGR)为25.1%。
- 国产生物药首次IND品种数量的近四年CAGR最高,达到47.0%,其次是国产中药(75.9%),而进口化药的CAGR为-7.7%。
创新药研发重心围绕肿瘤和血液领域,眼科领域受到关注
- 2023年国内IND新药申报适应症重点布局在肿瘤、血液疾病、心血管及感染领域,其中肿瘤领域近五年CAGR为21.9%。
- 近五年,眼科领域在国内受到关注,CAGR为31.7%。
创新药IND中CGT和ADC数量持续增长
- 国内首次IND新药类型分布中,申报重点集中于小分子化药和抗体。
- 新兴疗法中,CGT(细胞疗法、基因疗法和寡核酸药物)和ADC的创新药IND数量保持增长,近五年CAGR分别为65.7%和55.1%。
PD-L1/CD3/PD-1为创新药在研前三靶点
- 国内1类新药临床在研靶点中,与癌症治疗相关的靶点占据主要部分,如PD-L1、CD3、PD-1。
- 临床Ⅰ期药物占比最大(49.5%),PD-L1、PD-1、HER2、EGFR等靶点趋于研发成熟期,而CLDN18.2、CD137、CD19、MET等靶点正处于研发热
-

PIDC消费者洞察系列报告:探索:玻璃酸钠滴眼剂下一个增长点市场洞察与消费者研究
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






最新报告
- 核药:从“生物导弹”到诊疗一体化的变革
- 公司信息更新报告:2025年经营业绩稳健提升,创新布局赋能发展
- 26Q1非经营性因素影响减弱,向“医学智能诊断服务商”转型
- 1Q26 in line; overseas and emerging businesses driving growth
- 利润端高速增长,持续打造业绩增长新引擎
- 公司信息更新报告:2025年利润增速亮眼,整合资源深化创新中药布局
- 1Q26 results: a strong start driven by CDMO services
- 2025年报&2026一季报点评,乌灵系列稳健增长,“一路向 C”战略持续深化
- 公司信息更新报告:公司CGM业务稳定推进,海外市场拓展值得期待
- 医药行业专题报告:26Q1医药持仓回升,CXO等细分赛道现结构性机会
对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送