-
{{ listItem.name }}快速筛选药品,用摩熵药筛
 微信扫一扫-立即使用
微信扫一扫-立即使用

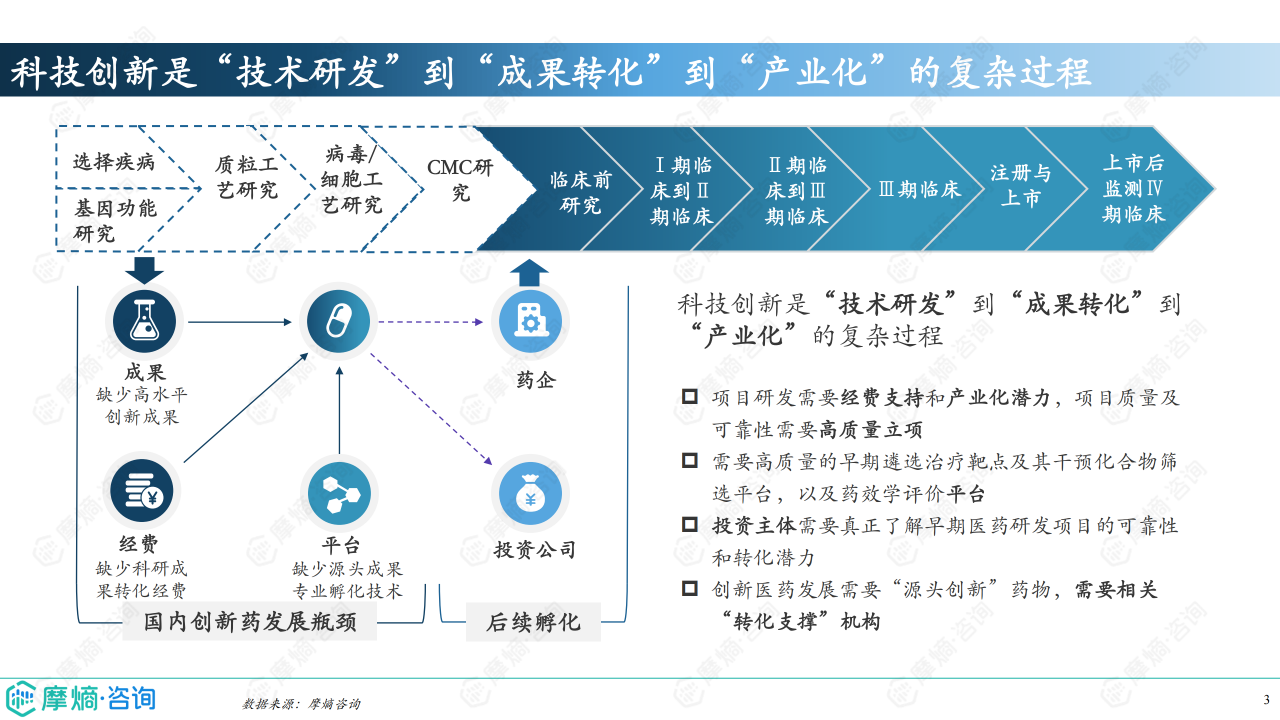
以终为始 ,数据助力高质量立项
高质量立项对医药行业至关重要,它确保研发项目与市场需求和企业战略相符,降低风险,提高资源利用效率,加速创新成果的市场转化,增强企业竞争力。本报告为医药行业带来了一场关于新药项目立项与仿制药产品线设计的深度洞察,报告不仅分析了当前医药行业的挑战与瓶颈,更提出了一系列切实可行的策略与建议,旨在帮助企业在激烈的市场竞争中做出明智的立项决策。
本报告涉及: 相关药物:盐酸美金刚片, 相关靶点:NMDA, 相关适应症:阿尔茨海默病 。
中心思想
本报告的核心观点是:高质量的新药立项需要“以终为始”,充分利用数据驱动决策,并结合公司战略、市场分析和风险评估等多方面因素进行综合考量。报告从新药项目的选择、评估(自研和引进项目)、仿制药产品线设计、信息获取渠道以及案例分析等方面,详细阐述了如何利用数据实现高质量立项。 具体而言,高质量立项需要:
- 清晰的疾病机制机理研究: 这是立项的前提条件。
- 基于大数据和KOL调研的未满足临床需求分析: 精准把握市场需求。
- 充分利用文献和专利数据: 探索新的方向和潜在机会。
- 完善的专利保护策略: 保障成果转化价值。
- 对现有产品、靶点、适应症和企业的全面分析: 了解竞争格局。
- 对临床试验结果的持续关注: 及时调整研发策略。
- 选择合适的CXO平台: 确保合作研究和代工生产的可行性。
- 关注行业热点和局限: 把握创新趋势。
主要内容
新药项目的选择
新药研发是一项高风险、高投入、周期长的复杂工程。选择适合公司自身战略发展的新药项目至关重要。公司需要考虑自身资金实力、人员数量和素质、场地大小、仪器设备、现有项目经验、管理制度、风险意识等实际情况,并结合发展战略和技术数据进行综合分析。 选择时应明确“世界上没有完美的新药项目”的真理,并根据现有数据,构建新药研发、生产、销售的完整模块,平衡风险与创新性,减少整体战略布局风险。技术数据解读应突出关键词:全面、显著的优势和劣势。发展战略可能根据自身情况不断调整,例如融资、强有力技术专家加盟、市场导向、现有项目取得重大突破等。
新药项目的评估
自研项目的评估
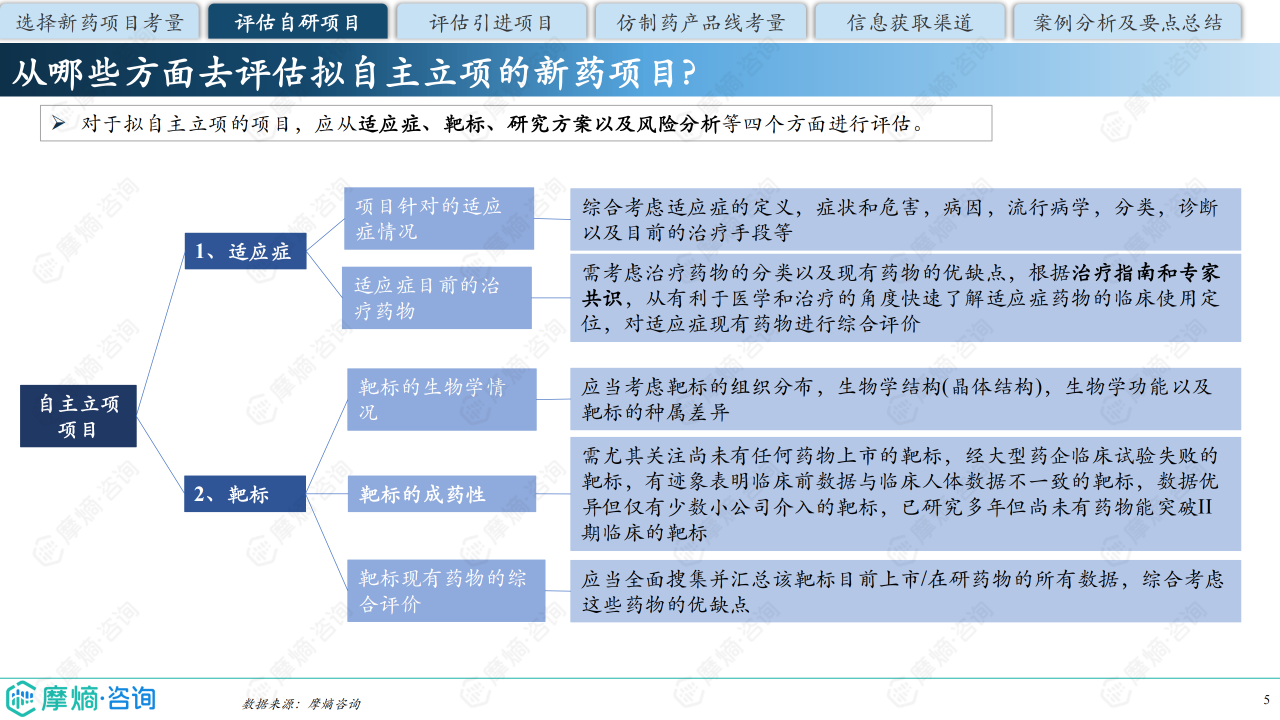
评估自研项目需从适应症、靶标、研究方案和风险分析四个方面进行评估。
- 适应症评估: 需考虑适应症的定义、症状、危害、病因、流行病学、分类、诊断以及目前的治疗手段等,并对现有药物进行综合评价。
- 靶标评估: 需考虑靶标的组织分布、生物学结构、生物学功能、种属差异以及成药性,并对现有药物进行综合评价,尤其关注尚未有药物上市、临床试验失败、临床前数据与临床人体数据不一致、数据优异但仅有少数小公司介入以及研究多年但尚未突破II期临床的靶标。
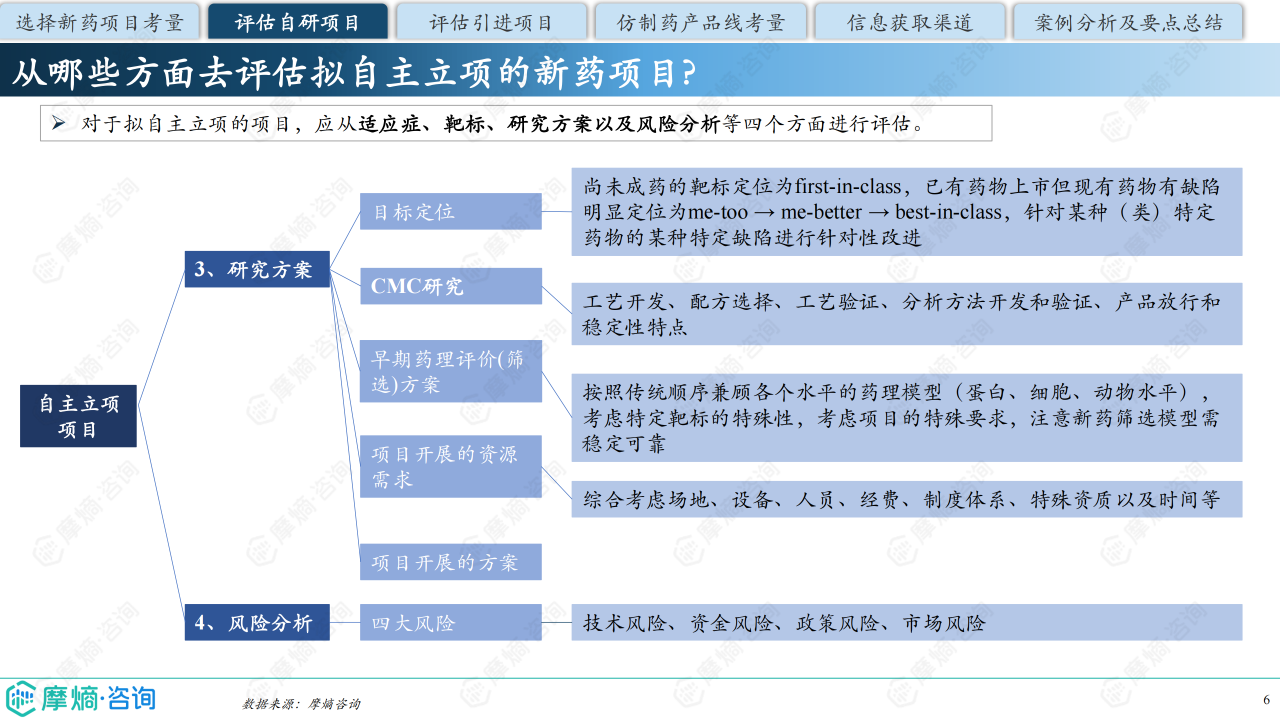
- 研究方案评估: 需考虑CMC研究(工艺开发、配方选择、工艺验证等)、早期药理评价方案(兼顾各个水平的药理模型)、项目开展的资源需求(场地、设备、人员、经费等)以及项目开展的方案。
- 风险分析: 需评估技术风险、资金风险、政策风险和市场风险。 项目目标定位应明确为first-in-class、me-too、me-better或best-in-class。
引进项目的评估
评估引进项目需考虑项目来源公司、项目转让动机、项目是否涉及特殊药物、专利布局、销售情况、技术数据以及是否与公司发展战略一致等八个方面。 需警惕项目存在重大技术或知识产权缺陷,以及项目转让方操纵价格等情况。 尤其需要关注特殊药物(强效药物、管制药物等)的研发、生产和流通成本以及监管要求。 此外,还需要分析上市后销售情况、竞争对手情况、药物流通情况(纳入基药目录和医保目录的可能性、进入OTC的可能性等)以及技术数据。
仿制药产品线设计
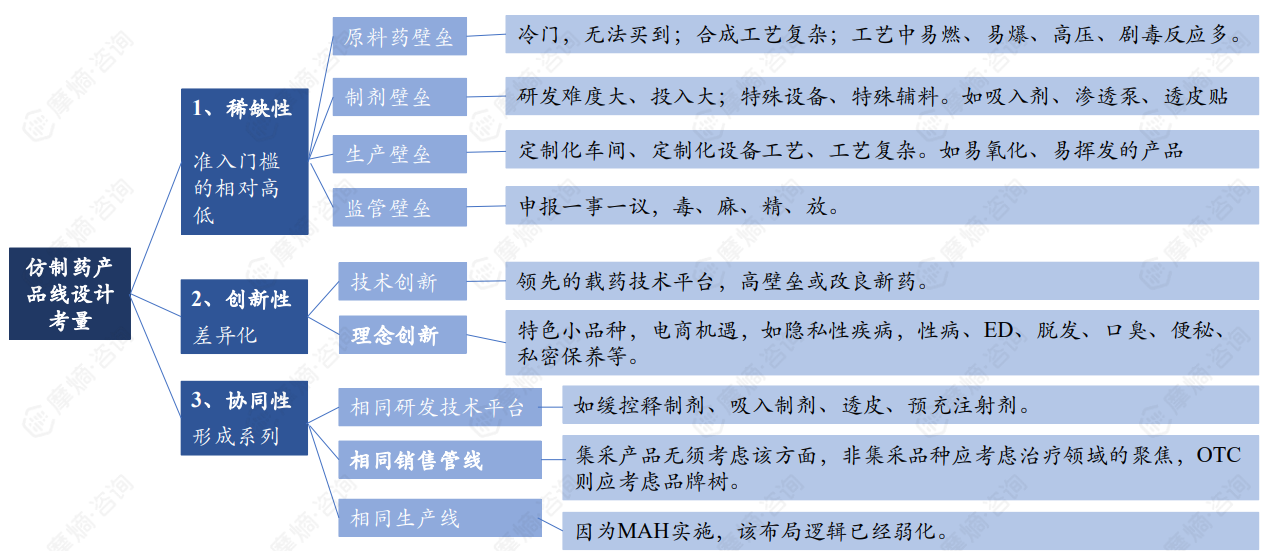
仿制药产品线设计需考量稀缺性、创新性(差异化)、与公司业务的协同性、延续性、前瞻性和技术可行性。 稀缺性体现在原料药和制剂壁垒,包括原料药的可及性、合成工艺复杂程度、生产设备和工艺的特殊性以及监管壁垒。创新性可通过领先的载药技术平台、特色小品种(如针对隐私性疾病的药物)以及理念创新来实现。协同性则体现在研发技术平台、销售管线和生产线的统一性。延续性需要考虑产品的升级和替代,以及渠道建设。前瞻性需要对政策、经济、治疗趋势、疾病谱变化和消费习惯进行预判。技术可行性则需要考虑合作研发、授权引进、贴牌代工和战略收购等多种途径。
信息获取渠道
评估信息可从以下渠道获取:
- 生物信息数据库: Genbank、RefSeq、UniProt、PDB等。
- 疾病基因组数据库: TCGA、OMIM等。
- 通路数据库: KEGG、Metacore、IPA等。
- 化学结构检索数据库: Scifinder、Reaxys等。
- 文献数据库: PubMed、Cochrane、Embase、Web of Science、知网、维普、万方等。
- 专利数据库: 中国国家知识产权局、欧洲专利局、美国专利局等。
- 临床试验数据库: ClinicalTrials.gov等。
- 药品监管和审批机构: FDA、EMA、NMPA等。
- 商业数据库: 摩熵医药、药渡、药智网、丁香园、米内网等。
- 制药公司官网
案例分析及要点总结
报告提供了三个案例分析:
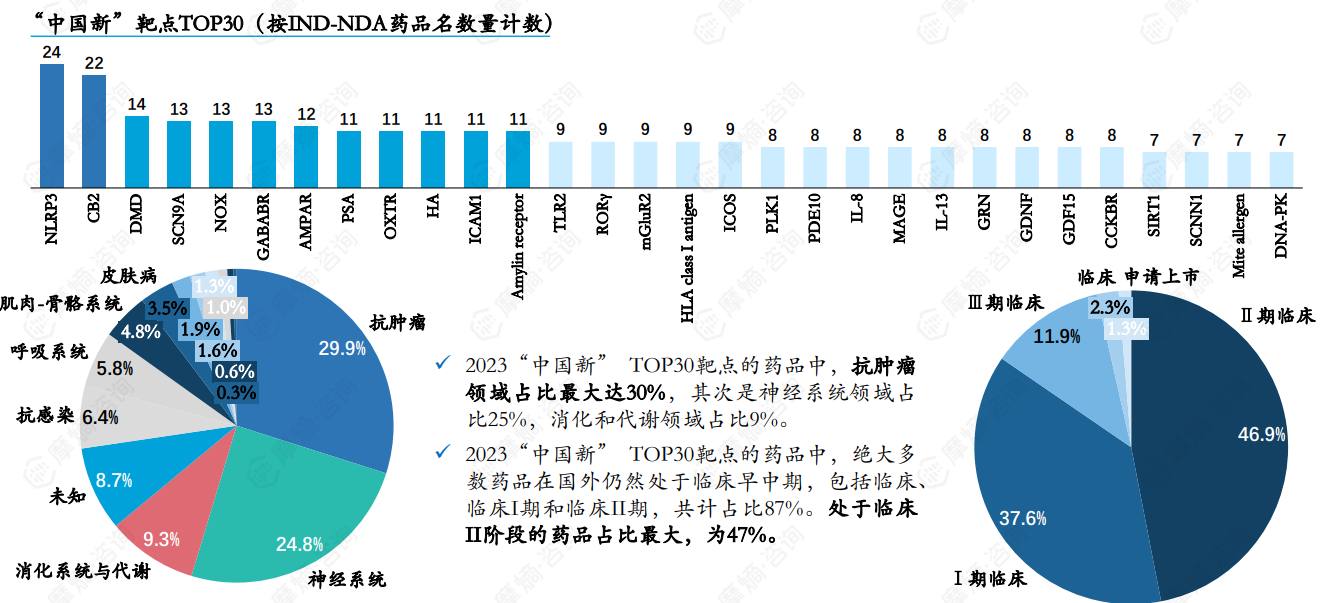
- 案例一:创新药——筛选2023“中国新”靶点: 通过比较全球和中国已有的药物研发靶点,筛选出在中国具有研发价值的“中国新”靶点,并分析其治疗领域和临床阶段分布。
- 案例二:儿童药——运用医疗大数据和KOL访谈进行市场规模和构成测算: 通过医疗大数据和KOL访谈,对中国儿童药物市场进行细分,并对不同细分领域的市场潜力进行量化评估。
- 案例三:仿制药——盐酸美金刚多奈哌齐缓释胶囊立项分析: 对盐酸美金刚多奈哌齐缓释胶囊的市场潜力、竞争格局、集采情况等进行分析,评估其立项的可行性。
总结
本报告系统地阐述了如何利用数据驱动高质量新药立项。通过对新药项目选择、评估、仿制药产品线设计以及信息获取渠道的详细分析,并结合具体的案例研究,为医药企业提供了科学、有效的立项决策方法。 “以终为始”的理念贯穿始终,强调了市场需求、技术可行性、风险评估以及公司战略在立项决策中的重要性。 充分利用大数据、KOL访谈、专利分析等多种手段,可以有效降低新药研发风险,提高立项成功率,最终实现高质量的成果转化和产业化。




-

ADC药物研发与市场全景研究报告
-

CAR-T药物研发与市场全景研究报告
-

2026年乳腺癌流行病学趋势及热门靶点药物市场表现洞察
-

2026年肝癌流行病学趋势及热门靶点药物市场表现洞察
摩熵咨询是摩熵数科旗下生物医药专业咨询服务品牌,由深耕医药领域多年的专业人士组成,核心成员均来自国际顶级咨询机构和行业标杆企业,涵盖立项、市场、战略、投资等从业背景,依托摩熵数科丰富的外部专家资源及全面的医药全产业链数据库,为客户提供专业咨询服务和定制化解决方案






最新报告
- 医药生物行业专题:MNC在CVRM赛道布局更新-海外制药企业2026Q1业绩回顾
- 基础化工行业周报:氟乐灵(华东)、硫酸(CFR西北欧)、丙烷(冷冻货,CFR华东)、新加坡汽油、新加坡石脑油价格涨幅居前
- 医药行业2026年中期投资策略:创新引领,多点开花
- 26Q1业绩环比改善,CGM海外销售持续突破
- 阿尔茨海默病药物研发与市场趋势研究报告
- 基础化工行业周报:4月份化学原料和化学制品制造业价格环比上涨8.3%,国际油价上涨
- 中国正畸行业概览:案例渗透增长,赛道大有可为
- 中国认知障碍康复设备行业概览:老年人口增长,如何满足市场对认知障碍康复设备不断上升的需求?
- 医药生物行业周报:新版药品管理法实施条例施行,市场独占期与数据保护制度落地
- 品牌运营业务稳健,坚定推进创新转型战略
对不起!您还未登录!请登陆后查看!
您今日剩余【10】次下载额度,确定继续吗?
请填写你的需求,我们将尽快与您取得联系
{{nameTip}}
{{companyTip}}
{{telTip}}
{{sms_codeTip}}
{{emailTip}}
{{descriptionTip}}
*请放心填写您的个人信息,该信息仅用于“摩熵咨询报告”的发送